JACS:合成“不可能”的分子——原甲酸
大约150年前,德国化学家Emil Erlenmeyer(就是发明了锥形瓶的那个Erlenmeyer)指出,同一个碳原子上携带一个以上羟基(-OH)的有机化合物极不稳定并且容易脱水。这也被称为“Erlenmeyer规则”。因此,制备那些一个碳原子上携带一个以上羟基的化合物(如:偕二醇(R2C(OH)2)、原羧酸(RC(OH)3)和原碳酸(甲烷四醇,C(OH)4))极具挑战性。例如,原羧酸(RC(OH)3)由于碳-氧双键相对于两个碳-氧单键的结合能更大并且相邻羟基的空间排斥作用导致其在热力学上极不稳定。如图1所示,甲二醇(CH2(OH)2)、原甲酸(CH(OH)3)和甲烷四醇(C(OH)4)均存在空间排斥,目前仅有甲二醇在气相中被检测到。此外,虽然原甲酸(1, CH(OH)3)尚未被监测到,但其结构异构体羟基过氧甲烷(2,CH3OOOH)和羟基过氧甲醇(3,CH2(OH)OOH)是存在于对流层的关键燃烧中间体(图2)。尽管羟基过氧甲烷2在对流层的寿命仅为20 ps,但其是单线态氧(1O2)、甲醛(H2CO)和过氧化氢(H2O2)等活性分子的主要来源。另一方面,大气臭氧(O3)与烯烃反应产生Criegee中间体(RR'COO),这不仅是大气化学、气溶胶生长背后的主要驱动力,也是环境羟基(ȮH)自由基的重要来源,后者反过来有助于2的生成;同时最简单的Criegee中间体——亚甲基(氧)氧鎓(H2COO)通过水合反应即可生成3。然而,计算结果表明1需要高能引发(如:光化学活化过程)才可形成,并且三种CH4O3异构体单分子分解成甲醇(CH3OH)和分子氧(O2)或H2CO和H2O2等产物时在热力学上均不稳定。
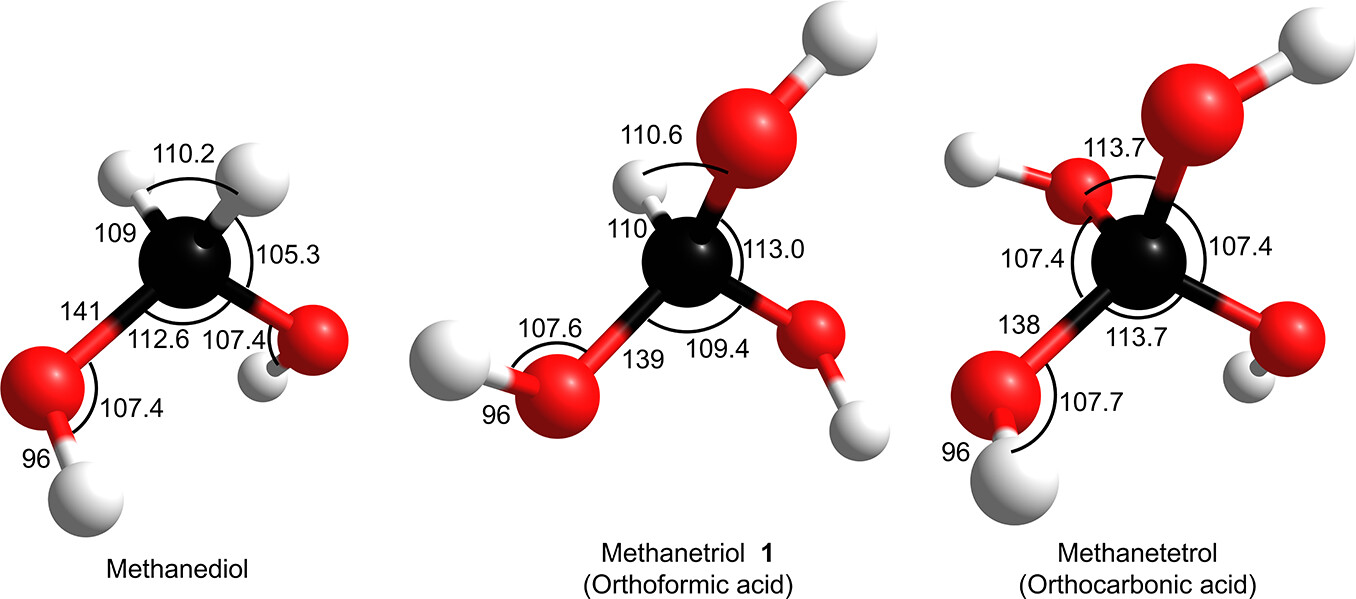
图1. 甲二醇、原甲酸和甲烷四醇最低能量构象异构体的结构。图片来源:J. Am. Chem. Soc.
近日,美国夏威夷大学马诺阿分校的Ralf I. Kaiser教授、美国佛罗里达国际大学的Alexander M. Mebel教授和华东师范大学的杨涛研究员合作,通过高能辐射首次在低温(5 K)和甲醇-分子氧(CH3OH-O2)混合冰中制备原甲酸(1)及其异构体羟基过氧甲烷(2)和羟基过氧甲醇(3),并在程序升温脱附(TPD)升华过程中利用真空紫外(VUV)光电离和反射飞行时间质谱(Re-ToF-MS)技术在气相中鉴定出三种异构体。相关成果发表在J. Am. Chem. Soc. 上。
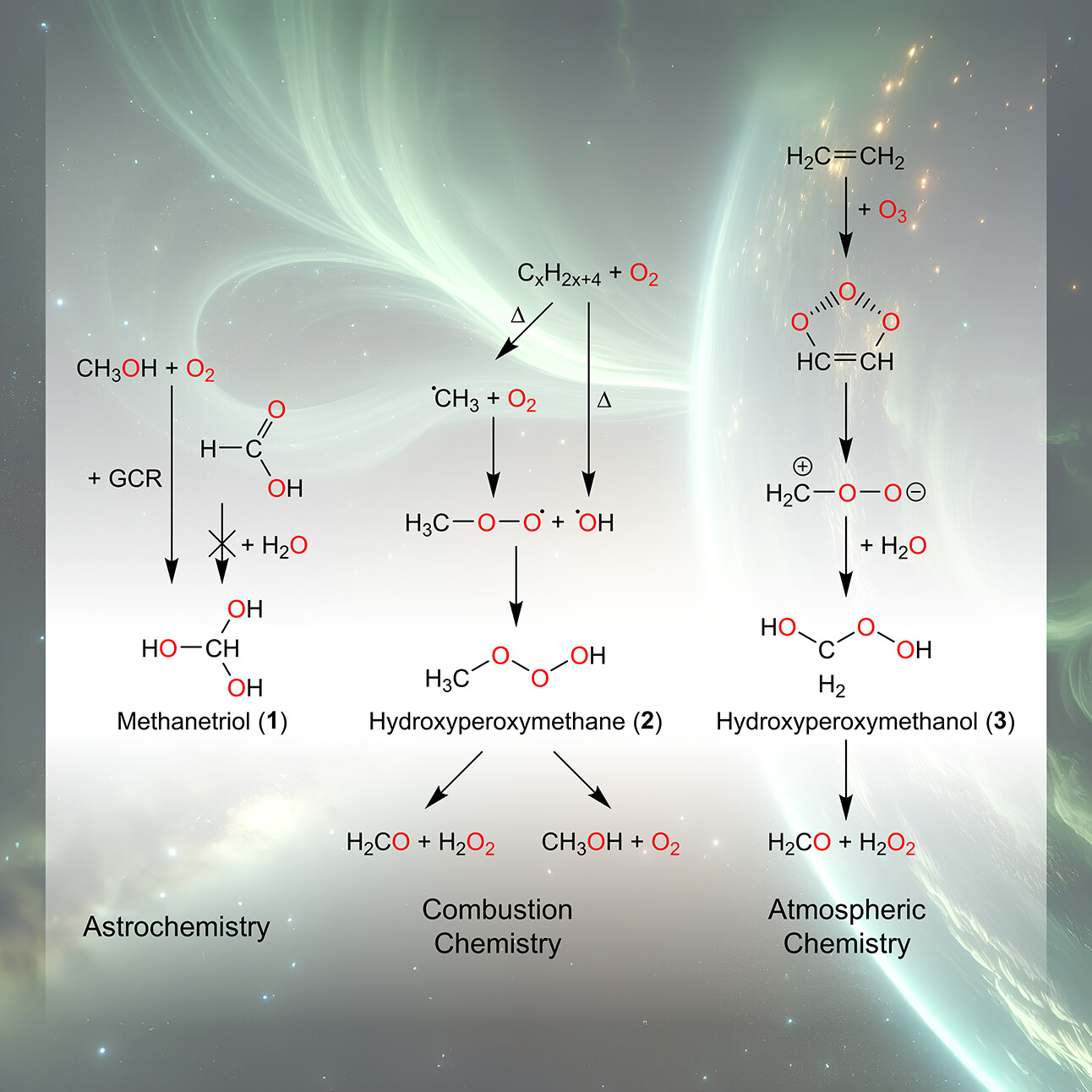
图2. CH4O3异构体的合成简介。图片来源:J. Am. Chem. Soc.
由于分子中存在吸电子基团(如:-OH)会促进自由基阳离子的解离倾向,因此作者通过计算量子化学预测原甲酸(1•+)、羟基过氧甲烷(2•+)和羟基过氧甲醇(3•+)自由基阳离子的解离方式。如图3所示,甲醇和分子氧(CH3OH-O2)在冰中绝热电离到最稳定trans-gauche-gauche构象1a•+态的阈值和C(OH)3+的表观能为10.79±0.04 eV,而垂直电离到gauche-gauche-gauche构象1b•+态为10.97±0.04 eV(图4),CH(OH)2+片段的表观能为11.03±0.04 eV,这些结果表明1可能会发生光电离解离。另外,对羟基过氧甲烷(2)和羟基过氧甲醇(3)的自由基阳离子解离动力学的计算研究表明两种异构体在光电离解离方面具有更强的稳定性,其中分子2仅有两个构象并且能量相差10±4 kJ mol-1,其绝热电离能约为9.77-9.95 eV。对于最稳定的阳离子(2a•+)而言,裂解过氧羟基(ȮOH)和质子化甲醛(H2COH+)之间的[H3CO-OOH]•+键所需的能量约为198 kJ mol-1,这主要是2a绝热或垂直电离的结果。然而,在单分子反应中反应物和产物之间没有确定的过渡态,并且能量随着OO键的延长而单调增加。如果2电离产生H2COH+,那么H2COH+的表观能为11.96±0.04 eV。相反,从3•+产生上述相同片段的解离通道需要裂解CO键而非OO键。对于该异构体,6个构象中的任何一种绝热电离能预期为9.65-9.87 eV,表观能为10.70±0.04 eV,这与实验值10.6-10.7 eV基本一致。尽管2(9.77-9.95 eV)和3(9.65-9.87 eV)可能绝热电离能的重叠范围阻碍单独使用光子能量进行异构体选择性光电离,但是新生离子的裂解可作为一种强有力工具来明确区分原甲酸及其异构体。
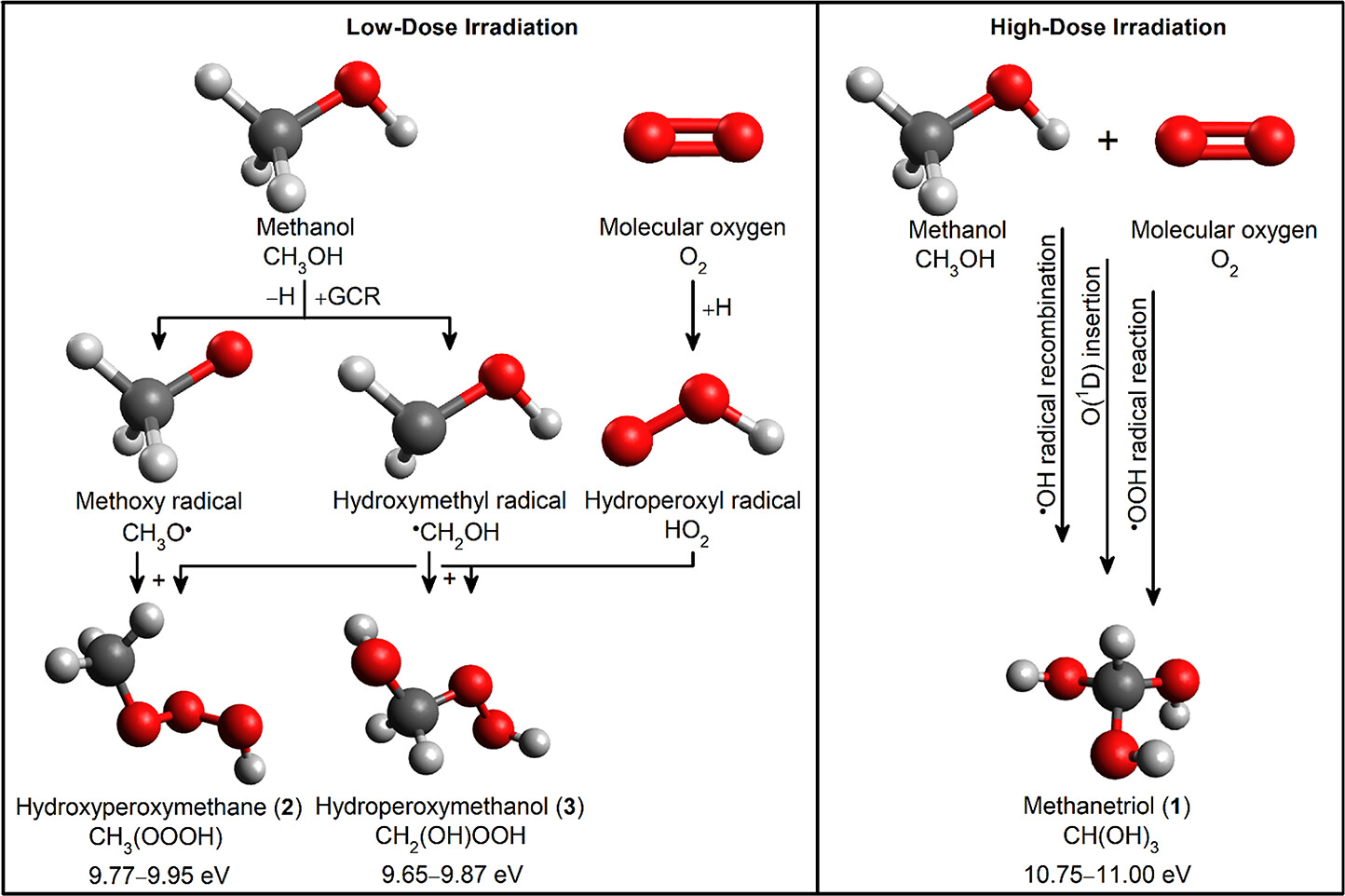
图3. 甲醇和分子氧(CH3OH−O2)在冰中的反应示意图。图片来源:J. Am. Chem. Soc.
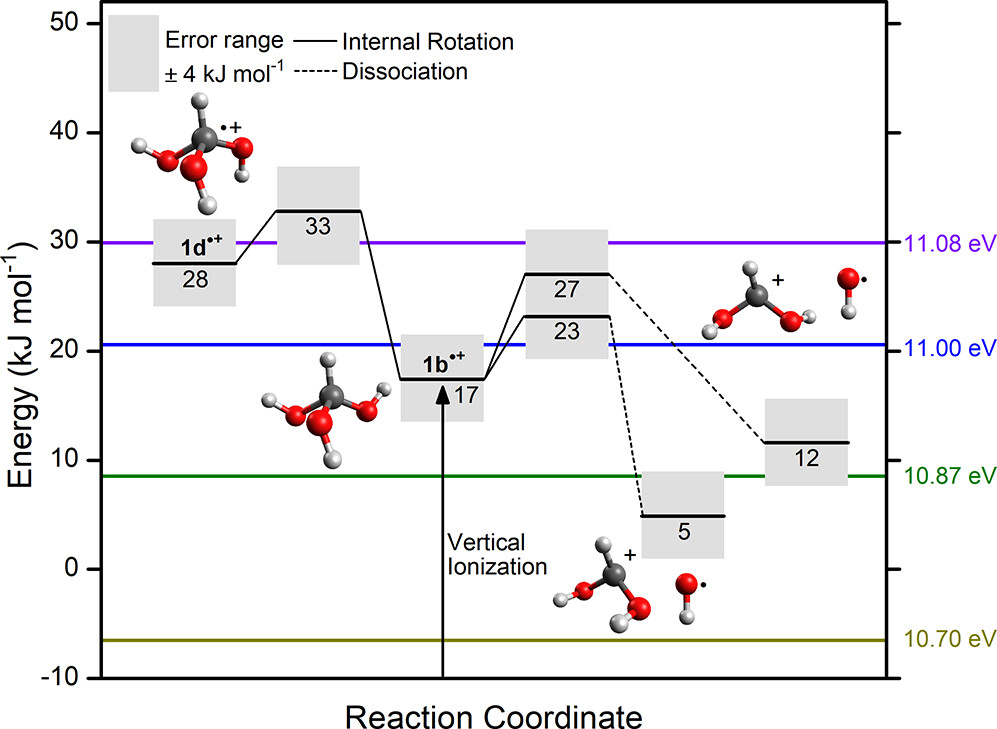
图4. CH(OH)3+·的势能面。图片来源:J. Am. Chem. Soc.
作者在甲醇-分子氧(CH3OH-O2)冰的程序升温脱附(TPD)过程中使用单光子光电离反射飞行时间质谱法(PI-ReToF-MS)进行分析(图5),结果显示空白对照试验(未辐照)中仅检测到甲醇阳离子(CH3OH+),而CH3OH-O2冰在11.08 eV下进行的质谱实验在m/z =47处观察到相关离子,而在m/z=63处没有发现相关离子。如图6a所示,在11.08和11.00 eV光电离下,CH(OH)2+片段在190 K时明显升华并且在11.00 eV下峰值强度降低6倍,这表明光电离解离过程非常接近其在11.00 eV时的阈值。其次,作者使用同位素标记的甲醇证实了m/z=47片段的分子式(图6b),并且该峰在13CH3OH-O2冰中发生变化(m/z=48),进而证实碎片中恰好存在一个碳原子;同时在CD3OD-O2冰中检测到m/z=50,进而证实了碎片中恰好包含三个氢原子。鉴于13C和D同位素标记结果中未标记物种的15 amu由碳和3个氢原子组成,因此32 amu的差值一定是两个氧原子。值得一提的是,所鉴定片段的分子式CH3O2与预测的1垂直电离解离相一致(图4),并表现出对波长变化的预测响应。
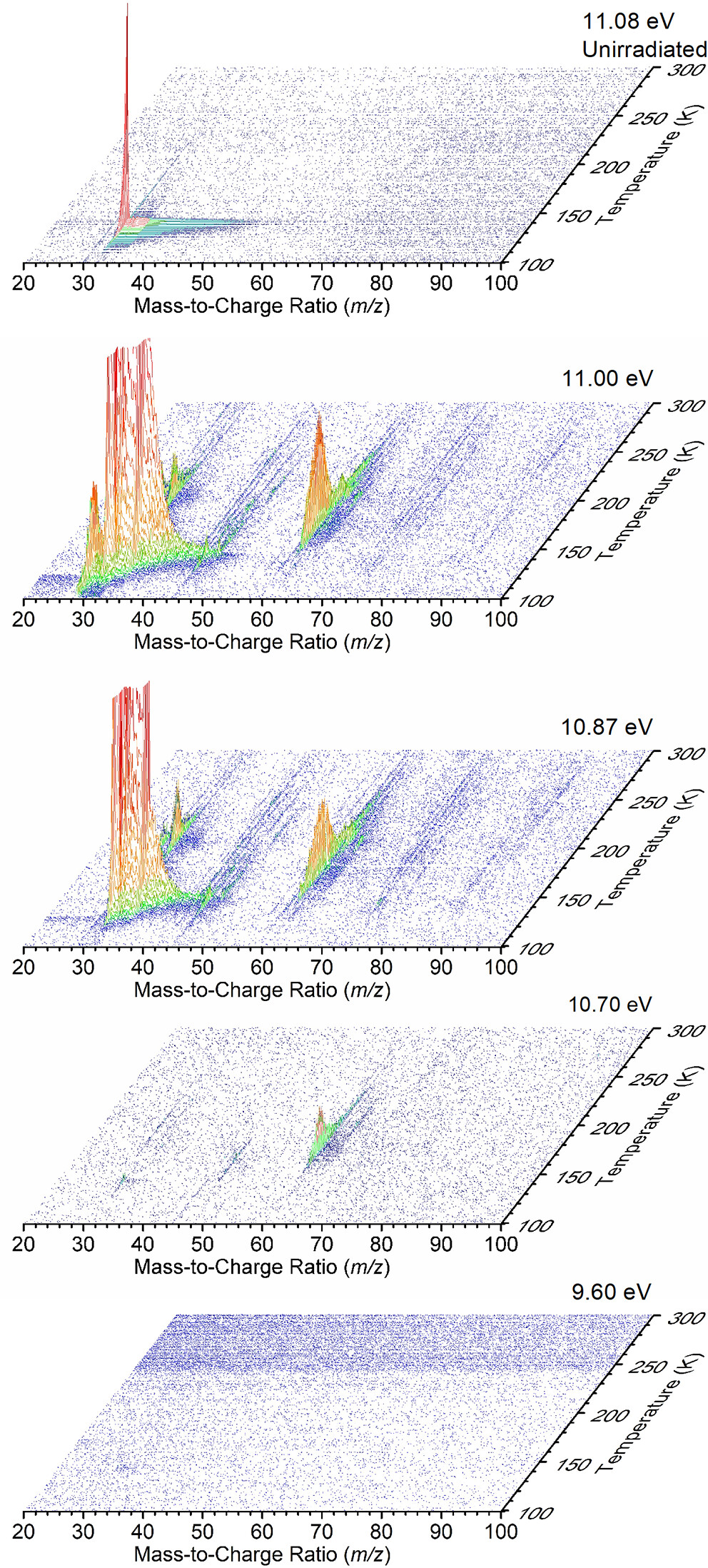
图5. CH3OH–O2冰在TPD过程中测量的质谱。图片来源:J. Am. Chem. Soc.
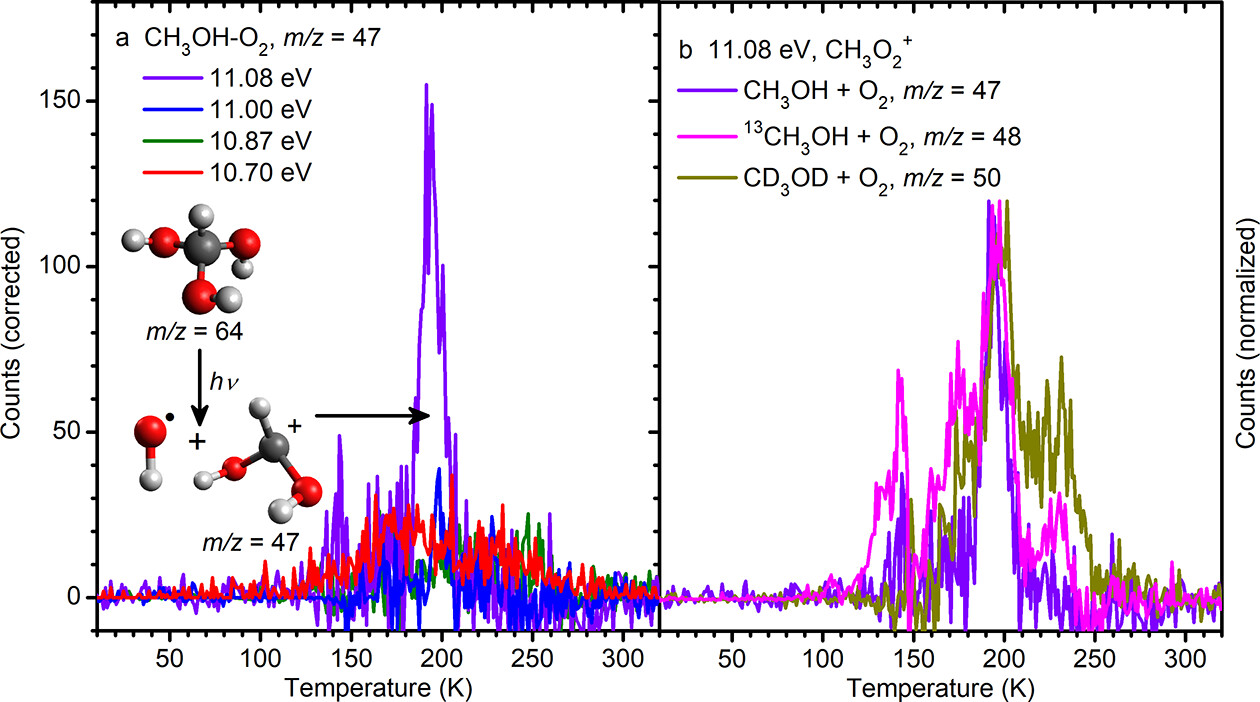
图6. 原甲酸片段的TPD图谱。图片来源:J. Am. Chem. Soc.
在确定化合物1存在后,作者专注于化合物2和3的制备。两种异构体的预测电离能(2:9.77-9.95 eV,3:9.65-9.87 eV)表明在9.50 eV时不能检测到离子,但在能量>9.95 eV时两种异构体均可检测到离子。如图7所示,当光子能量超过绝热电离时,在m/z=64处可以观察到两个峰。对于10.86、10.82、10.48和10.25 eV的光电离,在170 K和200 K处发现m/z=64的峰值,并且这两个峰值可以根据它们作为气相自由基阳离子的不同单分子分解势垒来区分,例如:200 K处的峰轮廓在m/z=31或64时是相同的,而在170 K仅观察到m/z=64峰(图8a)。类似地,作者采用同位素标记确定了m/z=64和m/z=31片段峰的分子式,并根据m/z=64和m/z=31片段峰的分子式将170 K处的峰归为化合物2,而将200 K处的升华事件归为化合物3(图8b-8e)。
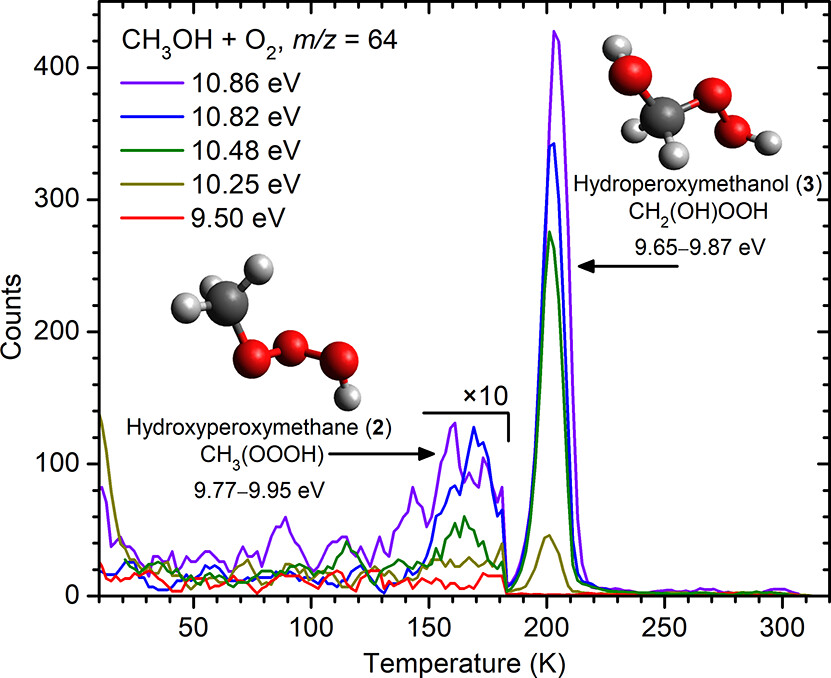
图7. m/z=64的TPD剖面。图片来源:J. Am. Chem. Soc.
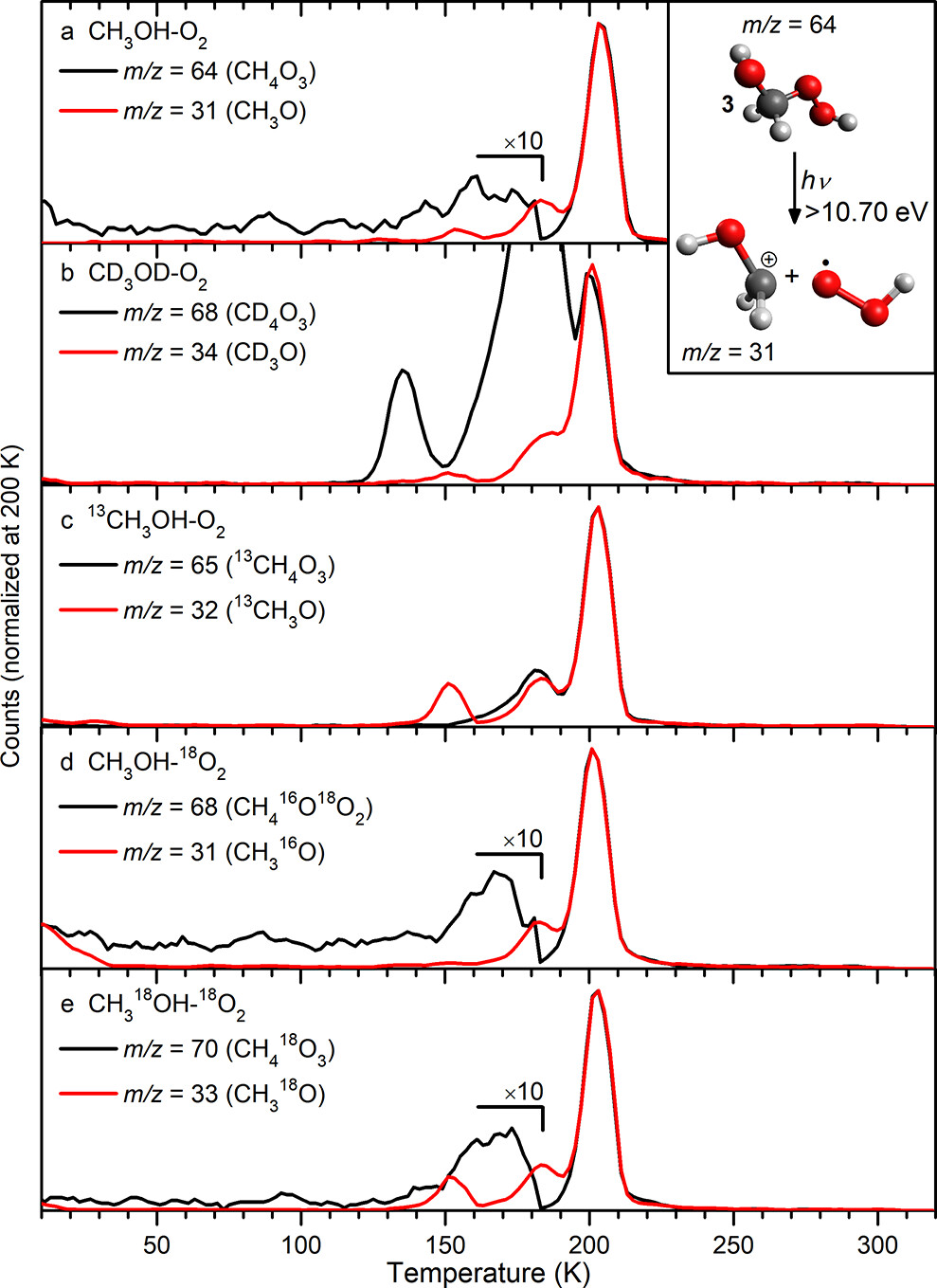
图8. CH4O3+和CH3O+同位素异构体在10.86 eV下光电离TPD谱。图片来源:J. Am. Chem. Soc.
随后,作者还研究了1和3的形成过程(图9)。首先,CH3OH在高能辐射下裂解C-H键形成相应的 H2OH和
H2OH和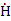 (反应[1a])以及CH3
(反应[1a])以及CH3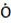 和
和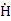 (反应[1b])。由于反应[1a]和[1b]吸热,因此必须在冰中进行并且在5 K进行辐照。接着,释放的氢原子(
(反应[1b])。由于反应[1a]和[1b]吸热,因此必须在冰中进行并且在5 K进行辐照。接着,释放的氢原子(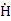 )与分子氧(O2)进行重组形成
)与分子氧(O2)进行重组形成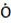 OH(反应[2]),此时这三种自由基可以通过反应[3]和[4]发生无障碍自由基-自由基重组并形成CH2(OH)OOH和CH3OOOH,CH2(OH)OOH(3)通过光电离解离生成羟甲基阳离子(CH2OH+)和
OH(反应[2]),此时这三种自由基可以通过反应[3]和[4]发生无障碍自由基-自由基重组并形成CH2(OH)OOH和CH3OOOH,CH2(OH)OOH(3)通过光电离解离生成羟甲基阳离子(CH2OH+)和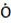 OH(反应[5]),其中CH2OH+片段的原子来源于CH3OH,而
OH(反应[5]),其中CH2OH+片段的原子来源于CH3OH,而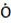 OH片段的原子源于分子氧。尽管由于缺乏碎片化导致2的形成机制不太确定,但是该异构体仅在CH316OH-18O2冰中观察到m/z=68峰,进而说明它也是由涉及反应1b、[2]和[4]的自由基-自由基重组机制形成。
OH片段的原子源于分子氧。尽管由于缺乏碎片化导致2的形成机制不太确定,但是该异构体仅在CH316OH-18O2冰中观察到m/z=68峰,进而说明它也是由涉及反应1b、[2]和[4]的自由基-自由基重组机制形成。

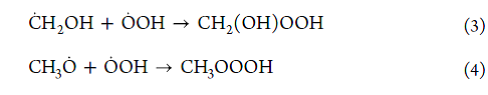
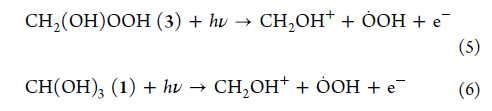
图9. 1和3的形成过程。图片来源:J. Am. Chem. Soc.
最后,作者对一系列分子CH4-n(OH)n(n=2,3,4,即甲二醇(CH2(OH)2)、1和甲烷四醇(C(OH)4))的最低能量构象进行了研究,并揭示了羟基之间的相互作用(图1)。虽然这些分子表现出相似的O-H和C-H键键长,但C-O键键长随着羟基数量的增加而减小,因此甲烷四醇的C-O键键长比甲二醇小3 pm,这说明尽管相应的自由基阳离子已经解离,但是羟基在中性分子中是相互增强的。此外,孤对电子价层电子对互斥理论(VSEPR理论)之间更大的空间排斥是影响这些物种键角的主要因素,例如:甲二醇的羟基相互排斥导致OCO角为112.6°,而氢产生的低排斥力导致OCH和HCH键角分别降低为105.3°和110.2°。
总结
本文研究团队通过高能辐射首次在低温(5 K)和甲醇-分子氧(CH3OH-O2)冰中制备原甲酸及其异构体——羟基过氧甲烷和羟基过氧甲醇,并在程序升温脱附升华过程中利用真空紫外光电离和反射飞行时间质谱技术在气相中鉴定出三种异构体。毫无疑问,原甲酸(CH(OH)3)的合成和检测对大气研究具有重要意义,该分子有可能参与大气有机气溶胶颗粒的形成。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Methanetriol─Formation of an Impossible Molecule
Joshua H. Marks, Xilin Bai, Anatoliy A. Nikolayev, Qi’ang Gong, Cheng Zhu, N. Fabian Kleimeier, Andrew M. Turner, Santosh K. Singh, Jia Wang, Jiuzhong Yang, Yang Pan, Tao Yang, Alexander M. Mebel, and Ralf I. Kaiser
J. Am. Chem. Soc., 2024, 146, 12174–12184. DOI: 10.1021/jacs.4c02637
(本文由吡哆醛供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号