JACS:双过渡金属电催化—脂肪羧酸的直接脱羧烯基化
在合成化学领域,烯烃是一种重要的基团,广泛应用于各类官能团化反应中,能够快速增加有机分子的复杂性。尽管烯基化反应研究已取得重大进展,但通过广泛易得、结构多样的原料合成结构多样的烯烃,尤其是向高度复杂的分子中引入烯烃,仍缺乏通用且具有化学选择性的方法。羧酸作为一种廉价易得、结构多样的原料,通过脱羧和催化成键过程,可将廉价羧酸直接衍生为高附加值化学品。2022年,Baran团队报道了电化学镍催化的活性酯脱羧烯基化合成萜烯的策略(Science, 2022, 375, 745,点击阅读详细),但这个过程需将羧酸预官能团化为氧化还原活性酯,这增加了反应步骤,限制了其应用。2015年,MacMillan团队报道了镍/光催化羧酸的脱羧烯基化反应(图1B),该策略适用于各种α-氧、α-氨基羧酸,但对于一级羧酸仍具挑战性。因此,开发一种新的催化策略,实现对简单一级烷基羧酸的直接脱羧烯基化,对于快速构建复杂烯烃具有重要意义。
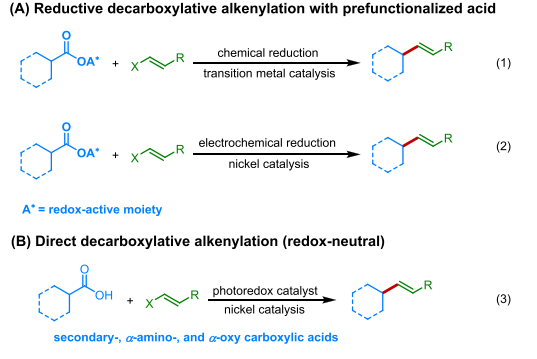
图1. 脱羧烯基化研究背景
有机电化学合成作为一种绿色合成方法,完美符合原子经济和绿色合成的要求。中国科学院化学研究所付年凯课题组最近报道了一种电光化学Ce/Ni双过渡金属催化的脱羧烯基化策略(图2)。这项成果发表于《美国化学会志》(J. Am. Chem. Soc.),通讯作者为中国科学院化学研究所付年凯研究员,第一作者为博士研究生鲁家庆,共同一作为直博生姚嫣、李浏博博士做出了重要贡献。

图2. 反应设计
作者采用了他们小组之前报道的电光催化脱羧芳基化条件进行了初步研究。遗憾的是,他们并未观察到预期的烯烃产物。通过仔细监测反应,他们发现在电解过程中产物先生成后被消耗了(图3),同时他们分离到对应的烯烃溴羟基化以及环氧化的副产物(SI)。通过反应条件的优化,他们发现向该体系中加入1.0当量的苯甲酸钾,可以显著提高反应效率,以75%的收率得到目标产物(entry 2)。

图3. 反应尝试及优化
在最佳条件下,他们对底物的适用性进行了研究(图4)。结果表明,该反应对乙烯溴化物的空间位阻不敏感,可以中等到良好的收率得到末端、1,1- 和1,2-二取代、三取代和四取代的烯烃(3和8-10)。对于各种烯基亲电试剂(-Cl、-Br、-I、-OTs、-OTf)均适用(11、15和23)。此外,该反应适用于一系列带有不同官能团的一级和二级烷基酸。为了验证该策略的实用性,他们将该策略应用到一些含羧基的药物分子,以良好的收率得到了对应的烯基化产物,如非天然氨基酸(45-47)、二肽(48)、琥珀酸单薄荷酯(49)、奥沙普秦(50)、吲哚美新(51)和胆酸(52-57)等衍生物。该策略可以很容易放大到克级规模(图5)。同时,他们发现将联吡啶配体换成市售的手性配体,能以超过99%的对映选择性得到目标产物(61)。

图4. 底物拓展
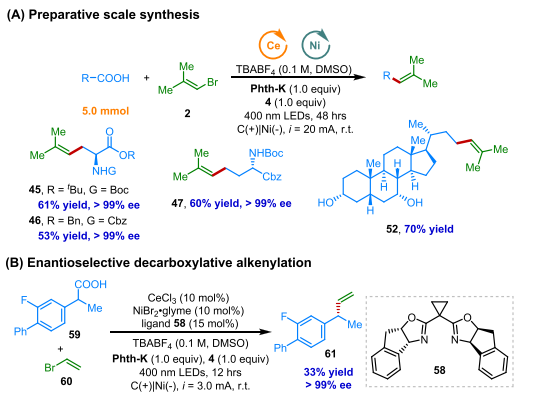
图5. 放大量反应及对映选择性合成
综合大量的机理验证,他们提出了可能的反应机理(图6),在阳极上,Ce(III) 74的形成使得Ce催化的过程在较低的阳极电位下进行,经过阳极氧化生成Ce(IV) 71后,通过LMCT过程进行脱羧反应,产生烷基自由基中间体72。在阴极上,还原镍催化剂启动镍催化循环,其中Phth-K起到了活化失活的镍寡聚物的作用,生成活性镍物种75,接着烯基亲电试剂与75发生氧化加成,得到Ni(III) 76,它可以快速地从阴极获得一个电子形成Ni(II) 73。苯甲酸根离子与镍中心的配位使得Ni(II)物种更加稳定,从而确保其从阴极脱离并捕获烷基自由基72。最后发生还原消除得到目标产物。
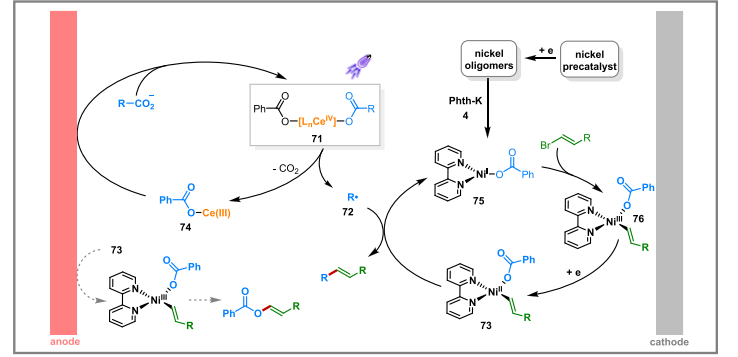
图6. 反应机理推测
小结
付年凯课题组报道了一种新型的双过渡金属光电催化脱羧烯基化反应体系。这种新的合成方法可以高效地制备高附加值的烯基化产物,并且可直接对复杂脂肪羧酸进行修饰。该反应适用范围广,易于放大规模制备,并且能够实现不对称的脱羧烯基化。详细的机理研究揭示了反应的关键中间体和途径。综上所述,这种新型的反应策略具有广泛的应用前景和重要的意义。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Dual Transition Metal Electrocatalysis: Direct Decarboxylative Alkenylation of Aliphatic Carboxylic Acids
Jiaqing Lu, Yan Yao, Liubo Li, and Niankai Fu*
J. Am. Chem. Soc., 2023, DOI: 10.1021/jacs.3c08839
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号