中山大学胡文浩课题组JACS:不对称多组分反应研究新进展
基于活性中间体的多组分反应,以其独特的优势,已经成为构建结构多样化化合物的有效方法之一。这种方法的核心在于利用活性中间体的特性,通过精确控制反应条件,实现对化学反应的高度选择性。卡拜(等价物)是一种同时具有卡宾和碳阳离子行为的中间体,它具备与多个组分同时成键的能力,理论上可使卡拜碳原子上一步形成三个σ键,这种特性使其在活性中间体参与的合成化学转化中具有巨大潜力(图1)。然而由于缺少合适的前体化合物分子以及精确控制反应选择性的方法,成功实现这类活性中间体高效转化的例子仍然很少,尚未有不对称控制研究的相关报道发表。

图1. 活性中间体参与的多官能团化反应研究
中山大学钱宇副教授(点击查看介绍)所在的胡文浩教授(点击查看介绍)课题组一直致力于金属卡宾等活性中间体参与的多组分反应研究,近日他们通过金属和手性质子酸的协同催化作用,实现了首例金属卡拜(等价物)参与的不对称多组分反应。这例反应揭示了金属卡拜(等价物)的独特反应性:即能够同时与两个亲核试剂和一个亲电试剂反应。研究以高价碘重氮作为卡拜前体化合物,首先通过金属铑催化形成金属卡拜(等价物),而后和醇/氨基甲酸酯作用生成叶立德中间体,随着离去基团脱离,叶立德中间体转化成为新的Fischer型杂原子金属卡宾,随后和另一分子醇/氨基甲酸酯作用第二次形成叶立德,最后与手性质子酸活化的亚胺分子实现不对称捕捉,即金属卡拜(等价物)—叶立德—金属卡宾—叶立德—亲电捕捉的全新转化途径,一步完成多个组分有序组装的全新化学,并实现了反应的高对映选择性控制(图2)。
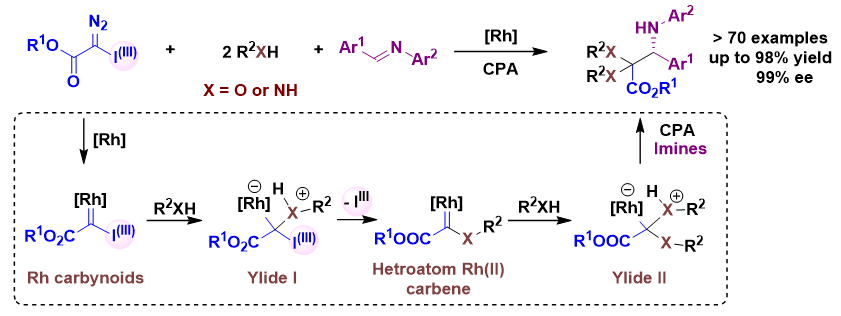
图2. 金属卡拜(等价物)不对称多组分捕捉新途径
为了研究和论证反应的机理,作者与中山大学柯卓锋教授团队合作进行了相关机理的理论计算研究。通过DFT计算,作者发现:a) 反应在第一次叶立德中间体形成后,转化成新金属卡宾的能垒A-IM2要低于发生捕捉反应的能垒B-IM2,也远远低于脱去金属形成碘(III)叶立德的能垒,而且整个反应过程能垒都是在往更加低的方向发展,这就使得后续的第二次叶立德形成成为可能,同时避免了更多副反应的发生;b) 作者通过对亲电捕捉二次叶立德中间体A-IM3加成过程中A-TS3两种构型的能垒计算,发现所得产物构型对应的A-TS3s能量是其中最低的。上述的计算结果很好的解释整个反应过程能够高效有序进行以及手性磷酸控制反应立体选择性的原因(图3)。

图3. 反应过程势能分布图及手性控制能垒
中山大学钱宇副教授、柯卓锋教授、胡文浩教授为本文的共同通讯作者,硕士研究生唐洁、博士后周晓雨、博士研究生罗健为共同第一作者,该项研究得到国家自然科学基金重大研究计划集成项目、面上项目、青年项目、广东省基础与应用基础研究基金以及广东省手性分子与药物发现重点实验室的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enantioselective Multi-Functionalization with Rh Carbynoids
Yu Qian*, Jie Tang, Xiaoyu Zhou, Jian Luo, Xiaoyan Yang, Zhuofeng Ke*, and Wenhao Hu*
J. Am. Chem. Soc., 2023, DOI: 10.1021/jacs.3c10460
导师介绍
钱宇
https://www.x-mol.com/university/faculty/65043
胡文浩
https://www.x-mol.com/university/faculty/49984
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号