西南交大高峰课题组:光诱导/钪催化的天然稀有Eupholathone型大戟二萜的仿生转化合成及抗HIV研究
近日,西南交通大学生命科学与工程学院高峰教授课题组与比利时鲁汶大学Rega医学院病毒研究所Dominique Schols教授以及乐山师范学院陈封政教授合作在Chem. Commun.在线发表天然产物领域研究论文,报道了大戟二萜仿生骨架转化研究最新成果。
大戟二萜因化学结构复杂、骨架繁多、生物活性多样显著,而备受天然产物研究领域的广泛关注。具有骈合5/7/7/4复杂环系的Eupholathone型大戟二萜在自然界中极为少见,仅有两例该类天然产物被报道。由于天然含量极低、提取分离困难,其生物活性研究尚是空白。合理解决稀有Eupholathone型大戟二萜的来源问题,将为其生物活性开发提供必要保障。高峰教授长期聚焦金属/光催化的天然药物化学研究(Angew. Chem. Int. Ed. 2023, 62, e202306326; Adv. Synth. Catal. 2022, 364, 1002; Bioorg. Chem. 2023, 131, 106329; J. Nat. Prod. 2023, 86, 939; J. Nat. Prod. 2022, 85, 2026; J. Nat. Prod. 2021, 84, 2374),在前期稀有大戟二萜骨架的仿生转化合成工作基础上(Org. Lett. 2023, 25, 597; Org. Lett. 2022, 24, 8598; Bioorg. Chem. 2023, 138, 106595; J.Org. Chem. 2022, 87, 13411; J. Nat. Prod. 2021, 84, 1838),受大戟二萜生源关系启发,以植物体内大量共存的5/11/3型续随子烷Euphorbia factor L1为原料,完成了天然稀有具5/7/7/4环系Eupholathone型大戟二萜的仿生骨架转化合成研究。
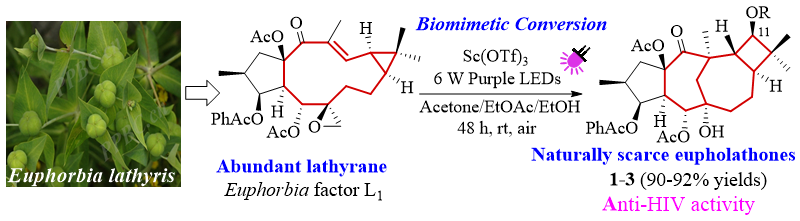
图1. 光诱导/钪催化的续随子烷向天然稀有Eupholathone型二萜仿生骨架转化合成
通过Sc(OTf)3促进可见光催化的串联式重排反应,以来源丰富的续随子烷型大戟二萜Euphorbia factor L1为原料,采用丙酮作为反应溶剂,成功地制得天然稀有的Eupholathone型骨架重排产物Euphornin E(1)(R = OH)(图1)。当反应溶剂更换为乙酸乙酯或乙醇时,分别以优秀的收率得到C11位由相应不同基团亲核加成的Eupholathone型产物2(R = OAc)和3(R = OEt)。反应机理推测,反应溶剂或空气中的水参与该反应进程,此转化过程可能涉及串联光异构化/Michael加成/SN2/Wagner-Meerwein重排反应。随后,在与比利时鲁汶大学Rega医学研究院病毒所Dominique Schols教授团队合作开展的抗HIV大戟二萜研究工作中发现,Eupholathone型骨架表现出潜在的抗病毒活性,化合物1具有良好的抗HIV-1作用。本研究从化学角度论证了续随子烷与Eupholathone大戟二萜间的生源关系;也为稀有Eupholathone型二萜的高效转化合成提供一条简明路径,解决了稀缺化合物来源问题,同时为Eupholathone型抗HIV活性大戟二萜的深度挖掘奠定基础。
该论文第一作者为徐巾卜博士后和温鹏硕士,通讯作者为乐山师范学院陈封政教授和西南交通大学高峰教授。该研究工作得到了国家自然基金面上项目(22277101)的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Photo-Induced Scandium-Catalyzed Biomimetic Skeleton Conversion of Lathyrane to Naturally Rare Eupholathone Euphorbia Diterpenes
Jin-Bu Xu, Peng Wen, Neng Wang, Xiaohuan Li, Jia-Hong Li, Steven De Jonghe, Dominique Schols, Feng-Zheng Chen*, Feng Gao*
Chem. Commun., 2023, DOI: 10.1039/D3CC03541G
导师介绍
高峰
https://www.x-mol.com/university/faculty/186036
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号