适配体驱动DNA瓦片自组装

图1. AMP适配体驱动DNA线性结构的自组装。
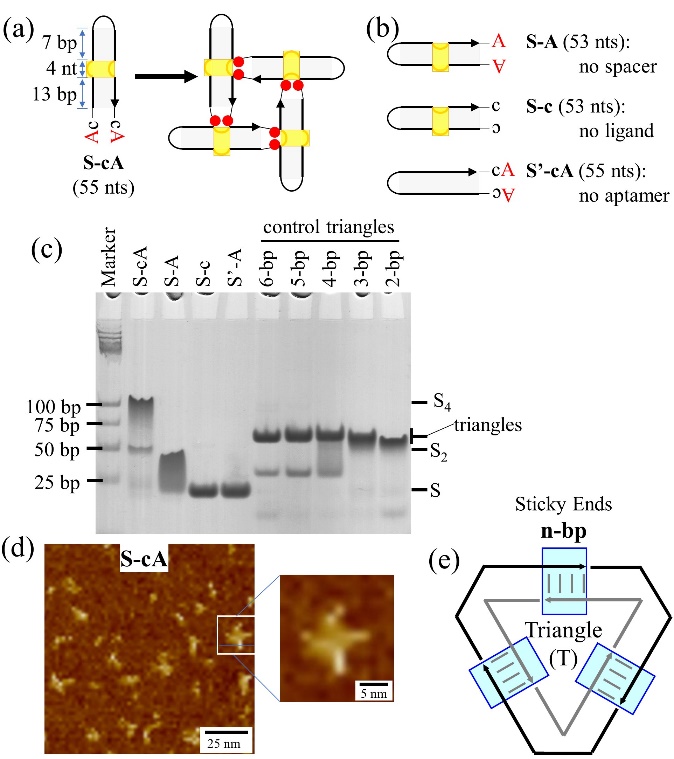
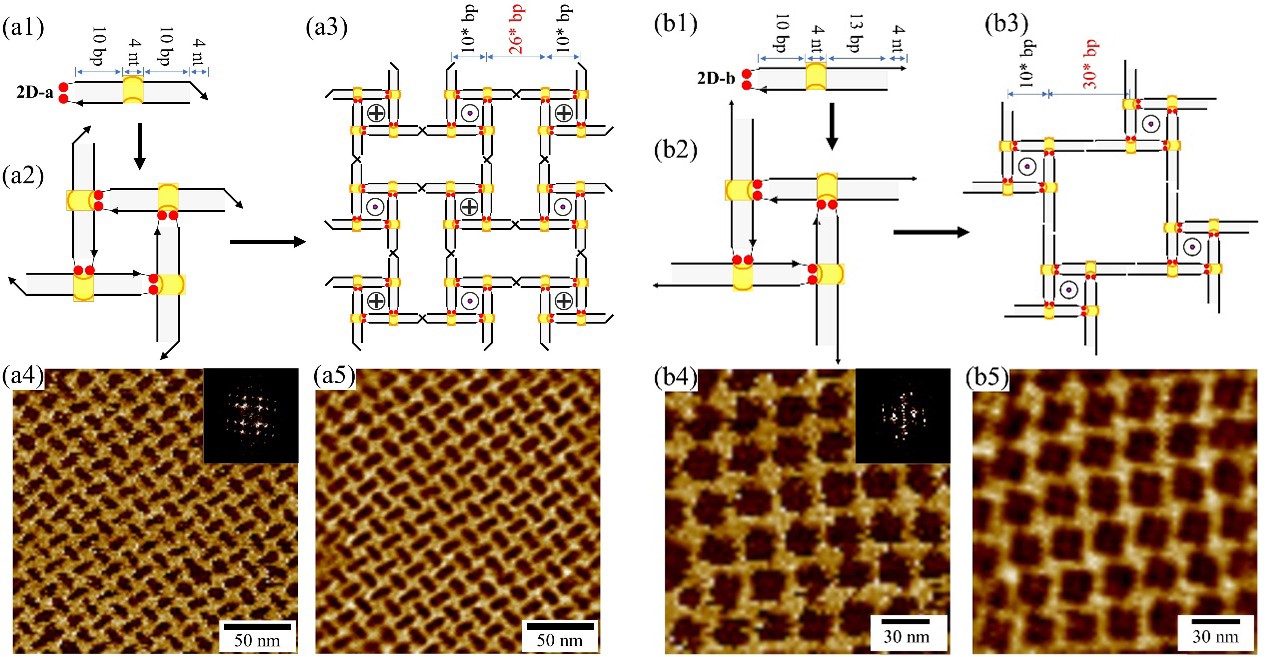

AMP Aptamer Programs DNA Tile Cohesion without Canonical Base Pairing


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
相关文章
-
大尺寸手性DNA纳米管的自组装 2020-01-08
-
“种子”链程序化调控DNA纳米结构的组装 2020-04-11
-
预组织的刚性核酸二价适配体的设计策略 2022-03-30
-
西南大学药学院团队发现pH-响应的DNA基序的一般设计原则 2019-11-28
































 京公网安备 11010802027423号
京公网安备 11010802027423号