生物正交反应介导的CRISPR/Cas9靶向递送系统用于固有免疫和适应性免疫的双重激活
近年来,CRISPR/Cas9系统在肿瘤免疫治疗中的应用引来越来越多的关注。然而,目前尚缺乏有效的靶向肿瘤部位递送CRISPR/Cas系统的工具,这使得CRISPR/Cas系统的体内高效安全递送面临巨大挑战,严重制约着其临床应用。日前,南京大学宋玉君教授团队与南京中医药大学韩欣教授团队合作,利用生物正交反应实现CRISPR/Cas9系统在肿瘤部位的靶向递送,并通过同时激活固有和适应性肿瘤免疫,实现良好的抗肿瘤效果。
首先,制备同时具有高药物负载效率及肿瘤微环境响应性质的空心二氧化锰纳米材料(H-MnO2),用于实现生物正交前体(Ac4ManNAz)在肿瘤部位的特异性释放,并通过参与肿瘤细胞糖代谢过程对肿瘤部位选择性的标记。利用该标记策略,可克服天然标志物受体数量有效的缺点,亦可对缺少特异性标志物的肿瘤进行改造。随后,负载CRISPR/Cas系统的脂质纳米材料(DBCO-Lipo/p)通过生物正交反应聚集在肿瘤组织,提高了CRISPR/Cas系统在肿瘤部位的积累和基因编辑活性,减少了非目标器官的编辑效应。
此外,Ac4ManNAz/H-MnO2@Gel和DBCO-Lipo/p的联合应用还依次激活了固有免疫和适应性免疫系统,在活体实验中展现出卓越的抗肿瘤效果。Ac4ManNAz/H-MnO2@Gel在肿瘤部位降解释放Ac4ManNAz的同时,也会原位释放出Mn2+,激活肿瘤部位细胞的cGAS-STING通路,逆转肿瘤微环境免疫抑制状态,将“冷”肿瘤转变为“热”肿瘤。而DBCO-Lipo/p通过点击化学反应聚集于肿瘤部位,可同时敲除肿瘤部位免疫细胞及肿瘤细胞中的Ptpn2基因,增强T淋巴细胞增殖及肿瘤细胞对IFN-γ的敏感性。
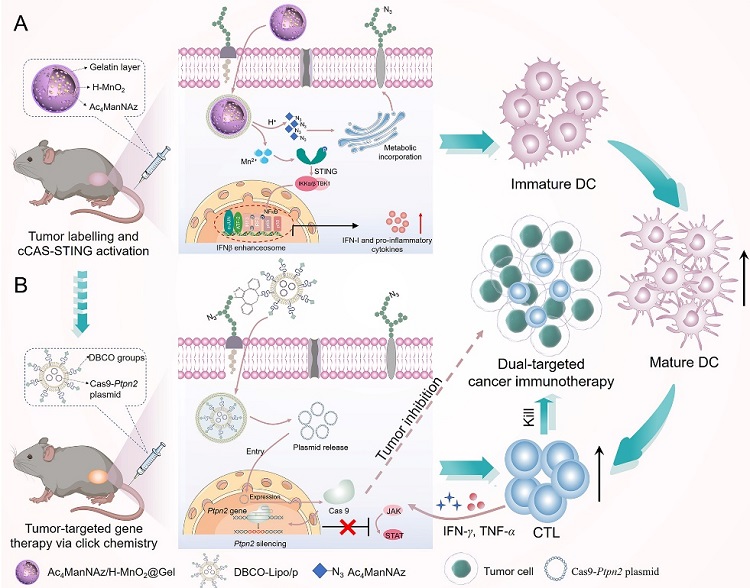
图1. 通过生物正交反应实现CRISPR/Cas系统的靶向递送及级联免疫激活示意图
在细胞层面,生物正交反应可有效增强CRISPR/Cas9系统在肿瘤细胞中的编辑效率。在活体层面,该生物正交反应介导的CRISPR/Cas9肿瘤靶向递送策略可有效敲低目标基因的表达并激活抗肿瘤免疫,为CRISPR技术用于肿瘤免疫治疗转化应用提供了有力支撑。
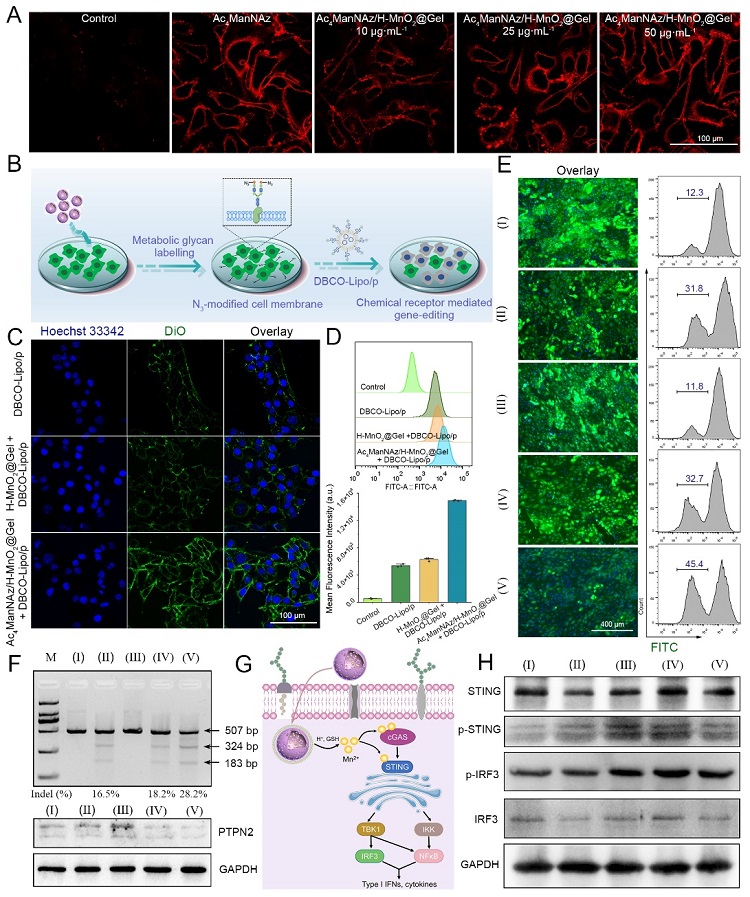
图2. Ac4ManNAz/H-MnO2@Gel和DBCO-Lipo/p的联合应用可有效增强CRISPR/Cas9系统在目标细胞中的编辑效率,并激活cGAS-STING通路
这一成果近期发表在Angewandte Chemie International Edition 上,文章的通讯作者为南京大学宋玉君教授及南京中医药大学韩欣教授,第一作者为南京中医药大学副教授杨婧婧及青年教师杨开勇。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Bioorthogonal Reaction-Mediated Tumor-Selective Delivery of CRISPR/Cas9 System for Dual-Targeted Cancer Immunotherapy
Jingjing Yang, Kaiyong Yang, Shiyu Du, Wen Luo, Chao Wang, Hongmei Liu, Kunguo Liu, Zhibin Zhang, Yanfeng Gao, Xin Han, Yujun Song
Angew. Chem. Int. Ed., 2023, DOI: 10.1002/anie.202306863
导师介绍
宋玉君
https://www.x-mol.com/groups/song_yujun
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
















































 京公网安备 11010802027423号
京公网安备 11010802027423号