Nano Res.[生物]│齐宪荣教授团队:仿生免疫激活剂共呈递自噬促进和共刺激分子用于协同癌症免疫治疗的研究
本篇文章版权为齐宪荣教授团队所有,未经授权禁止转载。
背景介绍
手术切除是治疗原发实体肿瘤的常用方法,但是,手术残留肿瘤细胞的微转移,以及循环肿瘤细胞(CTC)常常导致肿瘤复发和治疗失败。通过刺激免疫反应,利用自身免疫系统清除剩余的肿瘤细胞和CTC是一个非常值得探索的方向。然而,肿瘤免疫抑制微环境(TIME)中的弱免疫原性和受损的T细胞浸润限制了免疫效果。迫切需要重编程TIME、有效识别和清除残留肿瘤细胞和激活免疫的新策略。
成果简介
本研究构建了一种以血小板(PLT)为基础的共同递送自噬诱导肽(Bec1)和GITR激动剂(DTA-1)的原位仿生免疫激活剂(PLT-Bec1/DTA-1),它具有血小板在肿瘤募集和激活方面的天然优势。PLT-Bec1/DTA-1作为自触发释放库,通过血小板微粒(PMPs)的分泌,深度递送联合免疫增强剂Bec1和DTA-1,通过自噬诱导和GITR触发的TReg抑制,重塑肿瘤免疫微环境。结果显示,PLT-Bec1/DTA-1促进了抗原呈递和T细胞增殖,逆转了肿瘤抑制环境中BMDCs的免疫抑制状态,提高了CD8+T/TReg比率,抑制了小鼠肿瘤手术切除模型中的肿瘤复发。并且PLT-Bec1/DTA-1通过原位免疫激活阻止了肺部肿瘤定植。我们的研究结果强调了通过仿生载体递送自噬诱导剂与免疫激活剂,引发肿瘤微环境中效应免疫细胞自动原位激活以根除肿瘤的合理性与有效性,为改善癌症免疫治疗以克服临床应用方面的瓶颈提供了广阔的前景。
图文导读
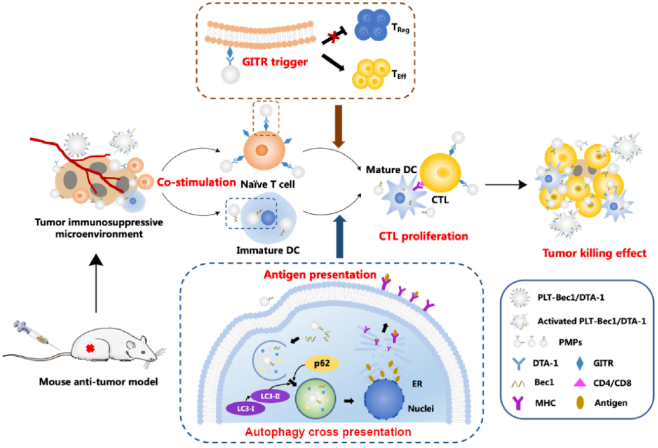
PLT-Bec1/DTA-1是一种原位仿生免疫激活剂,具有血小板对肿瘤募集和激活的天然优势。它在肿瘤部位特异性释放货物,通过自噬诱导和GITR触发促进DC抗原呈递和T细胞活化,改善肿瘤免疫抑制微环境并消除肿瘤。
作者简介
通讯作者:齐宪荣,教授、博士生导师。长期从事纳米材料与技术在肿瘤治疗领域的研究。作为第一作者和通讯作者已在《NanoToday》、《ACS Nano》、《Biomaterials》、《Journal of Controlled Release》、《NPG Asia Materials》、《Advanced Healthcare Materials》等国内外期刊发表论文140余篇,研究成果多次获得省部级奖励。
第一作者:彭祎玮,北京大学药学院药剂学博士研究生。主要研究方向为纳米药物靶向递送与抗肿瘤治疗。
文章信息
Peng Y, Yang Y, Yang Z, et al. Bionic immunoactivator copresenting autophagy promoting and costimulatory molecules for synergistic cancer immunotherapy. Nano Research, 2023, https://doi.org/10.1007/s12274-023-5933-2.

识别二维码或点击左下角“阅读原文”可访问全文

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号