浙工大Nat. Commun.:环肽构建及多肽偶联药物领域新进展
环肽类物质其实是一种结构独特、生物活性范围广泛、作用机理独特的环型化合物。与线性肽相比,环肽的构型稳定、亲和力强、代谢稳定性高,因而具有更强的药理特性,在抗肿瘤、抗病毒等新药研发中广受关注。但当前环肽的构建主要是通过氧化、缩合等反应,在氨基酸残基侧链活泼官能团上进行环化反应,结构较为单一,并且容易改变多肽的生物功能。利用C-H功能化反应实现复杂分子末期修饰的研究思路,可拓展环肽的结构多样性,进一步提高环肽的生物稳定性和活性,有助于深入挖掘环肽药物先导物,为开发具有自主知识产权的新药研发奠定良好基础。
浙江工业大学生物工程学科朱勍教授(点击查看介绍)团队打破常规环化策略的局限性,利用过渡金属铑作为催化剂,在温和的条件下成功实现了多肽色氨酸惰性C(7)-H键上位点特异性马来酰亚胺环化,活性氨基酸,如天冬氨酸、谷氨酸、精氨酸、丝氨酸、赖氨酸等的存在皆不影响反应,表现出很好的底物兼容性,并制备了22-41元环的环肽。课题组还利用色氨酸取代的马来酰亚胺与巯基的点击反应特性,发展了一种快速、高效构建多肽偶联药物的独特方法,表明其作为点击官能团在化学生物学和药物化学中的潜力。并以整合素靶向多肽RGD为例,通过色氨酸C(7)-H的马来酰亚胺环化反应构建了具有高整合素亲和性的RGD环肽,然后通过与含巯基阿霉素之间的生物正交反应成功构建了多肽药物偶联(PDC) RGD-GFLG-DOX,并经分子互作、流式细胞术及竞争性等实验,验证了该PDC药物化合物比常用的DOX具有更好的选择性、结合亲和力和抗肿瘤细胞增殖活性。这种快速制备订书肽的策略可能成为构建PDC的强大工具。
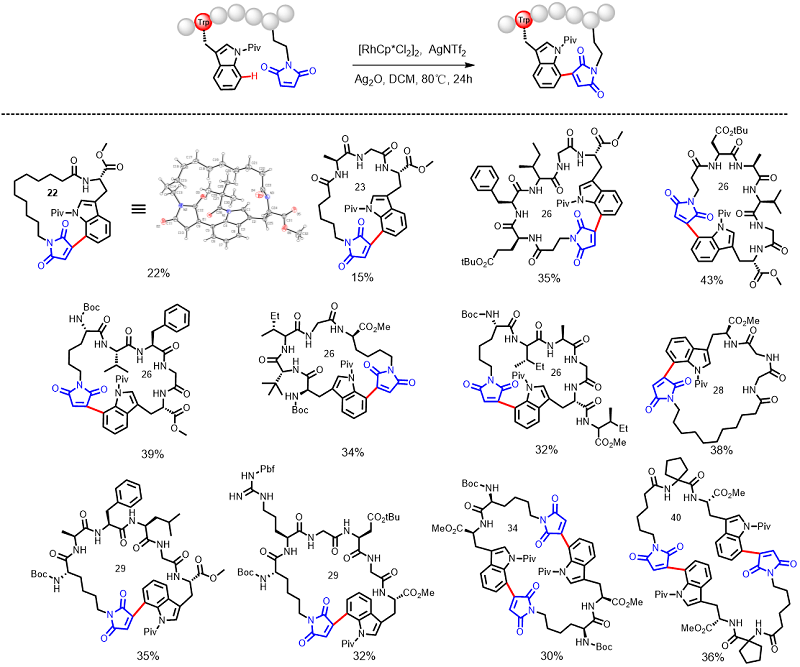
图1. 过渡金属铑催化色氨酸C(7)-H键马来酰亚胺环化反应
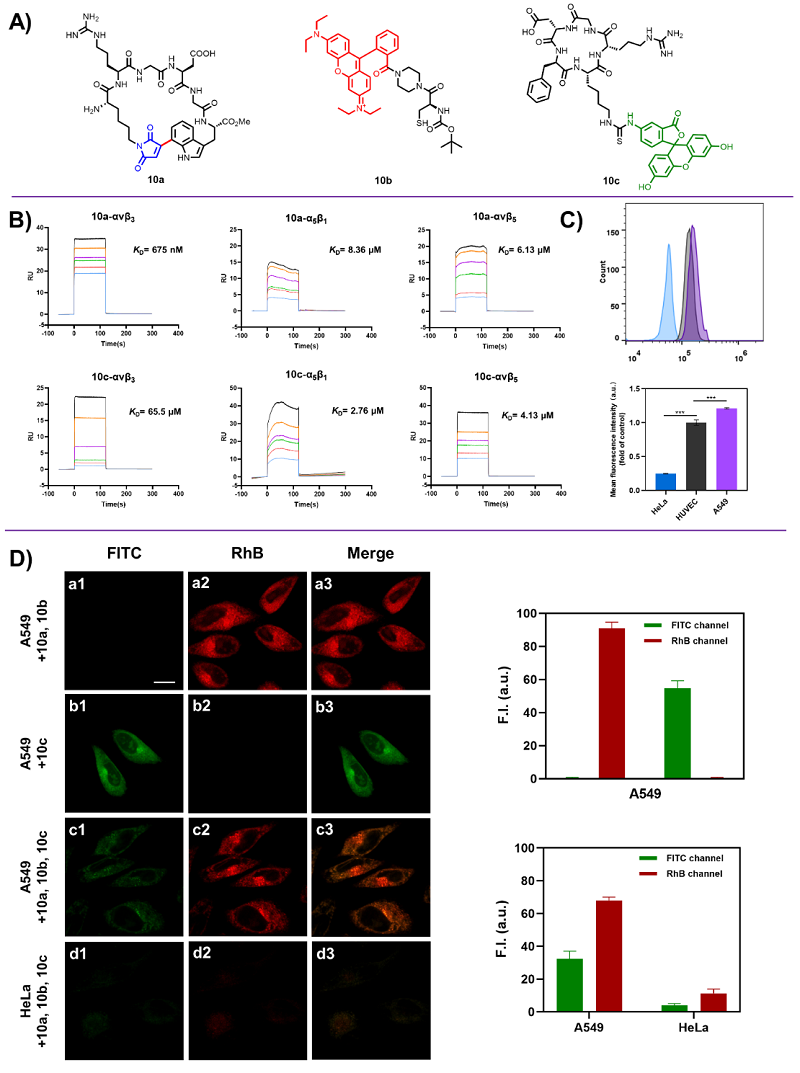
图2. RGD-GFLG-DOX与DOX的分子互作、流式细胞术及竞争性实验
上述成果近日发表于《自然-通讯》(Nature Communications)。在读博士研究生王鹏为第一作者,博士刘江和在读研究生朱小梅为论文共同第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Modular synthesis of clickable peptides via late-stage maleimidation on C(7)-H tryptophan
Peng Wang, Jiang Liu, Xiaomei Zhu, Kenry, Zhengqing Yan, Jiahui Yan, Jitong Jiang, Manlin Fu, Jingyan Ge, Qing Zhu & Yuguo Zheng
Nat. Commun., 2023, 14, 3973, DOI: 10.1038/s41467-023-39703-y
朱勍博士简介

浙江工业大学生物工程系教授,2001年于浙江大学取得博士学位,2001-2005年在新加坡国立大学化学系、美国哥伦比亚大学化学系工作,2005年7月起就职于浙江工业大学。
研究领域是基于C-H功能化的复杂分子末期修饰及小分子活性探针开发应用研究。在J. Am. Chem. Soc.、Nature Commun.、ACS Appl. Mater. Interface、Chem. Commun.等国际期刊上发表相关SCI论文40余篇;主编参编书和教材1部;授权专利30余项。
https://www.x-mol.com/university/faculty/149963
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!














































 京公网安备 11010802027423号
京公网安备 11010802027423号