Angew:胞外miRNA响应性人工DNA受体用于生物标记物驱动的治疗
精准医疗的目标是开发针对特定病理状态自动响应的治疗策略,旨在提高疗效、特异性和安全性。疾病相关生物标志物在疾病诊断和预后中起着至关重要的作用。已经开发了许多智能设备来有效地感知生物标志物并自动评估疾病状态,从而产生响应性治疗。然而,这些设备大多依赖于体积庞大的电子元件或转基因细胞,缺少自动响应疾病生物标志物并执行治疗功能的分子设备。胞外微小RNA (miRNA) 是一类小的非编码核酸分子,因其作为新型生物标志物和信号分子的潜力而越来越受到关注。局部释放的细胞外miRNA可以提供病理进展的原位实时信息,有可能促进基于生物标志物的疾病评估和响应性治疗。但由于缺乏对miRNA响应的天然或人工受体,实现胞外miRNA病理生物标志物驱动的精准治疗仍具挑战。
近日,湖南大学化学化工学院的聂舟(点击查看介绍)课题组结合动态DNA纳米技术和功能核酸分子,成功开发了一种非遗传改造的miRNA响应性嵌合DNA受体 (miRNA-responsive Chimeric DNA Receptor, miRNA-CDR),实现了由生物标志物驱动的活体治疗(图1)。该miRNA-CDR由传感器模块和执行器模块组成,通过核酸适配体锚定到天然膜受体上,可感知细胞外miRNA水平,通过miRNA驱动的互补介导的链置换反应(miRNA-driven Complementary-mediated Strand Displacement reaction, miRNA-CSD) 引起DNA的动态自组装,进而诱导二聚化介导的受体激活。该模块化的miRNA-CDR平台是高度可定制的,能够以可调的灵敏度响应用户定义的miRNA输入,实现指定的受体信号输出。此外,miRNA-CDR装置对同一细胞群体中的两种指定miRNA以正交方式促进不同受体信号传导。最终,miRNA-CDR可用于药物诱导急性肝损伤(DILI)的原位修复和肝功能恢复。
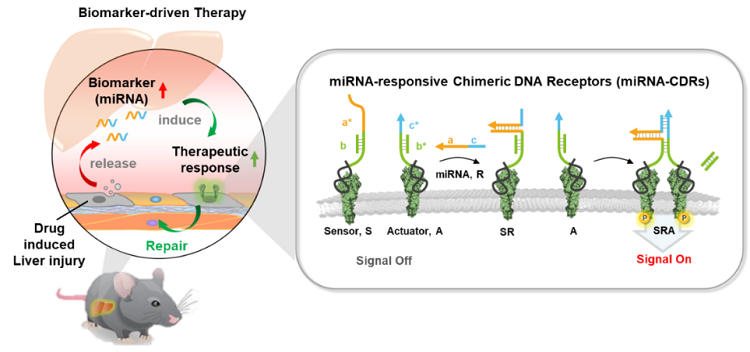
图1. miRNA响应性嵌合DNA受体(miRNA-CDR)作为肝损伤生物标志物驱动的治疗纳米设备的分子工程示意图。
为了探索miRNA驱动的miRNA-CSD反应的可行性,作者在活细胞膜上构建了miRNA-CSD系统,其传感器模块中的茎结构域(Stem)长度影响与miRNA靶标结合的亲和力,执行器模块中的Toehold结构域长度影响反应的速率,作者对这两个模块进行了优化,最终确定14 nt 茎部和8 nt 的Toehold结构域能够高效实现miRNA的动态响应(图2)。
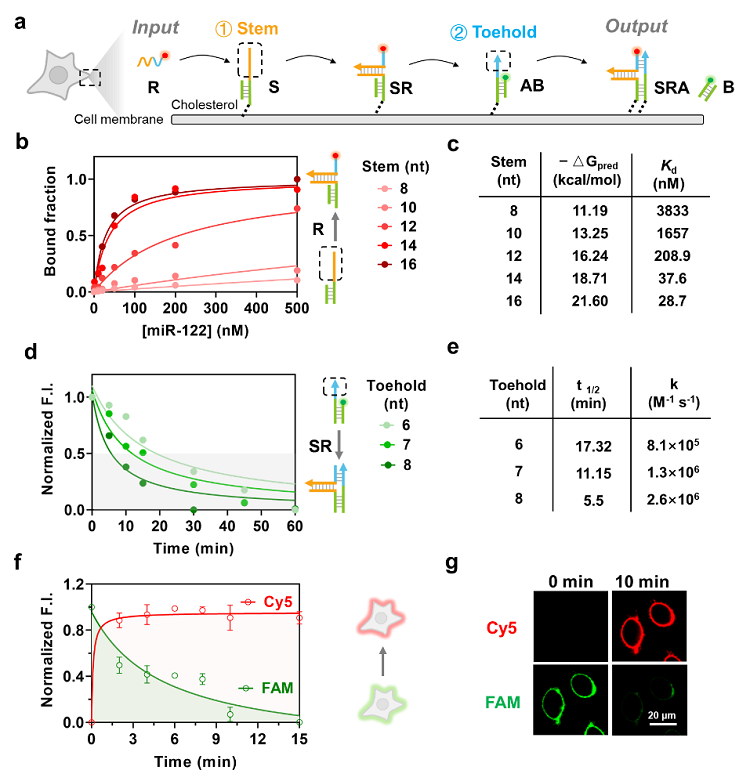
图2. miRNA响应性嵌合受体的可控调节。
之后,作者成功构建了miRNA-CDR,其能够特异性的响应靶标miR-122,并且激活肝细胞生长因子受体(MET)自磷酸化和下游信号转导通路(图3)。通过改变传感器模块中的识别结构域长度,能够以可调的灵敏度响应用户定义的miRNA。MiRNA-CDR中的靶标miRNA的识别输入模块和受体靶向的信号输出模块可以进行用户定制,作者最终在同一细胞群体中实现了两种指定miRNA驱动的受体信号激活的正交调控(图4)。
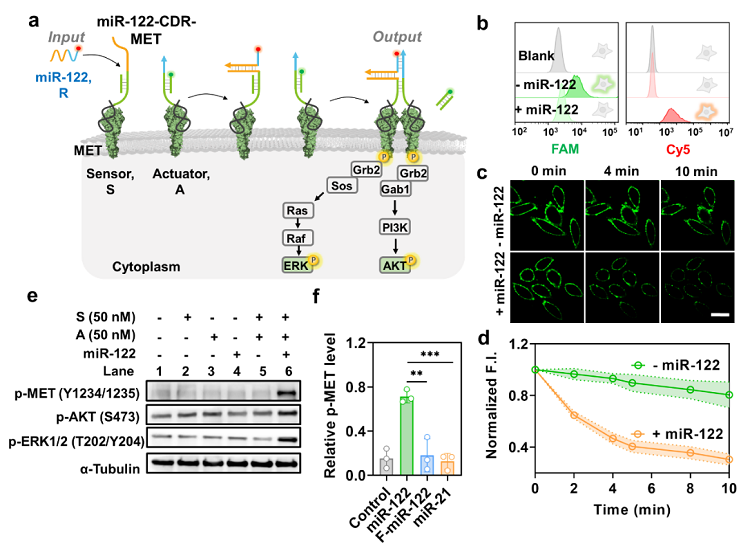
图3. 通过miRNA-CDR对细胞信号转导进行重编程。
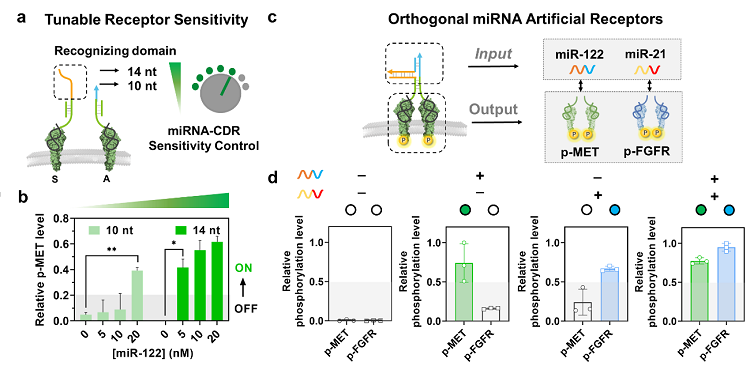
图4. 通过miRNA-CDR进行可定制和可调控的受体工程。
最后,作者将miRNA-CDR用于药物诱导的急性肝损伤的修复。作者证明了miRNA-CDR主要靶向肝脏组织,并在原位进行miR-122的特异性响应,实现了肝组织的原位再生与肝功能修复(图5)。
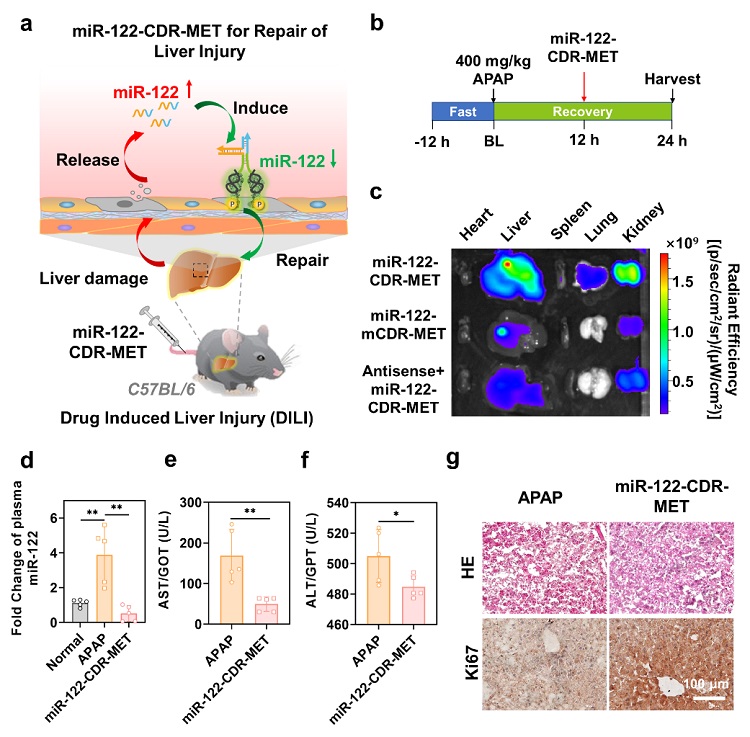
图5. MiR-122-CDR-MET促进药物诱导的急性肝损伤的修复。
总之,本研究开发的miRNA-CDR是第一个能够感知细胞外miRNA并调节原位组织再生的生物标志物驱动的治疗分子设备。该工作为治疗具有明确miRNA生物标志物的其他疾病创新治疗策略奠定了基础,也为未来开发具有可编程功能的定制分子设备提供了新的思路,此项研究进一步推动了精准医疗的发展。
相关论文发表在Angew. Chem. Int. Ed.上,湖南大学化学化工学院博士研究生贺芳为文章的第一作者,聂舟教授为通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

An Extracellular miRNA-Responsive Artificial Receptor via Dynamic DNA Nano-assembly for Biomarker-Driven Therapy
Fang He, Meixia Wang, Jieyu Wang, Prof. Hong-Hui Wang, Zhou Nie
Angew. Chem. Int. Ed., 2023, DOI: 10.1002/anie.202305227
导师介绍

聂舟,教授,博士生导师,现任湖南大学研究生院副院长兼学位办主任,生物大分子化学生物学湖南省重点实验室主任。长期从事生命分析化学基础研究,紧密围绕生物医学中关键机制研究的需求,系统性开展生物分子工具创建及其生命分析应用基础研究。近年以通讯作者在 J. Am. Chem. Soc., Angew. Chem. Int. Ed.,Science Advances, Nano Lett.等高水平期刊发表学术论文100多篇,出版个人专著2章,授权国家发明专利7项,主持国家自然科学基金杰青、重点、优青项目及国家重点研发计划课题等项目。担任中国化学会理事、青年化学工作者委员会副主任委员、英国皇家化学会《RSC Advances》副主编(2015-2022)、《分析化学》编委,入选长江学者青年学者、万人计划青年拔尖人才等高层次人才计划,获药明康德生命化学研究奖学者奖、中国化学会青年化学奖、卢嘉锡优秀导师奖、湖南省优秀科技工作者、湖南省优秀研究生导师等奖励荣誉,作为主要成员获得湖南省科学技术创新团队奖、湖南省高等教育教学成果一等奖。
https://grzy.hnu.edu.cn/site/index/niezhou
https://www.x-mol.com/university/faculty/10090
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号