北大刘涛团队与南科大蒋伟团队Chem:四嗪生物正交反应的超分子调控
生物正交化学反应是指能够在生物体系中进行且不会与天然生物化学过程相互干扰的一类化学反应,它为科学家对生命进程的原位研究带来了革命性的技术,已经成为化学生物学这一新兴交叉领域的核心方向之一,也因此于2022年获得诺贝尔化学奖。其中四嗪参与的生物正交反应——逆电子需求的Diels–Alder(IEDDA)反应,以其超快的反应速率、温和的反应条件和极好的生物相容性,被广泛应用于蛋白质的化学修饰以及生物医学的研究,对该反应的精确调控也具有着重要意义。然而,目前的调控方式大多局限于光催化或电化学的手段,对生物体具有毒性,且操作不便。因此,对四嗪的反应活性进行简便、无毒且高效地调控,是亟待解决的科学难题。
针对以上问题,2023年6月15日,北京大学药学院刘涛教授(点击查看介绍)课题组与南方科技大学蒋伟教授(点击查看介绍)课题组在Chem 杂志在线发表研究论文,报道了超分子萘管识别四嗪并调控其生物正交反应活性的策略。在这项工作中,刘涛团队基于自己之前使用超分子主体靶向蛋白表面以氨基酸侧链形式存在的客体的研究(Angew. Chem. Int. Ed. 2021, 60, 11196),以及蒋伟团队发现的能与苯基嘧啶有高亲和力的超分子萘管(CCS Chem. 2020, 2, 1078–1092),开发了四嗪生物正交反应的超分子调控策略(图1)。该策略通过萘管主体与四嗪客体的分子识别来调控四嗪的生物正交反应活性。萘管能以高亲和力识别各种生物分子上的苯基四嗪,从而以可逆的方式有效地抑制它们的生物正交反应活性。这种策略简便高效且生物相容性极好,有望扩展四嗪化学的应用。
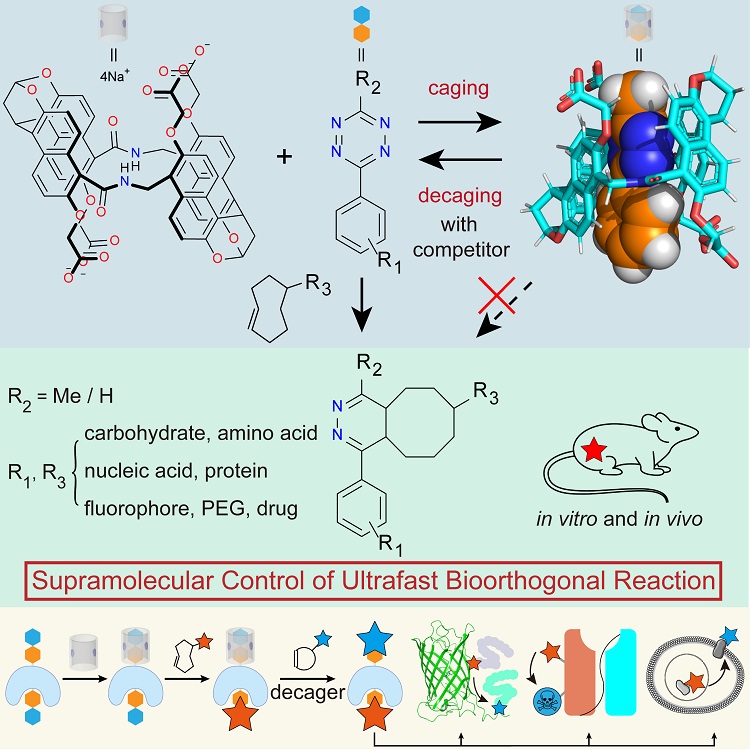
图1. 超分子萘管调控四嗪生物正交反应示意图
首先,鉴于萘管和苯基嘧啶有高亲和力,作者测试了一系列不同取代基的四嗪分子与顺式反式两种萘管的亲和力,发现苯基四嗪与反式萘管有高亲和力(~10-7 mol-1)(图2A,B)。DFT计算发现反式萘管和苯基四嗪结构有良好的相互作用,解释了该亲和力(图2C)。接下来通过停留光谱仪测定其与最常用的亲二烯体——反式环辛烯的反应速率,发现该结合能够有效抑制四嗪的反应活性(~99.9%)(图2D,E)。
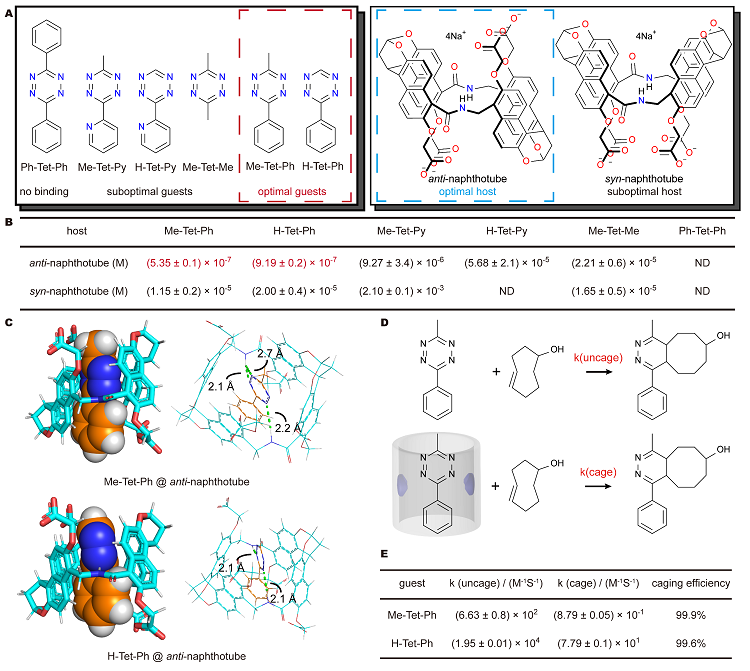
图2. 萘管和不同取代基的四嗪的分子识别及反应活性调控
然后,对于不同生物分子上修饰的四嗪,作者探索了这种结合是否还能够调控四嗪反应活性。他们尝试了糖、氨基酸、核酸的四嗪偶联物,发现其与反式萘管间仍然存在高亲和力,并且这种分子识别也能够调控这几种生物分子上四嗪的生物正交反应活性(图3A,B)。鉴于四嗪修饰的荧光分子有未反应时保持自淬灭的效果,并且已经广泛运用于细胞标记等领域,作者又尝试将IEDDA反应中的亲二烯体偶联到生物分子上,通过主客体识别调控四嗪荧光分子的IEDDA反应活性(图3C)。为了实现可逆的调控,作者开发了一系列与反式萘管有更高亲和力的竞争性小分子,希望这些小分子的加入可以恢复被包笼四嗪的反应活性(图3D,E)。实验结果也证明了该体系能迅速且彻底地对四嗪的反应活性进行抑制或恢复(图3F)。这表明该体系可以实现四嗪生物正交反应在多种生化分子(包括荧光分子、糖、氨基酸、核酸和蛋白质)上的可逆调控。
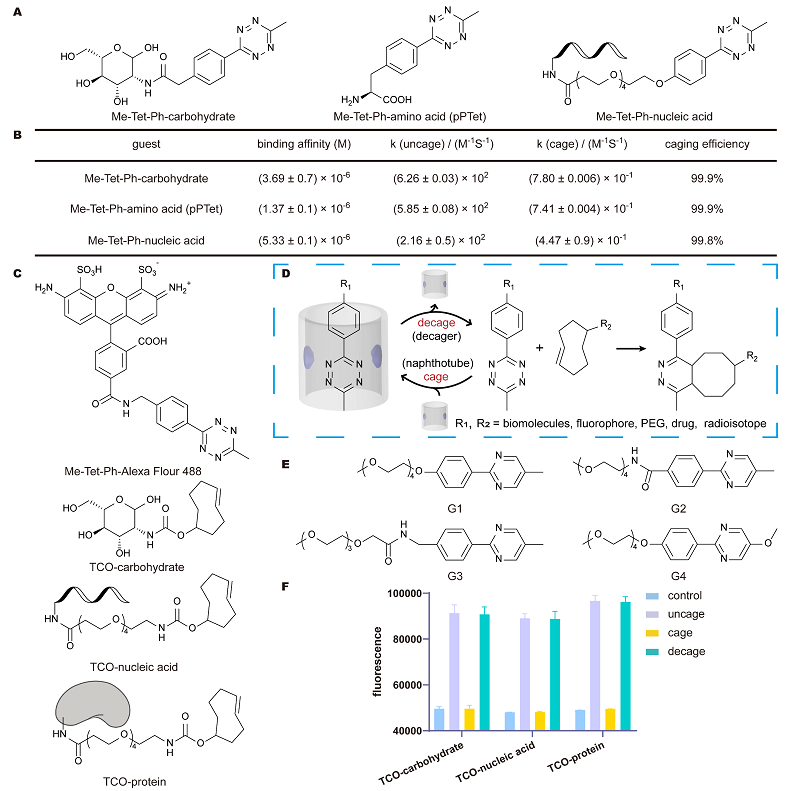
图3. 生物分子修饰的四嗪的分子识别与反应活性调控
通过将四嗪做成氨基酸侧链的形式,四嗪氨基酸可以被基因编码、参与蛋白质的翻译,实现对蛋白质的定点四嗪修饰,且四嗪氨基酸pPTet和mPTet也被证明与反式萘管有高亲和力(图4A,B)。以super folder GFP为模型,作者将不同位点突变成四嗪氨基酸,通过分子对接的理论计算发现,萘管只能识别在蛋白表面充分暴露在溶剂中的“站式”四嗪氨基酸,而不能识别贴在表面的“躺式”四嗪氨基酸,而二者本身都具有生物正交反应活性(图4C,D)。萘管与不同位点突变的蛋白的亲和力测定实验验证了这一点(图4E),且发现某些位点的四嗪氨基酸,其临近的氨基酸也可参与到与萘管的相互作用,从而提高亲和力(图4F)。

图4. 计算辅助的基因编码的四嗪氨基酸与萘管在蛋白表面的分子识别
接下来,作者验证了这种分子识别对蛋白表面基因编码的四嗪氨基酸反应活性的调控。通过测定不同位点处四嗪氨基酸在不同体系下的反应速率,发现萘管的加入可以高效地抑制“站式”四嗪的反应活性,而竞争性小分子的加入可以高效地恢复其反应活性(图5A-E);与此同时,“躺式”四嗪氨基酸不受调控元件的影响。因此,作者设想可通过先对“站式”四嗪氨基酸的包笼,让“躺式”四嗪氨基酸先进行生物正交反应,然后通过竞争性小分子的加入,让“站式”的四嗪氨基酸脱笼,并参与新的分子介导的生物正交反应,即“顺序IEDDA反应策略”(图5F)。通过在GFP上反应多种组合的亲二烯体接头,比如降冰片烯和反式环辛烯的聚乙二醇,该设想都得到了证明(图5G)。这种顺序IEDDA反应可以实现在插入多个四嗪氨基酸的蛋白质中进行快速定点的生物正交反应多修饰。
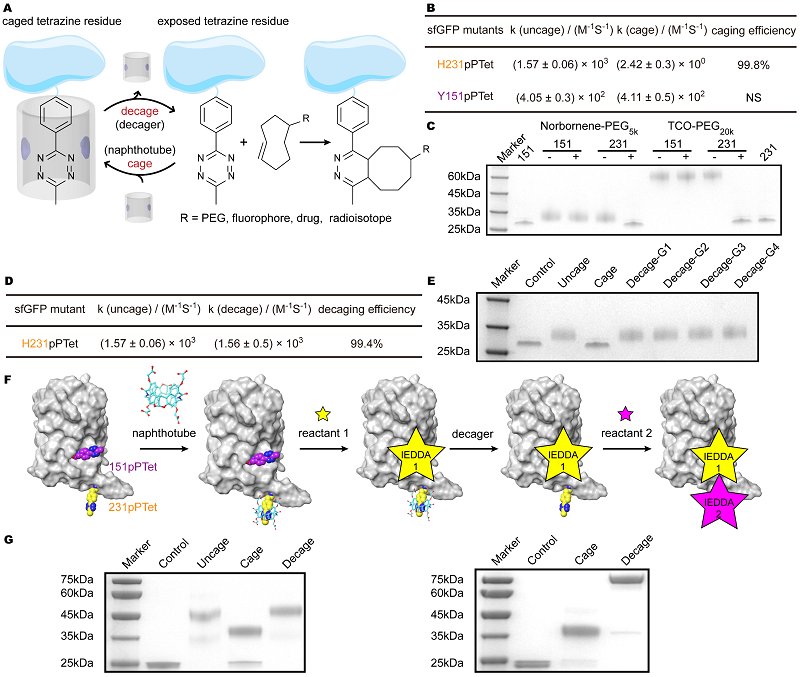
图5. 基因编码的四嗪氨基酸在蛋白质上通过顺序IEDDA反应实现快速定点多标记
鉴于抗体药物偶联物(Antibody-drug conjugates, ADC)广泛应用于临床治疗,且因抗体蛋白稳定性差,温和快速的IEDDA反应十分适用于制备抗体小分子偶联物。因此这样的顺序IEDDA反应首先应用于对于抗体的温和快速多标记。作者希望制备定点修饰的长效荧光抗体以及荧光抗体药物偶联物(图6A),于是选取trastuzumab的scFv作为模式蛋白,首先通过分子对接的理论计算找到了其蛋白表面两种性质的四嗪氨基酸突变位点——一种能使氨基酸与萘管结合,一种不能(图6B)。实验都证明了这两种位点的性质(图6C)。通过表达这两个位点都插入了四嗪氨基酸的抗体并进行顺序IEDDA反应,作者制备了定点修饰的长效荧光抗体(两个位点分别修饰聚乙二醇与荧光分子TAMRA)以及荧光抗体药物偶联物(分别修饰荧光分子TAMRA和毒素MMAE)并表征了其活性(图6D,E)。这表明顺序IEDDA反应的策略可实现抗体精准多位点修饰及抗体药物荧光双偶联。
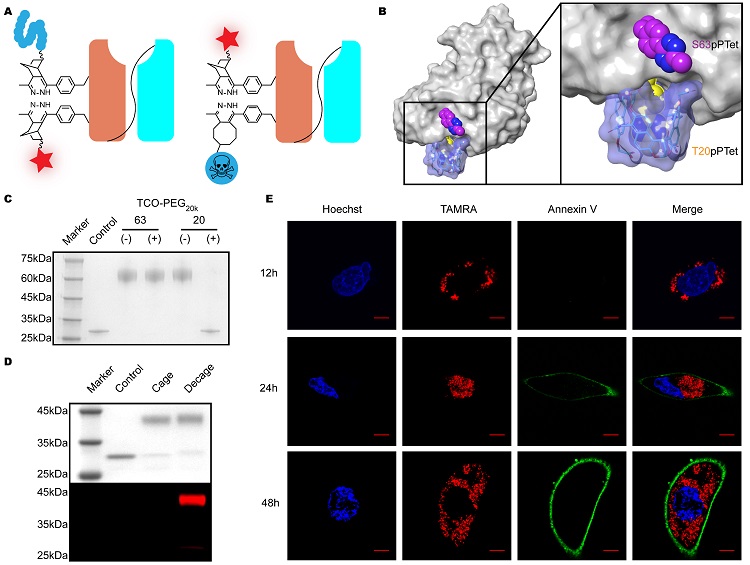
图6. 顺序IEDDA反应的策略实现抗体精准多位点修饰及抗体药物荧光双偶联
四嗪与反式环辛烯的IEDDA反应由于其温和快速的特点,被广泛应用于活细胞的标记。而超分子调控元件萘管等也具有极好的生物相容性。因此作者设想通过细胞自身表达多种含四嗪氨基酸的蛋白,顺序IEDDA反应可以实现对于同一活细胞内多种蛋白迅速且温和的定点修饰、标记与成像(图7A)。首先作者验证了该体系可对细胞膜蛋白表面四嗪的反应进行调控(图7B)。接着作者选取了两种蛋白,一种是锚定在膜表面的mCherry,在上面选取了能与萘管结合的四嗪氨基酸突变位点,一种是组蛋白,选取了不能与萘管结合的四嗪氨基酸突变位点,并通过与反式环辛烯的荧光染料反应验证了性质(图7C,D)。然后作者先通过mCherry四嗪的包笼,让组蛋白上的四嗪参与反应,然后进行mCherry四嗪的脱笼并参与另一种荧光分子的反应,进行了共聚焦成像,两种荧光分子分别定点标记了两种蛋白质(图7E)。这证明了顺序IEDDA反应可以实现活细胞多靶点定点高效成像。
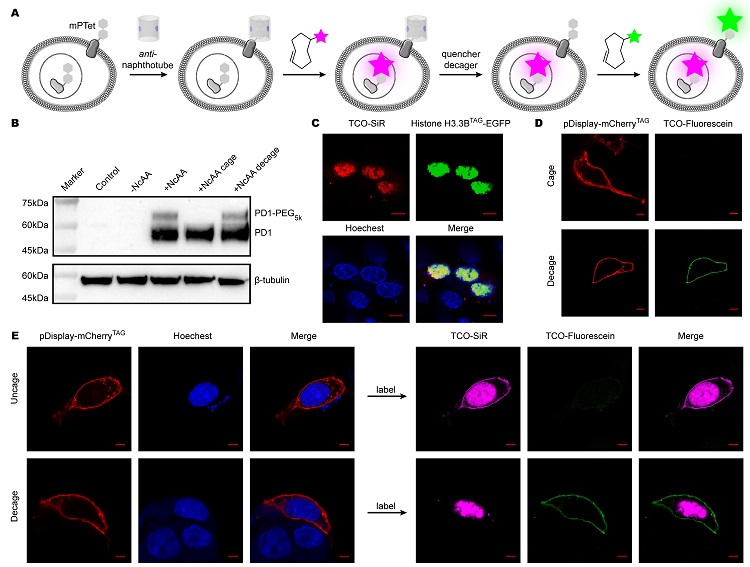
图7. 顺序IEDDA反应实现活细胞多靶点高效成像
四嗪IEDDA反应速率很高,这使得它可以用于活体内的反应。萘管也具有极好的生物相容性并曾用于小鼠活体实验(CCS Chem. 2022, 4, 1977–1989)。因此,本文也进行了在活体内实现四嗪生物正交反应活性调控的实验。通过向小鼠注射表面修饰四嗪的细胞和萘管,尾静脉注射反式环辛烯荧光染料和竞争性小分子,细胞上四嗪的生物正交反应得到了良好的调控(图8)。这证明该体系可用于小鼠活体内实现四嗪生物正交反应活性的可逆调控。

图8. 小鼠活体内实现四嗪生物正交反应活性的可逆调控
总结
该工作开发了一种基于超分子主客体识别的四嗪生物正交反应活性调控策略,该策略通过萘管主体与四嗪客体的分子识别来调控四嗪的生物正交反应活性。萘管能以高亲和力识别各种生物分子上的苯基四嗪,从而以可逆的方式有效地抑制它们的生物正交反应活性。这种调控方式对于一系列包含四嗪的生化分子以及复杂环境下仍然适用。并且通过顺序IEDDA反应的策略,该调控体系可用于制备定点修饰的长效荧光抗体以及荧光抗体药物偶联物、对同一活细胞内多种蛋白迅速且温和的定点修饰与标记。这种策略生物相容性好,操作便捷,有望扩展四嗪化学的应用。
北京大学药学院刘涛教授为本文的通讯作者。南开大学联合培养2015级博士生(已毕业)曹文兵、北京大学药学院2018级六年制学生王浩宇、深圳大学材料学院副研究员权茂为本文共同第一作者。团队成员李雨轩、苏晔宇、李雨航,南方科技大学蒋伟教授,天然药物及仿生药物国家重点实验室平台指导老师张晓辉和师晓萌以及北京大学医学部实验动物科学部指导老师赵祎洁也对该工作做出了重要贡献。该工作得到了国家自然科学基金(92156025, 92253301和U22A20332)、国家重点研发计划(2022YFA0912400和2021YFA0909900)和北京市自然科学基金(JQ20034)的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Reversible control of tetrazine bioorthogonal reactivity by naphthotube-mediated host-guest recognition
Wenbing Cao, Haoyu Wang, Mao Quan, Yuxuan Li, Yeyu Su, Yuhang Li, Wei Jiang, Tao Liu*
Chem, 2023, DOI: 10.1016/j.chempr.2023.05.034
刘涛教授简介

刘涛,博士,北京大学药学院长聘研究员,博士生导师,分子与细胞药理系主任,天然药物及仿生药物国家重点实验室PI,化学生物学交叉中心PI,北大医学-惠大基因密码子创新联合实验室负责人。国家高层次青年人才、国家优秀青年科学基金获得者、北京市杰出青年基金获得者。任中国医药生物技术协会委员合成生物学分会委员,中国生物医学工程学会青工委委员,获中国药学会以岭生物医药青年奖,拜耳研究员奖,首届屠呦呦青年学者奖,北大王选青年学者奖等。以通讯作者身份在Nat Chem Biol、Mol Cell、Nat. Commun、Sci Adv、Chem、JACS、Angew Chem等国际高水平期刊发表一系列研究论文。担任Journal of Molecular Biology编委,Chinese Chemical Letter编委等。研究集中在蛋白质药物化学修饰,基因编辑与细胞治疗,发展了含有人造氨基酸的蛋白质创新药物,应用在肿瘤及细胞治疗等多种领域,从而促进了生物药物的升级换代。
https://www.x-mol.com/university/faculty/49942
蒋伟教授简介

蒋伟,博士,原南方科技大学化学系、深圳格拉布斯研究院双聘教授,博士生导师。国家杰出青年基金获得者、国家优秀青年基金获得者、国家高层次青年人才、英国皇家化学会会士、深圳市“鹏城学者”特聘教授。获中国化学会“超分子化学青年创新学术讲座奖”,大环芳烃超分子化学“学术新星奖”,德国先令基金会“先令奖”等。以通讯作者身份在Nat. Chem.、Nat. Commun.、JACS、Angew. Chem. Int. Ed.、CCS Chem.等国际高水平期刊发表一系列研究论文。担任Chinese Chemical Letter青年编委、中国化学会高级会员等。研究集中在仿生分子识别,新型大环主体开发,并将其应用于环境污染物检测与治理、ee值光谱测量、神经毒气的解毒、药物增溶、分子机器、智能材料等多种领域。
https://www.x-mol.com/university/faculty/26767
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号