Chem Catal.:羟基氧化镍OER反应机理和侧边超氧镍物种的原位观测
电化学析氧反应(OER)是电解水、二氧化碳电还原、氮气电还原等能源相关电化学反应中至关重要的氧化半反应。酸性介质下,仅有Ir氧化物及其衍生物可实现稳定的OER催化性能,而碱性条件下诸多丰产金属的羟基氧化物展现出相当甚至优于Ir氧化物的OER性能。这类催化剂中,NiOOH引发了广泛关注,被认为是OER反应的高性能催化剂,因此对NiOOH催化OER反应的活性物种以及催化机理的研究十分关键。尽管当前有大量研究关注NiOOH的OER反应催化机理,对该过程的理解仍未建立实验上的认知。绝大多数工作关注点集中在静息态Ni的氧化态(存在相互矛盾的结论)、晶格氧的参与以及可能的“活性氧”中间体。
基于此,来自瑞士洛桑联邦理工大学的胡喜乐教授研究团队结合包括X射线吸收光谱(XAS)、紫外-可见光谱(UV-Vis)以及拉曼光谱在内的多种原位表征手段并结合电动力学,以Ni(OH)2纳米片为研究对象,研究了其催化OER反应的中间体与机理。光谱学数据揭示了两种中间体,一是由Ni(OH)2经二电子氧化生成的Ni(III)-O•物种;二是Ni(III)-O•经单电子氧化形成的Ni-OO-Ni侧边超氧镍中间体,可作为空穴积累的位点。反应动力学遵循内球反应模型(inner-sphere model),反应的决速步骤为OH-进攻Ni(III)-O•。基于光谱学和电动力学分析,作者提出了详细的反应循环,并为其中的关键步骤提供了实验上的支撑。相关工作发表于Cell Press细胞出版社期刊Chem Catalysis 上。

电化学行为与原位X射线吸收光谱分析
首先,作者选取超薄水镁石型Ni(OH)2纳米片作为研究对象,其厚度约为1.5至2纳米,具有明确的组成和结构,二维片状结构则有利于电子的快速转移。样品的离线拉曼光谱显示出位于450以及500 cm-1处的吸收带,源于NiII-OH和NiII-O的振动。TEM图像所得样品厚度与Ni(OH)2层状分子结构的对比得到该纳米片约由2-3层构成。在0.1 M KOH以及20 mV s-1的扫描速度下,Ni(OH)2的循环伏安曲线中位于1.42 V(相对于可逆氢电极)出现明显氧化峰,位于1.58 V的OER反应起始电位之前;在逆扫描过程中,还原峰出现在1.27 V。氧化峰和还原峰通常对应于Ni(OH)2和NiOOH的相互转变。
随后,作者利用原位X射线吸收光谱技术观测了电位依赖的Ni氧化态变化以及催化剂结构演变(图1)。X射线近边吸收谱显示干燥状态下Ni(OH)2的氧化约为2.6,当材料置于碱性条件下,其近边谱的shake-down效应增强,这是由于Ni中心与溶液中的OH-相互作用导致了结构扭曲所造成的(图1A和B)。随着所施加电位的逐渐升高,近边谱一阶导的峰位不断向高能移动,且显示出4p能量的裂分,表明Ni的氧化过程与施加电位的提高相关,且结构的对称性减弱。电位依赖的Ni氧化态变化可通过1s-4p吸收能量的变化推断(图1C),结果表明,从开路到1.40 V的电位,Ni的1s-4p吸收能量上升程度较小;而从1.40 V至1.50 V,Ni的1s-4p吸收能量出现显著上升,在1.50 V的电位下,Ni的氧化态约为3.6。这一氧化行为对应于循环伏安曲线中Ni(OH)2至NiOOH的转变。X射线吸收光谱数据表明Ni氧化物中Ni的1电子氧化可导致1s-4p吸收能量2.1 eV的上升。扩展X射线吸收精细结构谱揭示了催化剂的结构演变(图1D),干燥样品中Ni-O键长约为2.07 Å,归属于Ni(II)-O;从开路到1.30 V,其键长为2.07-2.08 Å,Ni-Ni键长为3.10-3.11 Å,表明该过程中Ni离子的氧化态保持不变。在1.40 V和1.50 V条件下,Ni-O和Ni-Ni键长显著下降,降至1.88-1.85 Å以及2.81-2.82 Å,证实了Ni氧化态的提升以及NiOOH的形成。
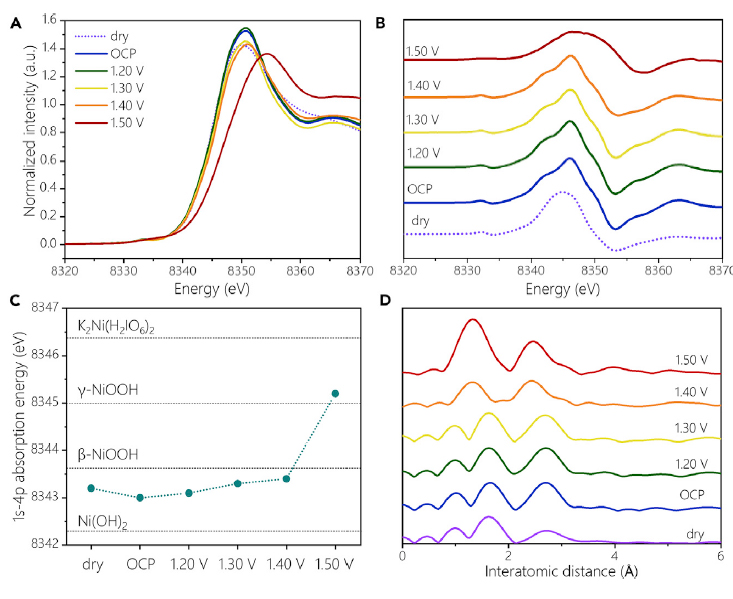
图1. 原位X射线吸收光谱分析
进一步,作者利用原位UV-Vis光谱追踪了不同电位下Ni的吸收特征(图2)。开路至1.375 V的过程中光谱仅显示若吸收,1.375 V至1.425 V电位下吸收明显增强,进一步提升电位吸收增强减缓。通过对不同电位下的吸收光谱进行归一化处理,位于550 nm的吸收特征峰随着电位的升高逐渐增强,表明氧化物种具有电位依赖的累积现象。

图2. 原位紫外-可见光谱分析
随后作者又采用原位表面增强拉曼光谱技术观测对应于NiII-O以及NiII-OH带的变化(图3A)。开路下,NiII-O以及NiII-OH的振动模式分别位于450 cm-1和500 cm-1,随着电位逐渐提升至1.35 V,光谱中位于560 cm-1处出现一特征吸收,同时在800至1200 cm-1之间出现一组宽峰(图3B)。前者表明NiOOH的生成,后者此前被认为是“活性氧(O-O)物种”。在1.4 V及以上电位时,位于480和560 cm-1处的特征吸收开始占据主导,且800-1200 cm-1的宽峰具有较高强度。当使用氧18标记的KOH作为电解液时,对应于NiII-O以及NiII-OH的吸收峰红移25 cm-1,表明晶格中的氧16可与电解质发生交换。而在NiOOH形成后,对应于NiIII-O的吸收带同样红移25 cm-1,800至1200 cm-1之间的宽峰红移50 cm-1,表明其对应的物种含有两个氧原子。而使用KOD的D2O溶液作为电解液,NiIII-O以及O-O吸收带并未移动,表明反应中NiIII-O和O-O并不会质子化或与邻近羟基形成氢键。
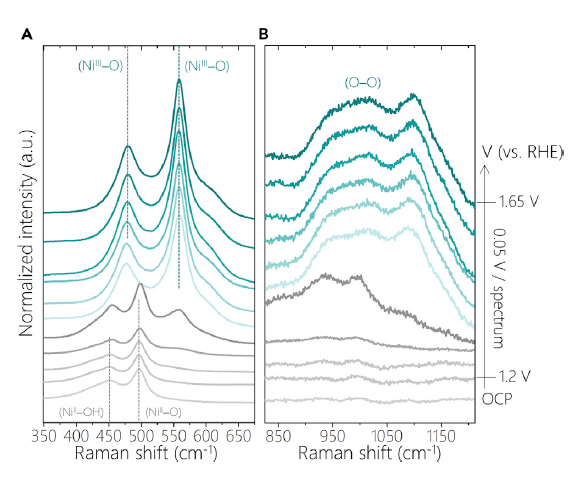
图3. 原位拉曼光谱分析
对于归因于活性氧物种的800至1200 cm-1之间的宽峰,作者进行了深入分析。该特征宽峰的起源还存在争议,部分人认为其归属于表面带负电的NiOO-物种,也有人认为其应对应于氧原子或过氧物种,并且还存在超氧物种的可能性。因此作者采用不同电位下LiNiO2以及NiO2的吸收情况作为对比(图4)。NiO2和LiNiO2的对比数据表明在800至1200 cm-1之间的宽峰中存在的特征吸收归属于Ni氧化物的晶格结构,而并非OER反应的活性氧中间体。通过对该范围宽峰的分峰拟合可进一步区分其中具有的复杂吸收(图5)。直到1.45V时其分峰特征与对比NiO2的吸收频率基本一致。当电位达到1.5V及以上时,原有的峰(i)变为峰(i’)以及(i’’)。位于950 cm-1的峰(ii’)随着电位的升高而增强,而峰(i’)保持不变,表明峰(i’’)可能源于OER中间体。对于同位素标记的电解液氧18-KOH或KOD-D2O(图6),KOD-D2O中未出现明显的峰位移动;氧18-KOH中活性氧吸收带可被分峰拟合为6个峰,包括5个相对于KOD-D2O移动45 cm-1的峰。该现象表明950 cm-1的吸收峰对应于O-O且未被质子化。
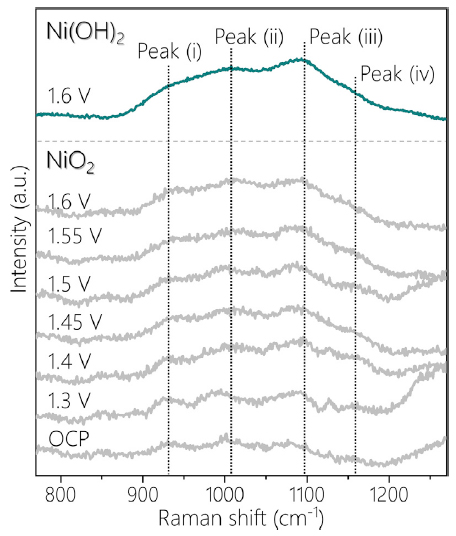
图4. 高波数区域NiO2的原位拉曼光谱
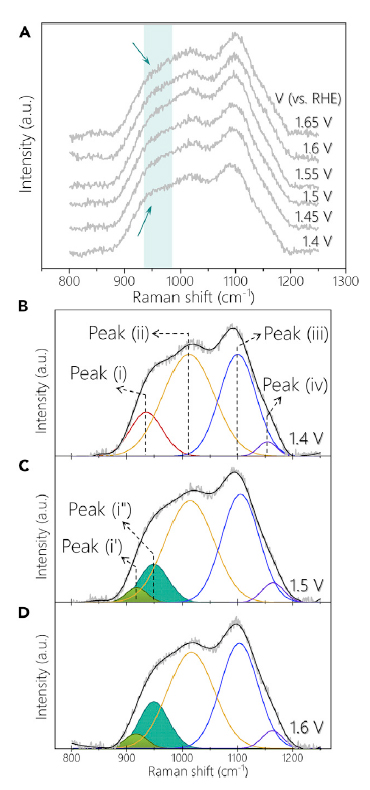
图5. Ni(OH)2纳米片的原位拉曼光谱分峰拟合

图6. 同位素标记对比实验下Ni(OH)2纳米片的原位拉曼光谱分峰拟合
样品的Tafel曲线测试显示出两个具有显著差别的区域(图7):1.54至1.62 V Tafel斜率为67.6mV dec-1,当电位高于1.62 V时,Tafel斜率升高至137.8 mV dec-1。考虑到存在两个显著区分的Tafel区域,分别选择需要在1 mA cm-2 (约1.58 V)以及1 mA cm-2(约1.65 V)下的电位以明确反应对OH-浓度的依赖。结果表明低电位区域反应相对于OH-浓度为一级反应,而高电位区域约为0.5级反应,同位素实验测得的KIE数值表明决速步骤涉及到了O-H键的断裂。
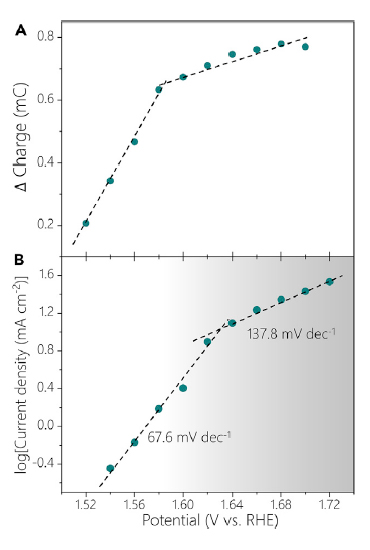
图7. 电动力学分析
结合电位依赖的位于950 cm-1的拉曼吸收峰积分面积的变化以及OER动力学,表明其对应的物种为催化反应的中间体。该吸收峰位置对应于超氧基元,最有可能具有侧边的结构而不是端基结构。H/D同位素交换实验表明超氧基元反应中并未质子化,且位于周围基团形成氢键。
OER反应机理
基于电化学、原位光谱学以及电动力学分析,作者提出了Ni(OH)2碱性OER的反应机理(图8)。首先,Ni(II)(OH)2的氧化产生了Ni(III)-O•-Ni(III)-O-二聚体(电动力学实验与X射线吸收光谱实验验证),随着电位的提升,二聚体的氧化生成了一种可能是侧边超氧物种,Ni(III)-OO-Ni(III)中间体(UV-Vis和拉曼光谱实验验证)。进一步的,溶液中的OH-进攻Ni(III)-O•,O-H键断裂,H转移到(ii’),同时(ii’)还原至(ii),该步骤为反应的决速步骤,(ii’)和(ii)的可逆互变涉及到质子和电子转移,与KIE数据相符。随后,作者提出Ni-OO-的氧化、氧气的析出以及Ni(III)-O•-Ni(III)-O-二聚体,完成催化循环。
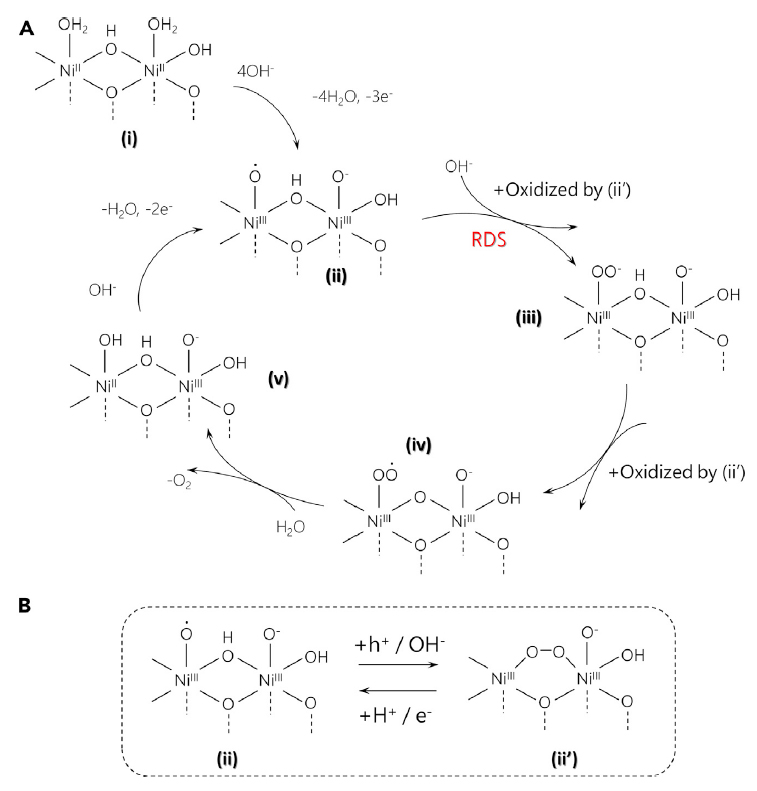
图8. OER反应的可能机理
总之,该工作强调了理解不同中间体在反应中的角色对电催化机理研究的重要作用。Ni(OH)2/NiOOH的反应机理将为后续Ni基多组分OER催化的分析提供新的参考。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Operando identification of a side-on nickel superoxide intermediate and the mechanism of oxygen evolution on nickel oxyhydroxide
Seunghwa Lee, You-Chiuan Chu, Lichen Bai, Hao Ming Chen, Xile Hu
Chem Catal., 2022, DOI: 10.1016/j.checat.2022.11.014
(本稿件来自CellPress)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号