Pd/C催化剂界面开路电位对苯甲醇水相氢解反应的影响
水是催化反应的常用溶剂,并且是多种催化反应的产物。相较于其他质子溶剂及非质子溶剂,水参与的反应体系更为复杂。近日,慕尼黑工业大学Johannes A. Lercher教授和华东师范大学的刘玥研究员团队研究了Pd/C催化剂在水中的开路电位(Open Circuit Potential, OCP)对苯甲醇氢解生成甲苯的影响。
水介质中,水解离生成的水合氢离子可以引发新反应路径 (如质子-电子耦合转移路径,PCET);同时,水在金属表面极化从而在固-液界面形成电势梯度,影响固-液界面的双电层结构、带电粒子的化学势以及粒子重排等。因此除直接参与基元反应的吸附物种,分布在外亥姆霍兹层的离子/分子,尤其是水合氢离子,对反应也能起到至关重要的作用。C-O键断裂的反应活性对反应体系 (包括溶剂和催化剂载体) 的酸性非常敏感。然而,该类反应中水合氢离子和金属在基元步骤中的作用,尤其是液固界面处微环境的影响尚不清楚,因此无法形成普遍接受的反应机制。
水相体系中Pd/C催化苯甲醇氢解的反应中当pH从7降到0.6,反应速率增加了2-3个数量级。通过系列动力学分析和动力学同位素效应,发现该反应遵循苯甲醇羟基质子化脱水生成苄基阳离子,然后氢化物加成生成甲苯的反应路径,其中质子化苯甲醇脱水是反应的速控步骤。作为质子供体,水合氢离子的活度可以影响速控步骤的初始态 (质子化苯甲醇) 的浓度,从而影响反应速率。此外,与氢气的准平衡电极反应建立的开路电位可以稳定基元步骤中的所有阳离子,包括速控步骤的初始态和过渡态。由于外亥姆霍兹层的氢键作用,过渡态更靠近催化剂表面,因此被稳定程度更高,从而降低了速控步骤的反应能垒 (图1)。H2对反应活性的影响主要基于与水合氢离子形成氧化还原对,影响电极电势。除了开路电压外,在电催化体系中的施加负电位也被证明可以以相同的方式提高该反应的速率。该工作揭示了溶液酸性对苯甲醇氢解反应活性影响的物理化学内因,有利于提高对液-固界面化学微环境的认识。
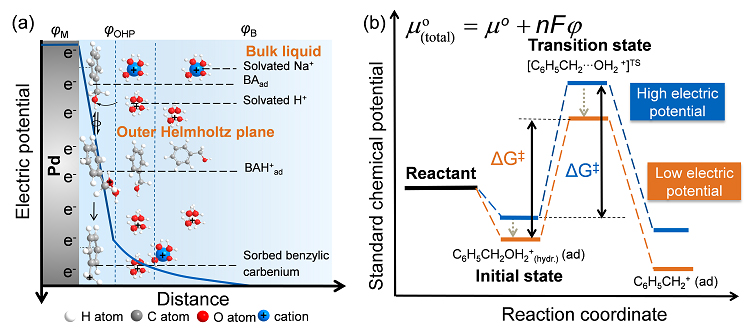
图1. 决速步骤 (左图) 和能量图 (右图) 的示意图。
这一成果近期发表在Nature Communications 上,文章的第一作者程冠桦博士现在山东大学材料科学与工程学院工作,慕尼黑工业大学Johannes A. Lercher教授和华东师范大学的刘玥研究员为共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Importance of interface open circuit potential on aqueous hydrogenolytic reduction of benzyl alcohol over Pd/C
Guanhua Cheng, Wei Zhang, Andreas Jentys, Erika E. Ember, Oliver Y. Gutiérrez, Yue Liu & Johannes A. Lercher
Nat. Commun., 2022, 13, 7967, DOI: 10.1038/s41467-022-35554-1
导师介绍
Johannes A. Lercher
https://www.x-mol.com/university/faculty/2388
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号