南方科技大学刘心元团队Nature Chemistry:铜催化的不对称自由基杂原子硫–氧偶联反应
过渡金属催化的有机卤化物与亲核试剂之间的交叉偶联反应已经发展成为应用最为广泛的构建碳–碳和碳–杂(p区元素)键的方法之一,在现代有机合成中占有重要的地位(图1a)。然而,通过过渡金属催化的杂原子和杂原子相互交叉偶联反应构建杂–杂(p区元素)键的报道则相对较少,而不对称反应更是罕见。实现该类反应最大的挑战在于杂–杂键成键时最后还原消除的步骤十分困难(图1b)。另一方面,杂–杂(p区元素)键化合物是有机化学中一类非常重要的化合物,更是天然产物、活性药物分子等不可或缺的合成砌块,也是构建新配体、新材料的重要组成成分。因此实现过渡金属催化的杂–杂偶联反应,尤其是实现不对称杂–杂偶联反应具有重要的学术意义。
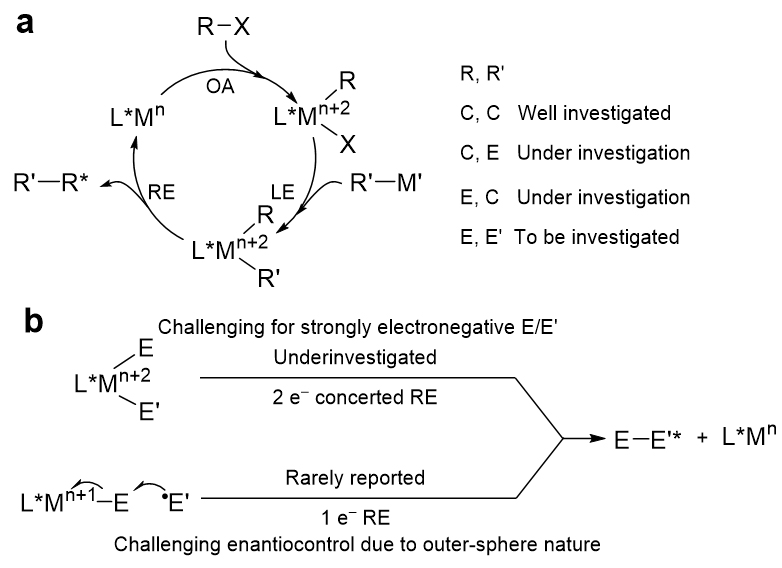
图1. 过渡金属催化的杂原子–杂原子交叉偶联反应的发展和挑战
南方科技大学刘心元团队一直围绕过渡金属催化的不对称自由基化学开展系统性研究工作(Acc. Chem. Res. 2020, 53, 170; Nat. Chem. 2019, 11, 1158; Nat. Catal. 2020, 3, 401; Nat. Catal. 2020, 3, 539; Nat. Chem. 2022, 14, 949等)。在这些工作的基础上,刘心元团队设想通过单电子还原消除的方式解决杂–杂键难以发生双电子还原消除的问题,同时通过手性配体调控来实现不对称杂–杂偶联反应。基于此设想,刘心元团队使用磺酰氯作为杂原子亲电试剂,在一价铜的还原下产生磺酰基自由基中间体和二价铜,前手性或内消旋二醇作为杂原子亲核试剂首先与产生的二价铜进行配体交换,最后磺酰基自由基与二价铜中间体进行单电子还原消除,从而实现了铜催化的不对称自由基杂原子硫–氧偶联反应(图2a)。该反应的底物适用范围十分宽泛,内消旋1,2-二醇、前手性1,3-二醇、前手性2-氨基-1,3-二醇、前手性1,2,3-三醇,以及部分羟基被保护的内消旋四醇、五醇、六醇等都可以很好的进行不对称自由基杂原子硫–氧偶联反应(图2b)。更重要的是,利用此策略便可以实现大宗化工原料甘油的不对称转化,实现高附加值手性C3合成子的构建(图2c)。除此之外,利用该反应作为关键步骤,可以实现肌醇的高对映选择性4,6-位去对称化,为手性肌醇-4(or 6)-磷酸酯的合成提供了新的策略(图2d)。该反应的实现为挑战性的非环全碳季碳手性中心以及资源分子高效不对称转化提供了多样化便捷的合成平台,为不对称自由基杂–杂偶联反应提供了新策略和新思路。相关研究成果以“铜催化的不对称自由基杂原子硫–氧偶联反应(Cu-catalysed enantioselective radical heteroatomic S–O cross-coupling)”为题,在《自然•化学》(Nature Chemistry)上发表。
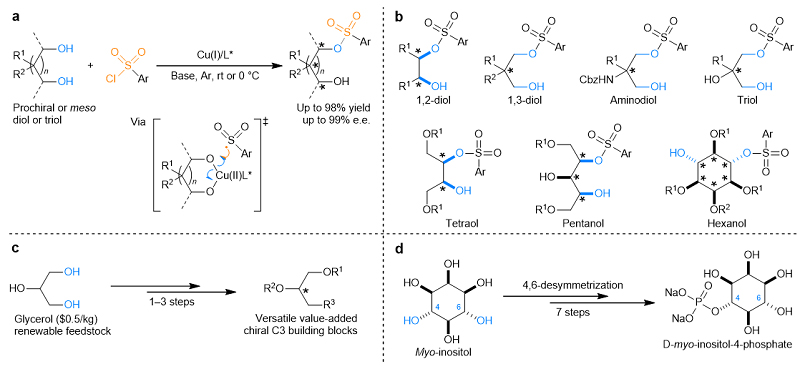
图2. 铜催化的不对称自由基杂原子硫–氧偶联反应
机理研究发现,当向反应体系中加入自由基捕获试剂(TEMPO、1,4-苯醌、BHT)时,主反应被明显抑制,同时可以观察到BHT捕捉磺酰基自由基的产物(图3a)。此外在未加入二醇的标准条件下进行自由基钟实验,发现可以得到环丙烷开环的产物(图3b)。基于以上实验,作者推测反应中有磺酰基自由基的产生,同时磺酰基自由基的产生不需要二醇的参与。
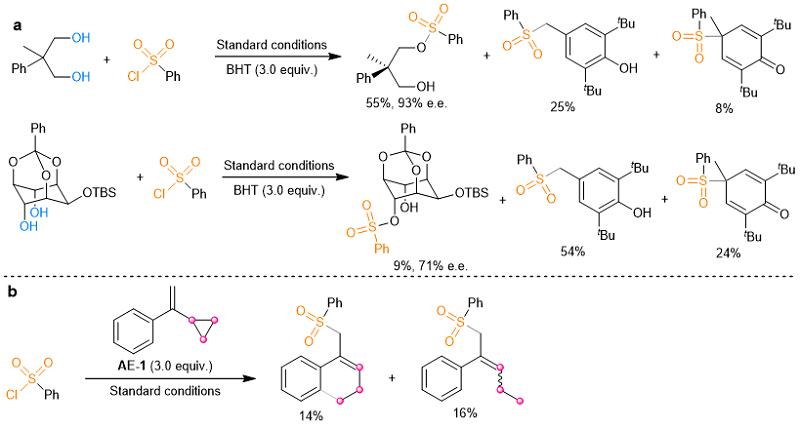
图3. 自由基捕获实验和自由基钟实验
为进一步证实硫–氧偶联产物是通过磺酰基自由基中间体生成的,作者使用其他已知策略来产生磺酰基自由基,并验证是否能得到目标硫–氧偶联产物。作者发现使用烯基砜作为磺酰基自由基前体,通过自由基加成,β-裂解产生磺酰基自由基,可以得到目标硫–氧偶联产物,并具有不错的对映选择性(图4a);使用硫代磺酸酯作为磺酰基自由基前体,通过自由基取代产生磺酰基自由基,也可以得到具有较好对映选择性的目标硫–氧偶联产物(图4b);使用磺酰肼作为磺酰基自由基前体,通过自由基攫氢、脱氮气产生磺酰基自由基,同样可以得到88% e.e.值的目标硫–氧偶联产物(图4c)。此外,当使用苄基磺酰氯在标准条件下进行反应时得到的产物几乎是消旋的,同时有少量双磺酰基化的副产物和苄基自由基自身偶联的副产物生成,作者推测由于苄基磺酰基自由基容易脱二氧化硫生成苄基自由基,消旋产物通过离子型背景反应得到。
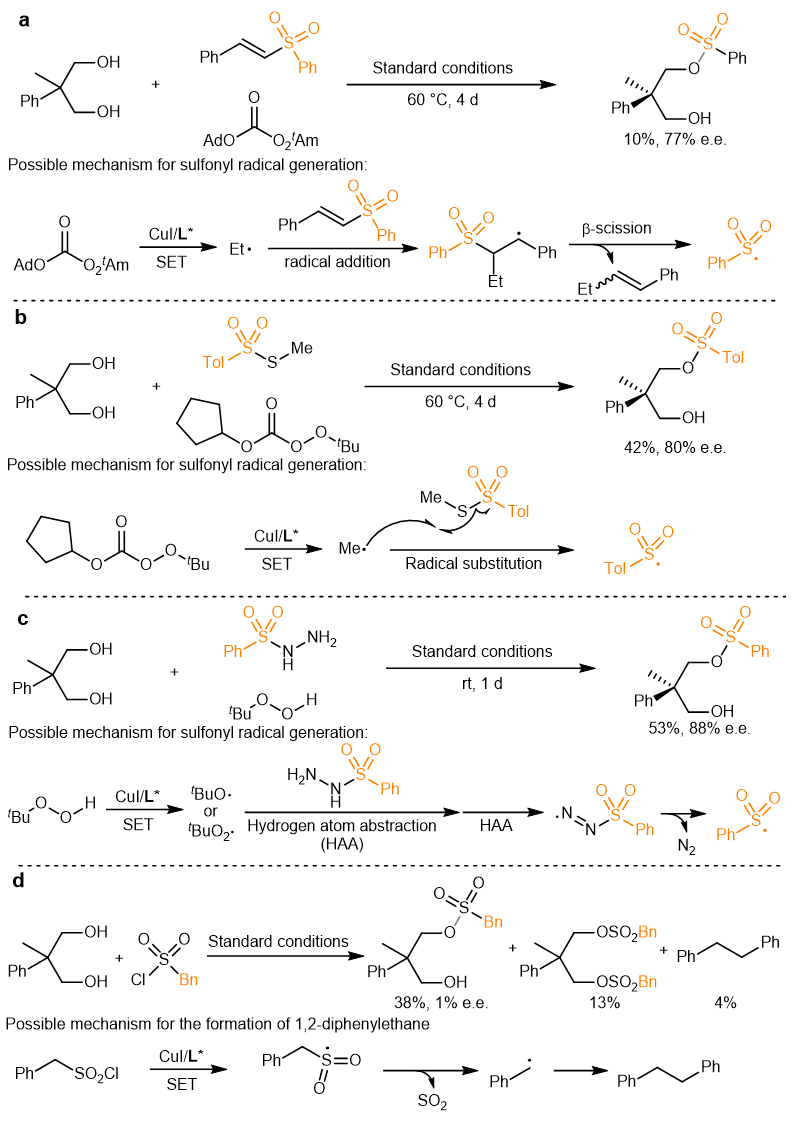
图4. 通过磺酰基自由基中间体生成硫–氧偶联产物
为了进一步揭示反应机理,作者与浙江大学洪鑫团队合作,通过DFT计算对反应的机理进行了深入的研究。理论计算表明,关键的硫–氧成键过程经历开壳层单重态的、外球自由基取代型机理(图5a)。在过渡态TS84-Minor中由于金鸡纳碱配体的奎宁环部分与磺酰基自由基具有一定的位阻作用,因此其能量比TS84-Major高2.7 kcal mol−1(图5b),这与实验测得的结果是一致的(94% e.e.)。
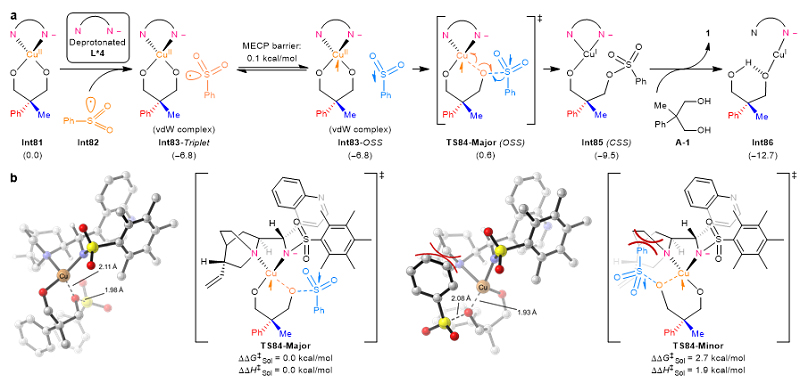
图5. 理论计算
总结
南方科技大学刘心元、顾强帅团队与浙江大学洪鑫团队合作,使用磺酰氯作为杂原子亲电试剂,前手性或内消旋二醇作为杂原子亲核试剂,实现了首例铜催化的不对称自由基杂原子硫–氧偶联反应。该反应的底物适用范围十分宽泛。同时还可以实现大宗工业原料甘油的不对称自由基杂原子硫–氧偶联反应,完成从工业原料到高附加值手性产物的转化。此外还可以实现肌醇的4,6-去对称化,为手性肌醇-4(or 6)-磷酸酯的合成提供了新的策略。实验和理论计算研究表明关键的硫–氧成键过程经历开壳层单重态的、外球自由基取代型机理。研究成果为不对称自由基交叉杂–杂偶联反应提供了可行策略和新思路。
该课题组所有研究项目都得到了国家自然科学基金委员会、科技部、深圳市科创委、深圳市诺贝尔奖科学家实验室等项目的大力资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cu-catalysed enantioselective radical heteroatomic S–O cross-coupling
Yong-Feng Cheng, Zhang-Long Yu, Yu Tian, Ji-Ren Liu, Han-Tao Wen, Na-Chuan Jiang, Jun-Qian Bian, Guo-Xiong Xu, Dan-Tong Xu, Zhong-Liang Li, Qiang-Shuai Gu,* Xin Hong,* Xin-Yuan Liu*
Nat. Chem., 2022, DOI: 10.1038/s41557-022-01102-z
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!










































 京公网安备 11010802027423号
京公网安备 11010802027423号