林君/程子泳/马平安团队Adv. Mater.:声催化介导的氢气治疗
声动力治疗 (SDT) 是利用低强度超声 (US) 作为激发源触发声化学反应产生高细胞毒性的活性氧 (ROS),因US对人体的高组织穿透性和安全性而受到越来越多的关注。尽管有这些无可比拟的优势,SDT仍处于基础研究阶段,尚未实现广泛的临床应用。这是因为声敏剂的缺乏和肿瘤微环境 (TME) 的特异性阻碍了ROS的持续产生。因此,在过去的十几年里,人们开发出了各种性能优异的声敏剂来克服这一难题。值得注意的是,阻碍ROS生成的因素是多种多样的,如声激发电子/空穴对的快速重组、肿瘤固有缺氧以及过表达的谷胱甘肽(GSH)。然而,基于ROS的新型纳米平台的设计很难考虑所有的限制因素。因此,开发既能产生不依赖氧的治疗分子,又不受TME限制的声敏剂对于推动SDT的持续发展极具价值。
鉴于此,中国科学院长春应用化学研究所林君(点击查看介绍)/马平安(点击查看介绍)研究团队与广东医科大学程子泳(点击查看介绍)研究团队合作,首次提出声催化产氢的概念并将其定义为:US提供外部能量输入以激活声催化剂通过裂解水在肿瘤部位原位产氢。这一概念将SDT和氢疗法联系起来,旨在探索未来声敏剂设计的可行性。
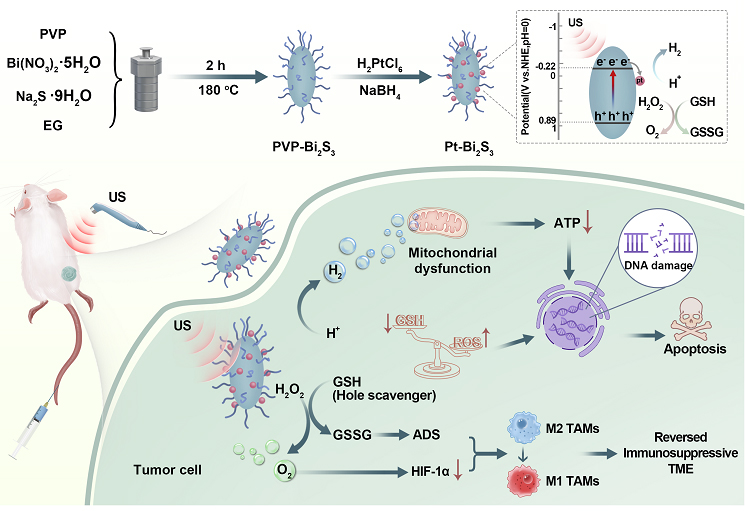
图1. Pt-Bi2S3纳米催化剂声催化析氢机制及诱导癌细胞凋亡过程示意图。
该研究采用具有合适能带结构的Bi2S3纳米棒作为声催化剂,并通过原位生长铂 (Pt) 纳米粒子来优化其催化性能。在US照射下,声激发的电子可以通过肖特基结从Bi2S3纳米棒表面转移到Pt纳米粒子的费米能级,并且能带弯曲可以防止电子回流。同时,Bi2S3纳米棒价带上的空穴将被天然的空穴牺牲剂GSH消耗。这两者的共同作用提高了Pt-Bi2S3纳米声催化体系中载流子的分离效率,促进H2长期稳定生成。该纳米声催化体系在体内外均表现出优异的产氢性能和消耗GSH的能力,并通过抑制细胞内能量代谢和破坏肿瘤的抗氧化防御系统来诱导肿瘤细胞凋亡,抑制肿瘤生长。此外,Pt纳米粒子和声激发空穴还能够催化H2O2生成O2来缓解肿瘤缺氧,从而与GSH耗竭协同逆转免疫抑制TME。重要的是,这种基于声催化的治疗策略不仅可以在低氧环境中杀死癌细胞,还可以通过破坏TME抑制癌细胞的继续增殖,有望成为一种临床可行的癌症治疗方式。
这一成果近期发表在Advanced Materials 上,中国科院长春应用化学研究所博士研究生袁梦为论文第一作者。中国科学院长春应用化学研究所林君研究员和马平安研究员、广东医科大学程子泳教授为本文的共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Rational Design of Platinum-Bismuth Sulfide Schottky Heterostructure for Sonocatalysis-Mediated Hydrogen Therapy
Meng Yuan, Shuang Liang, Ling Yang, Fang Li, Bin Liu, Chunzheng Yang, Zhuang Yang, Yulong Bian, Ping'an Ma, Ziyong Cheng, Jun Lin
Adv. Mater., 2022, DOI: 10.1002/adma.202209589
导师介绍
林君
https://www.x-mol.com/university/faculty/15805
马平安
https://www.x-mol.com/university/faculty/281066
程子泳
https://www.x-mol.com/university/faculty/47833
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!

















































 京公网安备 11010802027423号
京公网安备 11010802027423号