中国药科大学J. Med. Chem.:全面解析小分子雄激素受体(AR)降解剂的研究进展及发展方向
前列腺癌(PC)是全球男性第二大恶性肿瘤,已被证实高度依赖于雄激素受体(AR)信号的异常激活。长期使用雄激素剥夺疗法(ADT)治疗前列腺癌会不可避免地导致去势抵抗性前列腺癌(CRPC),大量研究表明在CRPC中AR仍然是关键的致癌驱动因素。尽管已经有多代AR拮抗剂(如恩扎鲁胺)进入临床使用,但多种机制导致的抗雄激素耐药性在CRPC中依然会迅速出现。因此,迫切需要制定新的策略来解决这一未被满足的临床需求。靶向AR降解的研究近年来正处于蓬勃发展阶段,越来越多的临床研究强调了AR降解剂对CRPC患者的益处。近日,中国药科大学向华团队在Journal of Medicinal Chemistry 上发表了题为“A Comprehensive Overview of Small-Molecule Androgen Receptor Degraders: Recent Progress and Future Perspectives”的综述文章,全面总结了近20年来小分子雄激素受体(AR)降解剂的构效关系、生物医学应用与临床疗效,并剖析了该领域未来的发展方向(图1)。中国药科大学药学院向华教授和骆国顺副研究员为文章共同通讯作者,课题组2021级硕士研究生哈斯为文章第一作者。
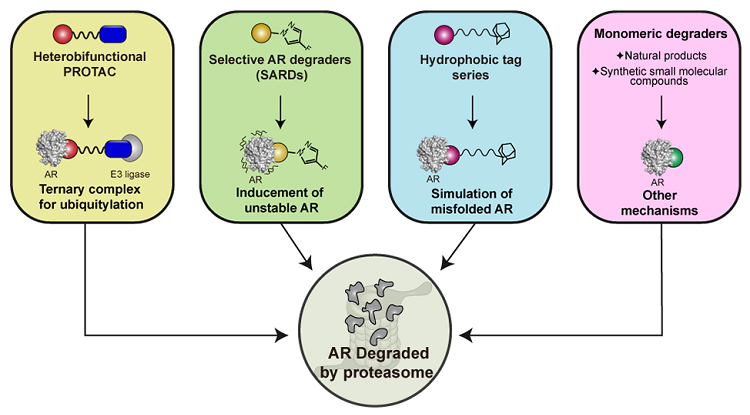
图1. 文章内容的图片摘要
AR蛋白主要分为三个功能域,从N端到C端依次为内在无序的N端结构域NTD,高度保守的DNA结合结构域DBD,以及由铰链区相连的配体结合结构域LBD。其中,LBD区含有一个隐藏的口袋,该口袋被称为雄激素结合位点,也是现有AR拮抗剂的主要作用位点。抗雄激素治疗一段时间后,AR-LBD区会产生点突变和剪接变异,是导致耐药的重要机制(图2)。
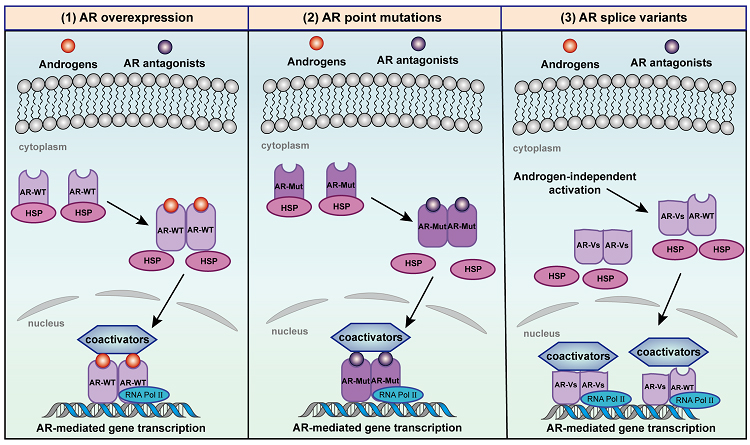
图2. 诱发抗雄激素耐药的机制包括AR过表达、AR点突变和缺乏LBD的AR剪接变异体
在本文中作者全面总结了具有不同作用机制的小分子AR降解剂,包括AR蛋白水解靶向嵌合体(AR PROTACs)、选择性AR降解剂(SARDs)、疏水标签AR降解剂(HyT)和其他具有不同作用机制的AR降解剂(图3)。作者希望通过本工作为基于AR降解策略治疗CRPC提供参考和有价值的见解。
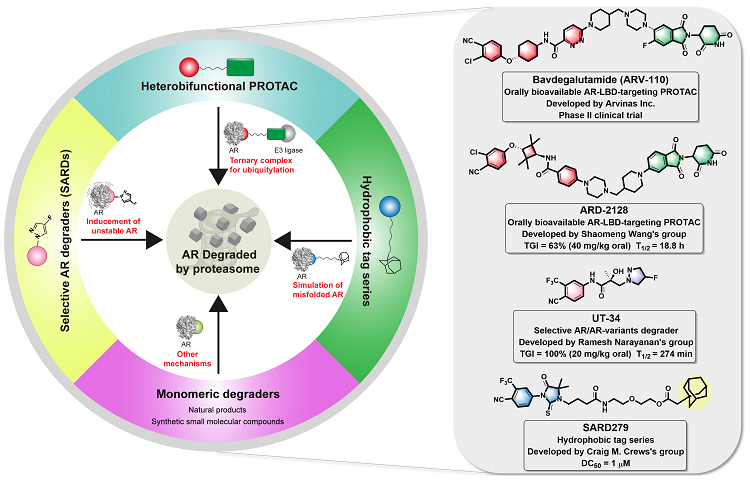
图3. 现有靶向降解AR的策略及其相应的代表性化合物
在AR PROTACs部分,作者首先阐明了PROTAC的作用机制,然后按靶向AR蛋白LBD和DBD两个不同功能域分类,从论文、专利以及临床实验等多角度详尽介绍了数十种已被报道的AR PROTACs(图4,表1),并对正处于临床Ⅱ期的明星分子ARV-110(Bavdegalutamide)(图5)以及其它代表性PROTACs的结构改造思路进行了详细阐述,可能为未来AR PROTACs的开发提供有价值的参考。
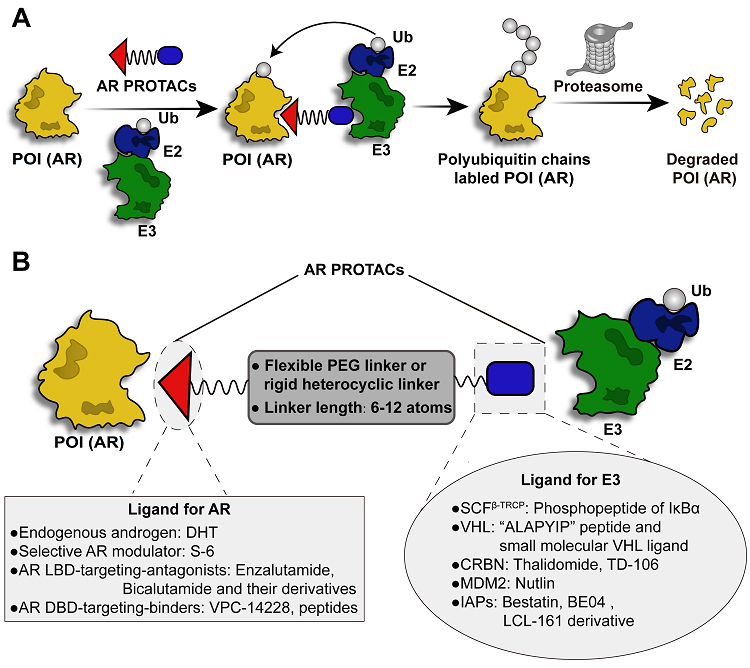
图4.(A)PROTACs与E3连接酶和靶蛋白(POI)形成三元复合物,E3 连接酶介导泛素结合酶 E2 对 POI 泛素化标记,最终POI通过26S蛋白酶体被降解;(B)现有AR PROTAC的化合物结构组成总结
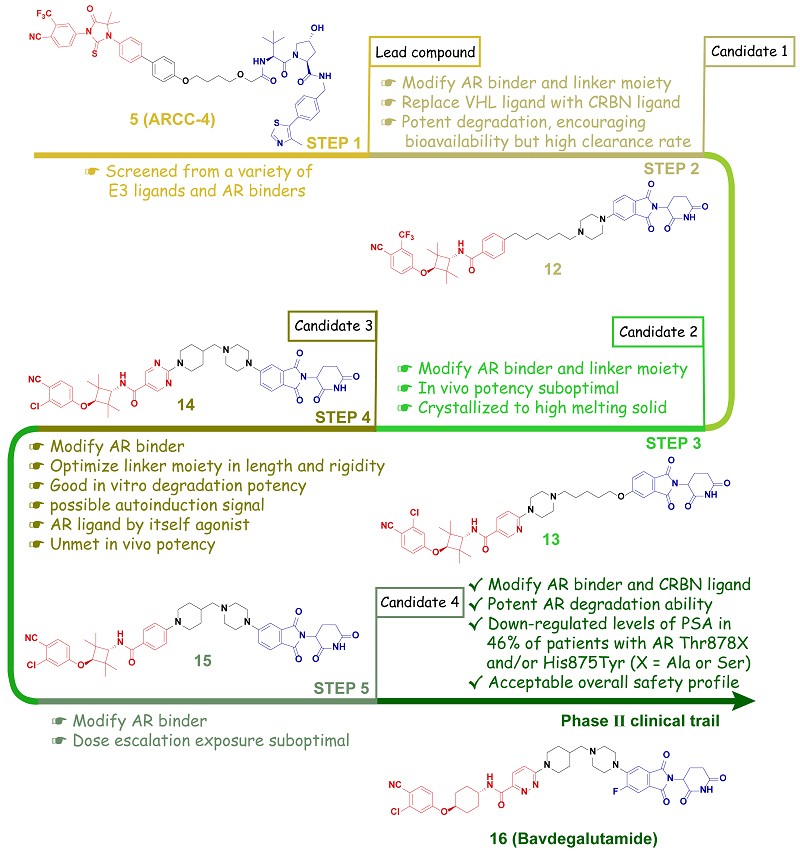
图5. Arvinas公司在2021年公布的ARV-110(Bavdegalutamide)的结构改造思路
表1. 除Bavdegalutamide外在临床试验阶段中的代表性AR PROTACs
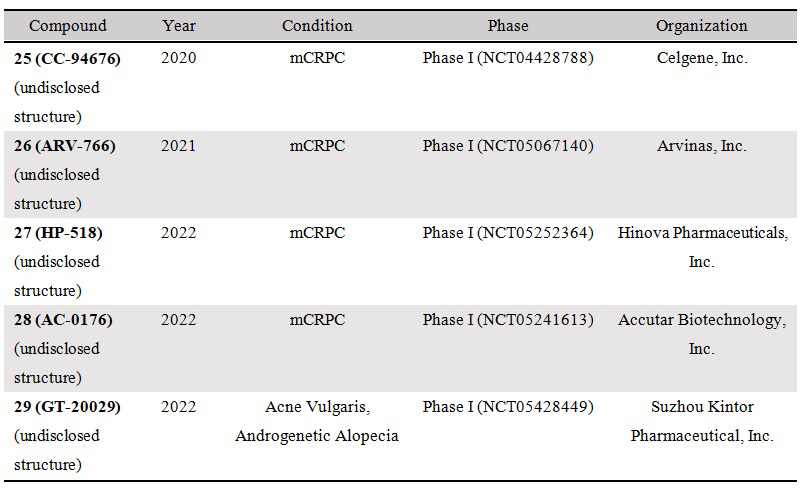
注:mCRPC指转移性去势抵抗性前列腺癌
在选择性AR降解剂(SARDs)部分,作者介绍了Galeterone及其衍生物、UT系列以及Darolutamide衍生物等一系列能选择性降解AR的小分子降解剂。尤其值得关注的是UT系列中能靶向AR NTD区的降解剂(如UT-155)为克服AR剪接变异体耐药提供了可行的思路(图6)。
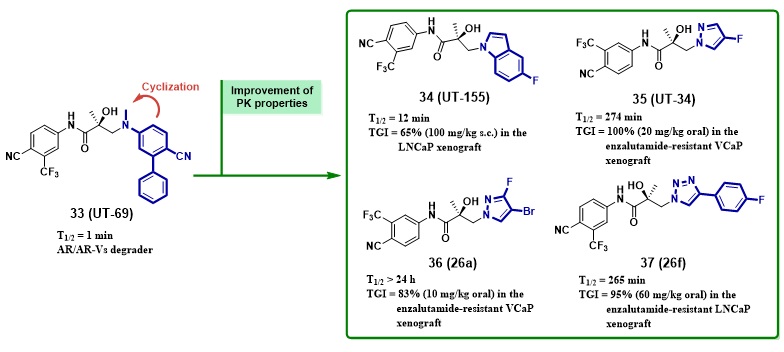
图6. 靶向AR NTD和LBD的“UT系列”SARDs的结构改造与活性数据
在疏水标签AR降解剂(HyT)部分,作者介绍了几种以金刚烷作为疏水标签的AR降解剂,其可以模拟体内蛋白错误折叠构象进而引发AR降解(图7)。
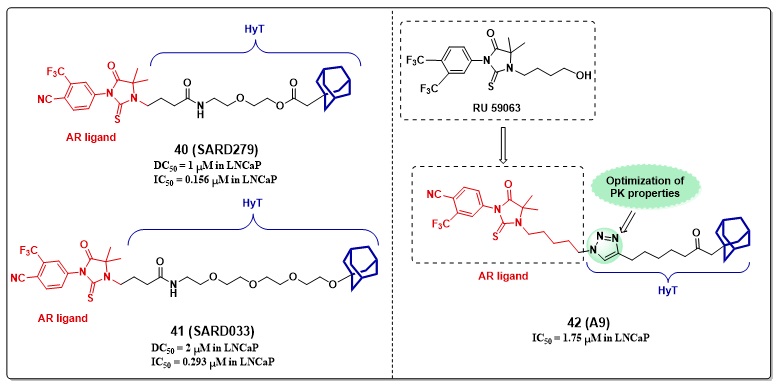
图7. 疏水标签AR降解剂(HyT)结构与活性数据
在其他具有不同作用机制的AR降解剂部分,作者从天然产物、老药新用、处于临床或临床前研究阶段的AR降解剂几个角度介绍了数十种作用机制有待深入探究的AR降解剂。对于这类化合物的作用机制研究,作者在展望部分提出了可以从分子胶的概念入手进行探索。分子胶是一种蛋白-蛋白相互作用调节剂,可以结合在蛋白质的表面或界面上,填补间隙并稳定与新底物的相互作用,最终导致细胞反应的激活或抑制(图8)。
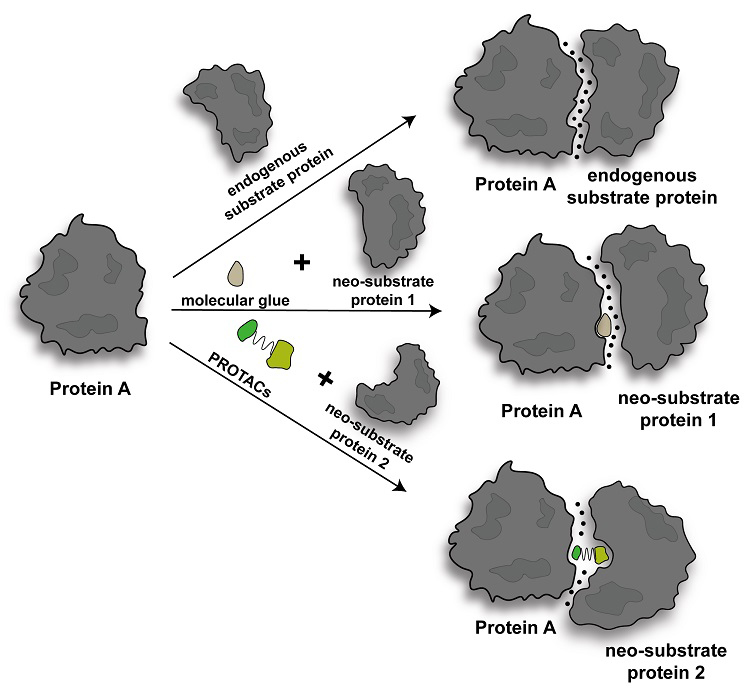
图8. PROTAC与分子胶作用模式对比
小结
综上所述,大多数CRPC的病理机制依赖于AR轴信号通路的激活。然而,现有临床治疗CRPC的AR靶向抑制剂未能规避AR异常引起的耐药。在临床前和临床研究中,靶向AR降解策略已经获得了良好的概念验证结果,一些小分子AR降解剂有望成为未来治疗CRPC的主导力量。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Comprehensive Overview of Small-Molecule Androgen Receptor Degraders: Recent Progress and Future Perspectives
Si Ha, Guoshun Luo*, and Hua Xiang*
J. Med. Chem., 2022, DOI: 10.1021/acs.jmedchem.2c01487
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号