Chem:非金属催化脂肪胺的选择性自由基α-C-H键硼化
α-氨基硼酸广泛应用于有机合成、材料科学和药物研发中(图1),代表性药物包括Bortezomib(治疗多发性骨髓瘤)、Vaborbactam(β-内酰胺酶抑制剂)、Dutogliptin(DPP-4抑制剂)、Taniborbactam(β-内酰胺酶抑制剂)。传统的α-氨基硼酸合成方法往往需要对起始原料进行预官能团化并经历多步合成,因此原子经济性和步骤经济性不高。相比之下,通过胺的α-C-H键硼化反应来制备α-氨基硼酸酯或许是一个不错的选择,例如过渡金属(TM)催化的导向C-H键活化或在强碱性条件下去质子化(图2A),这两种情况都涉及碳金属化中间体(A和B)。尽管如此,但是过渡金属催化的反应通常需要加热、安装/脱除导向基并且仅限于末端或者活化的2°C-H键,而后一种方法则需要强碱条件并且仅在三级苄基位点进行反应。因此,迫切需要发展一种条件温和、操作简单且通用的C-H键硼化方法。

图1. α-氨基硼酸类药物。图片来源:Chem
近年来,二硼试剂(自由基捕获剂)参与的无金属硼化反应受到了化学家们的广泛关注。在此基础上,美国德克萨斯大学达拉斯分校(UT Dallas)的Vladimir Gevorgyan教授课题组尝试利用市售且易安装和脱除的2-碘苯甲酰基(BzI)为导向基(DG),在光诱导下发生单电子还原形成芳基自由基D,后者经1,5-HAT得到关键的α-氨基烷基自由基E,最后被二硼试剂捕获便可获得所需的氨基硼酸盐(图2B)。然而,该过程面临着以下挑战:1)反应性更强的芳基自由基D过早硼化;2)α-氨基烷基自由基E发生环化或去饱和化;3)自由基D或E通过分子间HAT进行加氢脱卤。近日,他们报道了非金属催化脂肪胺的α-C-H键硼化反应,高区域选择性、非对映选择性地制备了一系列有价值的α-氨基硼酸酯。该反应不仅条件温和、操作简单、底物范围广、官能团耐受性好,而且还能实现结构复杂胺和药物分子的后期硼化以及胺的形式C-H键芳基化反应。相关成果发表在Chem 上。

图2. 胺的导向α-C-H硼化。图片来源:Chem
首先,作者选择2-碘苯甲酰基保护的二丁胺2c为模型底物对反应条件进行优化,并得到最佳条件:即在双(邻苯二酚)二硼酸酯(B2cat2,3.5 equiv.)为二硼试剂、Et3N(4.0 equiv.)为碱、DMA(0.1 M)为溶剂的条件下用427 nm LED照射48 h,能以80%的分离产率得到目标产物3c(图3)。另外,环状哌啶底物2j也能以72%的分离产率进行硼化反应,而带有2-碘苯基亚砜基(2am)、2-碘代苯磺酰基(2an)和2-碘代苄基(2ao、2ap)的哌啶底物则主要形成相应的还原(3-A)和去饱和化(3-B)副产物,硼化产物3痕量或没有。

图3. 条件优化。图片来源:Chem
在最佳反应条件下,作者对该反应的底物范围进行了考察(图4),结果显示各种链状脂肪胺(3a-3e)、不同环大小(3j-3l)及各种基团取代(3m-3x)的氮杂环均能兼容该反应,以中等至较好的产率得到所需产物,其中C-4取代的氮杂环(3q、3t-3x)能得到单一的非对映异构体。类似地,C-2取代的哌啶(如:氨基酸3y、氨基醇3z)以及含多种弱C-H键的哌啶衍生物(3ab)也能实现高区域选择性和非对映选择性硼化,尽管3y和3z产率较低。然而,具有竞争性α-一级和二级C-H位点的链状脂肪胺则得到了区域异构体混合物(3f/3f'和3g/3g',可通过柱色谱分离),并且反应倾向于二级C-H位点。另外,当底物中存在C-H键解离能(BDE)较低的三级位点时,仍优先在一级(3h)或二级(3i)C-H位点进行硼化反应,这可能是由于空间位阻所致。值得一提的是,该反应还能实现复杂氮杂环底物(3ac-3ah)和药物分子(3ai-3an)的后期修饰,进一步凸显出该方案对复杂胺底物进行后期官能团化的可行性。其次,作者还以中等至较好的产率得到其它硼酸酯(3ja-3jd),其中儿茶酚硼酸酯(3ja)可被氟盐淬灭得到氟硼酸盐(3jb),或者经原位酯交换得到丙二醇-(3jc)和(+)-蒎二醇(3jd)硼酸酯,后者常用于立体选择性合成。需要指出的是,该方法获得的产物和Hartwig课题组发展的硼化方法(Science, 2020, 368, 736,点击阅读详细; J. Am. Chem. Soc. 2012, 134, 12422)得到的产物形成了互补的区域选择性(图5A、5B)。
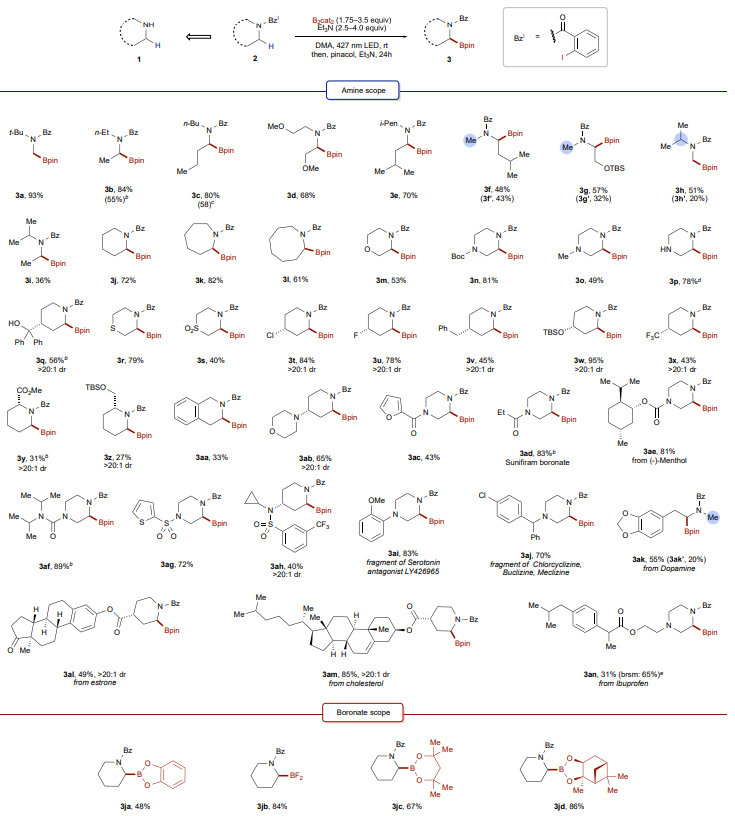
图4. 胺的底物范围。图片来源:Chem

图5. 所开发方法与现有导向硼化方法的互补。图片来源:Chem
接下来,作者进行了规模化实验(图6A),向标准条件下加入1.5 equiv. B2cat2后,可以良好的产率获得无环(3a)和环状氨基硼酸酯(3j、3t、3v)。另外,作者还对产物3进行了衍生化(图6B),具体而言:1)经Suzuki-Miyaura交叉偶联反应得到相应的芳基化产物(4a-4c);2)经Matteson同系化反应得到β-氨基硼酸酯4d,后者可进一步转化为β-氨基醇衍生物4e或者γ-氨基硼酸酯4f;3)在LiBH4的作用下脱导向基,接着经酰化得到一系列衍生物(4j-4m,图6C)。
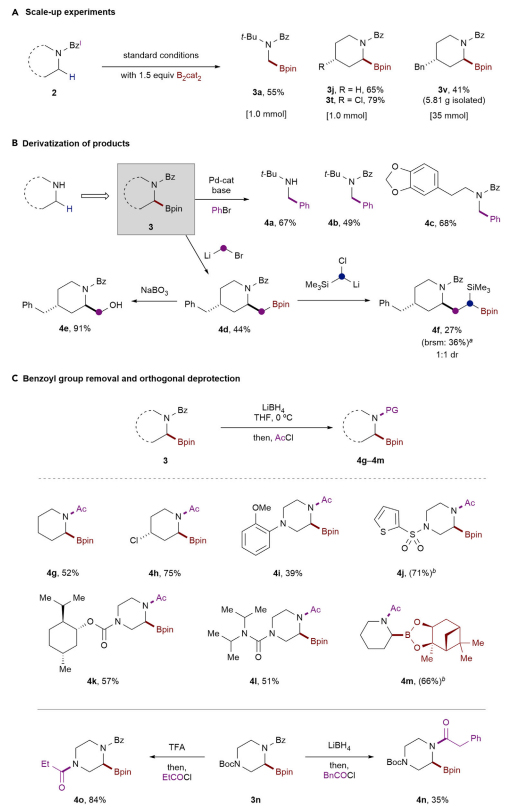
图6. 合成应用。图片来源:Chem
为了进一步探究反应机理,作者进行了一系列实验。具体而言:1)TEMPO参与的自由基捕获实验得到了痕量的硼化产物3a՛՛和9%的TEMPO-加合物5a(图7A),而自由基重排实验则得到了三元环开环产物6aq(图7B),两者均表明该反应涉及自由基中间体;2)氘代标记实验中观察到完全的氘原子转移(2j-D→3j-D),这进一步证实了选择性1,5-HAT过程(图7C);3)light on/off实验结果和量子产率值(2.6)表明该过程可能涉及自由基链式反应机理。

图7. 机理研究。图片来源:Chem
基于上述实验结果和文献报道,作者提出了可能的反应机理(图8):首先,2与B2cat2的络合物F在光照下得到中间体F*,后者通过单电子转移(SET)断裂C-I键并得到亲电性芳基自由基D。接着,D通过极性匹配的1,5-HAT过程生成亲核性的α-氨基烷基自由基E,后者与L•B2cat2发生自由基加成得到硼化产物G和硼基自由基H,其中H能与底物2通过卤原子转移(XAT)或单电子转移机理实现自由基链传递,而硼化产物G则能通过原位酯交换得到可分离的频哪醇硼酯产物3。需要指出的是,N-苯甲酰基在该反应中起到了至关重要的作用:1)提供了足够的Thorpe-Ingold效应;2)为1,5-HAT过程提供了有效的极性匹配;3)有效抑制α-氨基烷基自由基的自由基极性交叉(radical-polar crossover,RPC)以生成副产物3-B,从而有利于被二硼试剂捕获。

图8. 可能的反应机理。图片来源:Chem
总结
Vladimir Gevorgyan教授课题组报道了一种通用的脂肪胺α-C(sp3)-H键硼化方法,可以高区域选择性和非对映选择性地实现具有重要应用价值的α-氨基硼酸酯的合成。该反应不仅条件温和、底物范围广、官能团耐受性好,而且无需使用过渡金属和强碱。毫无疑问,该反应的发展为脂肪胺的α-C(sp3)-H键硼化过程提供了新的思路,预计这种操作简单、通用且实用的方法将在有机合成和药物发现中得到广泛应用。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

General and selective metal-free radical α-C–H borylation of aliphatic amines
Sumon Sarkar, Sidhant Wagulde, Xiangqing Jia, Vladimir Gevorgyan
Chem, 2022, DOI: 10.1016/j.chempr.2022.07.022
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
Science:非导向硼化开启烷基强C-H键多样性官能团化 2020-05-19
-
铱催化C(sp3)−H硼化区域选择性的内在控制因素与催化剂精准设计 2022-08-29
-
ACS Catal.:手性α-氨基硼酸衍生物的不对称催化氢化合成 2020-04-28
-
Nature:无金属参与的烷烃C(sp³)-H键硼化反应 2020-11-04
-
铱催化环丙胺的不对称C-H键硼化反应 2022-03-09
-
Metal-free selective acylation reaction of aliphatic alcohols in neutral conditionJournal of the Iranian Chemical Society (IF 2.2) Pub Date : 2022-11-24 ,DOI:10.1007/s13738-022-02694-6Babak Kaboudin, Rasul Pourbafarani, Sajedeh Alavi, Foad Kazemi, Hiroshi Aoyama


































 京公网安备 11010802027423号
京公网安备 11010802027423号