中山大学吴桐/谭彩萍/程斌/毛宗万Biomaterials:Ru(II)配合物修饰的TiO2纳米颗粒提供口腔鳞癌光免疫治疗新策略
口腔鳞癌是头颈部常见的恶性肿瘤之一,局部乏氧和免疫抑制是口腔鳞癌常规治疗效果不佳的重要原因。近年来利用光敏剂在特定波长光照射后生成活性氧(ROS)杀伤肿瘤细胞的光动力疗法(PDT)在临床取得一定效果,但传统PDT药物的高氧依赖性限制其进一步广泛应用。
近日,中山大学附属口腔医院吴桐副主任医师、程斌教授团队联合中山大学化学学院的谭彩萍教授、毛宗万教授团队设计了一种通过Ru(II)配合物修饰TiO2纳米粒子,并负载HIF-1α siRNA的新型纳米颗粒TiO2@Ru@siRNA。在可见光照射下,该纳米颗粒能显著上调细胞ROS水平,诱导细胞焦亡;通过介导溶酶体损伤,促使HIF-1α siRNA逃逸,改善肿瘤局部乏氧状态。同时该纳米颗粒通过HMGB1-NF-KB-PDL1轴下调肿瘤细胞PDL1水平,促进抗肿瘤细胞因子IL-24分泌增加,激活CD4+和CD8+ T细胞,重塑局部免疫微环境。在4NQO诱导的大鼠舌癌模型和人源异种移植瘤(PDX)小鼠模型中,TiO2@Ru@siRNA遏制上皮恶性转化,增强局部免疫,抑制肿瘤生长的效果均得到进一步验证。综上,该新型纳米颗粒TiO2@Ru@siRNA能够改善肿瘤局部乏氧状态,产生较强的光动力效应,同时重塑局部免疫抑制微环境,增强肿瘤杀伤作用。基于该纳米颗粒的光免疫治疗策略为口腔鳞癌的防治提供了一种新策略。
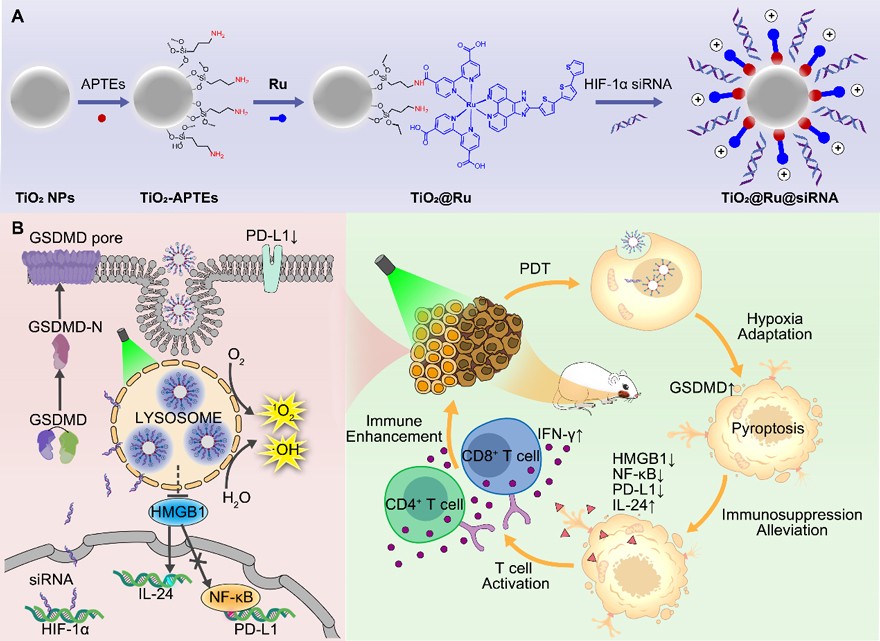
图1. TiO2@Ru@siRNA纳米颗粒合成及介导口腔鳞癌光免疫治疗模式图
相关结果已在Biomaterials 发表。吴桐副主任医师、谭彩萍教授、程斌教授、毛宗万教授为本文的共同通讯作者。周嘉颖(博士研究生)、汪文锦博士、张晨雨(硕士研究生)及凌钰怡(博士研究生),为本文的共同第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Ru(II)-modified TiO2 nanoparticles for hypoxia-adaptive photo-immunotherapy of oral squamous cell carcinoma
Jia-Ying Zhou, Wen-Jin Wang, Chen-Yu Zhang, Yu-Yi Ling, Xiao-Jing Hong, Qiao Su, Wu-Guo Li, Zong-Wan Mao, Bin Cheng, Cai-Ping Tan, Tong Wu.
Biomaterials, 2022, 289, 121757, DOI: 10.1016/j.biomaterials.2022.121757
导师介绍
谭彩萍
https://www.x-mol.com/university/faculty/15392
毛宗万
https://www.x-mol.com/university/faculty/15322
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!






















































 京公网安备 11010802027423号
京公网安备 11010802027423号