西交大李菲课题组Anal Chem:电位可编程扫描电化学显微镜用于体外心肌组织原位定量表征的研究
模拟在体心肌组织生理、结构特征的体外心肌组织模型是心脏疾病治疗和研究的重要工具,被广泛应用于心脏生理、病理机制研究以及新药药效和毒性筛查中。然而,在体外心肌组织的应用研究中,使用传统表征手段无法原位检测可直接表现其代谢活性和电生理状态的三个重要指标:呼吸活性、氧化应激(如H2O2)水平、搏动频率。这是由于心肌组织的这三个指标对外源性刺激响应迅速,并且与心肌组织的即时状态密切相关,易受检测手段自身的干扰。因此,需要可表征心肌组织这三个参数非侵入式的原位表征新技术。扫描电化学显微镜(scanning electrochemical microscopy, SECM)作为一种微区电化学技术,可实现对活细胞或组织所消耗或释放化学小分子的高时空分辨的原位、无标记检测,可作为原位表征体外心肌组织呼吸活性、H2O2水平和搏动频率的理想工具。
近日,西安交通大学生命科学与技术学院仿生工程与生物力学研究所 (BEBC) 李菲(点击查看介绍)课题组构建了体外心肌组织模型,结合电位可编程的SECM技术实现了对体外心肌组织的呼吸活性、H2O2水平、搏动频率以及药物(异丙肾上腺素、普萘洛尔)作用下心肌组织即时响应行为的原位、实时表征(图1)。
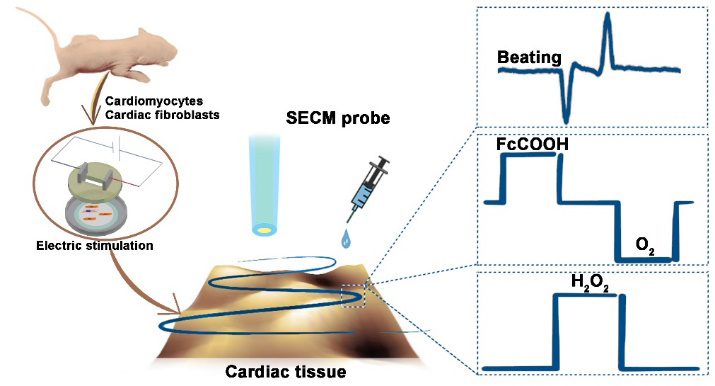
图1. 使用电位可编程的SECM技术检测体外心肌组织的呼吸活性、H2O2水平和搏动频率以及药物(异丙肾上腺素、普萘洛尔)的即时响应行为。图片来源:Anal. Chem.
该工作首先通过在聚丙烯酰胺水凝胶上对小鼠的心肌细胞和心肌成纤维细胞进行了共培养,并通过对细胞进行电刺激实现了体外心肌组织模型的构建。之后,以FcCOOH为氧化还原电对,应用SECM结合在探针电极上施加可编程的脉冲波形电位技术,实现了对心肌组织的形貌和呼吸活性的同时且长时间的追踪与电化学成像(图2)。其中,脉冲电位技术的使用减少了由于探针上施加氧气还原电位时造成的探针周围低氧环境对心肌组织正常生理状态的影响;可编程电位技术通过在探针上依次施加FcCOOH的氧化电位和氧气的还原电位,实现了对心肌组织的形貌和耗氧量的同时表征。之后,使用该方法原位表征了异丙肾上腺素(一种β受体激动剂)和普萘洛尔(一种β受体抑制剂)两种药物作用下心肌组织的形貌和呼吸活性。结果表明,加入两种药物后心肌组织的形貌没有明显变化,但异丙肾上腺素作用下心肌组织的呼吸活性呈现先上升后恢复的趋势,而普萘洛尔作用下心肌组织的呼吸活性呈现先平稳后下降的趋势。该结果证实了应用SECM结合探针可编程的脉冲波形电位技术可原位表征心肌组织的呼吸活性在β受体激活和阻断剂存在下的增强或减弱现象。
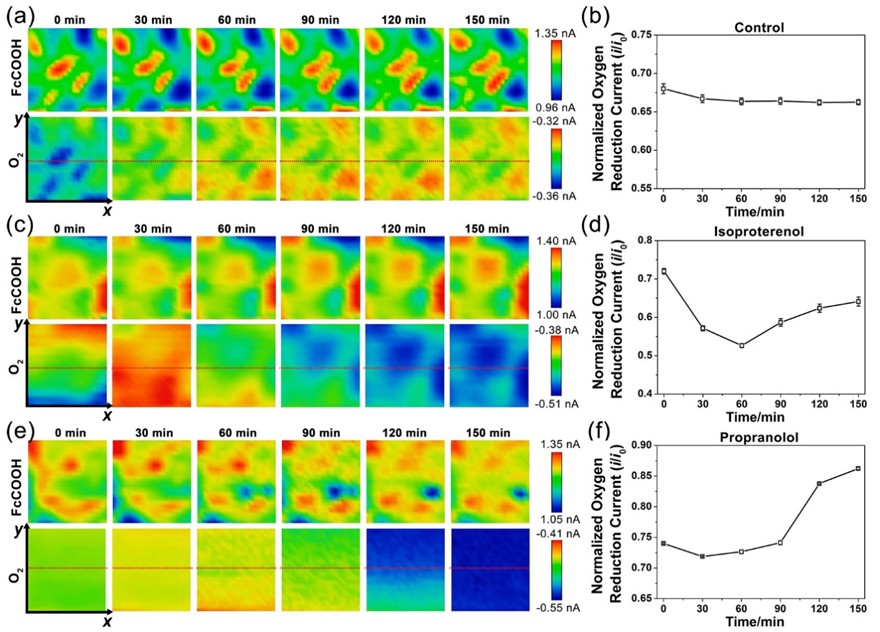
图2. (A) 应用SECM同时表征(a,b)未加入药物、加入(c,d)0.5 μM异丙肾上腺素和(e,f)0.5 μM普萘洛尔的心肌组织呼吸活性和形貌变化的(a,c,e)SECM图像和(b,d,f)归一化的氧化还原电流。图片来源:Anal. Chem.
另外,以FcCOOH为氧化还原电对,应用SECM通过检测心肌组织跳动时探针表面的FcCOOH氧化电流的变化,原位检测了异丙肾上腺素和普萘洛尔加入后心肌组织搏动频率的变化(图3)。由结果可知,心肌组织在异丙肾上腺素加入后搏动频率由1 Hz迅速增加至1.5 Hz左右,之后逐渐恢复至初始的1 Hz状态。而加入普萘洛尔后,心肌组织的搏动频率持续下降(由1 Hz下降至0.7 Hz左右),之后保持稳定。

图3. 应用SECM表征(a)未加入药物,加入(b)0.5 μM异丙肾上腺素和(c)0.5 μM普萘洛尔后心肌组织搏动频率的电流-时间曲线;(d)心肌组织的搏动频率和时间的关系图。图片来源:Anal. Chem.
最后,通过对探针施加H2O2的脉冲氧化电位,应用SECM原位检测了异丙肾上腺素和普萘洛尔加入后心肌组织的H2O2水平的即时变化(图4)。结果表明,异丙肾上腺素加入后心肌组织周围的H2O2浓度迅速增加5 μM左右,而普萘洛尔加入后心肌组织周围的H2O2浓度未发生明显变化。该结果证实了应用SECM结合脉冲电位技术可即时检测药物作用下心肌组织H2O2释放速率的变化。
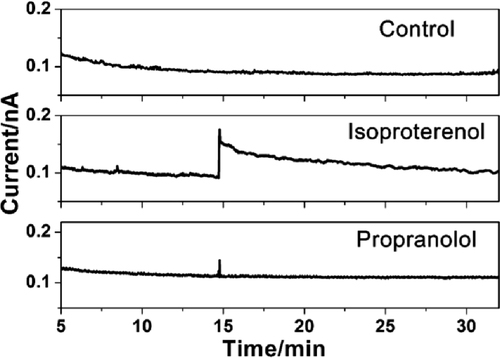
图4. 应用SECM检测未加入药物、加入0.5 μM异丙肾上腺素和0.5 μM普萘洛尔后心肌组织的H2O2氧化电流的电流-时间曲线。图片来源:Anal. Chem.
该工作首次应用SECM结合可编程脉冲电位技术实现了对体外心肌组织的呼吸活性、搏动频率和H2O2释放的原位、实时表征,为心肌组织的代谢和电生理特性的原位、定量表征提供了SECM新技术。该研究成果发表在美国化学会杂志Analytical Chemistry 上。该文章第一作者是西安交通大学博士生李亚北,通讯作者为西安交通大学李菲教授,其他作者还包括西安交通大学研究生叶朝阳、张俊杰、赵宇翔、朱彤、宋静静和徐峰教授等。该工作也得到美国哈佛仪器公司Frank Wang博士在SECM仪器方面的帮助,以及国家自然科学基金、陕西省自然科学基金、陕西省重点研发计划和中央高校基本科研业务费等项目的资助。
李菲教授课题组遵循“生命科学基础问题-电化学扫描探针显微镜平台研制-细胞原位电化学成像与表征”的学术思路,立足于电分析化学方法与技术,结合组织工程学、生物力学和医学等学科,开展疾病相关细胞物理微环境对细胞形态和化学等行为的原位电化学成像和细胞界面过程动力学研究,探究细胞微环境与细胞病理学的关系。该工作是李菲教授课题组自针对心肌纤维化疾病相关的心肌和心肌成纤维细胞氧化还原状态的SECM研究(Anal. Chem., 2020, 92, 4771-4779; Anal. Chem., 2021, 93, 5797–5804)后,将研究体系从心肌细胞拓展到心肌组织水平的SECM应用研究新成果。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

In Situ and Quantitative Monitoring of Cardiac Tissues Using Programmable Scanning Electrochemical Microscopy
Yabei Li, Zhaoyang Ye, Junjie Zhang, Yuxiang Zhao, Tong Zhu, Jingjing Song, Feng Xu, and Fei Li*
Anal. Chem., 2022, DOI: 10.1021/acs.analchem.2c01919
导师介绍
李菲
https://www.x-mol.com/university/faculty/13704
课题组主页链接
http://gr.xjtu.edu.cn/web/feili
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号