无痕活化及导向基策略构建4-取代-3-三氟甲基吡唑
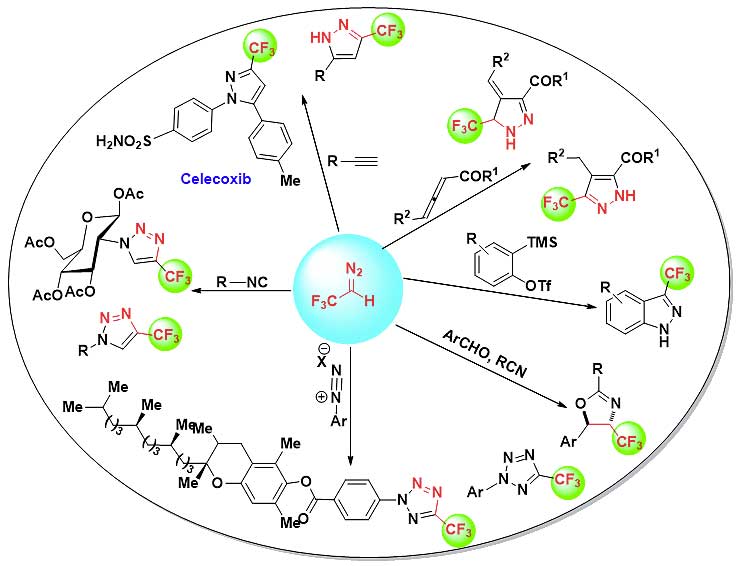
3-三氟甲基吡唑是许多药物、农药及相关生物活性分子的重要结构骨架,如何高效构建这类化合物受到有机化学家们的关注。传统制备3-三氟甲基吡唑的方法主要是通过3-三氟甲基-1,3-二羰基化合物与相应的肼类化合物缩合制得。但原料的难以制备以及反应的区域选择性大大限制了该方法的发展。分子间的偶极环加成反应是高效构建碳环以及杂环化合物的方法之一。在过去的十年里,2,2,2-三氟重氮乙烷作为一种有效的合成子,广泛应用于各种含氟化合物的合成。天津大学的马军安(点击查看介绍)团队一直致力于2,2,2-三氟重氮乙烷的反应性研究,合成了一系列三氟甲基杂环化合物,如5-位取代-3-三氟甲基吡唑(Angew. Chem. Int. Ed., 2013, 52, 6375-6378)、4,5-位双取代的3-三氟甲基吡唑(Org. Lett., 2014, 16, 3122-3125)、三氟甲基吲唑(J. Fluorine Chem., 2015, 174, 88-94)、三氟甲基三唑(Org. Chem. Front., 2015, 2, 1468-1474)、三氟甲基四唑(Chem. Commun., 2015, 51, 16545-16548)以及三氟甲基二氢噁唑化合物(Chem. Commun., 2015, 51, 8946-8949),并将部分反应作为关键步骤,成功用于相关药物和活性化合物的合成。
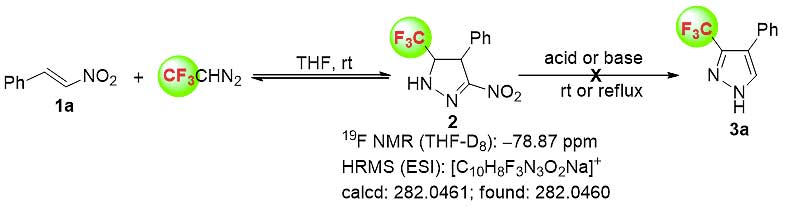
最近,该团队又利用无痕活化及导向基团的策略发展了一种构建4-取代-3-三氟甲基取代吡唑类化合物的方法。他们以硝基苯乙烯1a以及三氟重氮乙烷为起始原料,研究发现在室温条件下就能以13%的转化率得到环加成中间体2,当将三氟重氮乙烷的量增加到八个当量时,转化率可以提高到27%。高分辨质谱进一步确定了该中间体的结构。遗憾的是,该中间体无法分离,且改变反应温度、投料比以及向体系中加入碱或者酸均不能使该中间体转化为目标产物。随后作者发现,银盐可以有效地促进硝基烯烃向目标产物转化,经过一系列条件筛选确定了最佳反应条件。
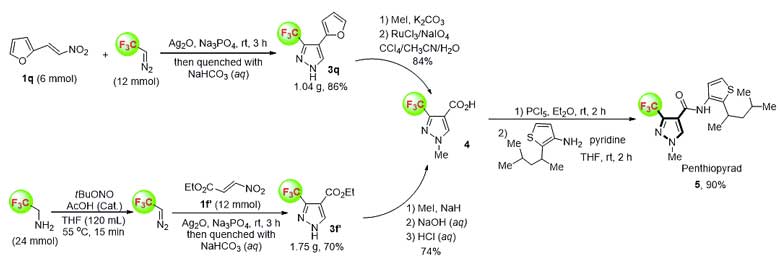
在最佳反应条件下,作者对底物的适用性进行了考察。他们发现苯环上无论带有吸电子取代基,还是供电子取代基,该反应均能很好地进行;稠环以及杂环取代的硝基烯烃如1-萘基、2-萘基、9-蒽基、2-呋喃基、2-噻吩基、2-吡啶基以及3-吡啶基的底物也能很好地适用于该反应体系;肉桂基以及苯乙炔基取代的硝基烯烃也是很好的反应底物。同时,该反应也可以用于多种脂肪族取代的3-三氟甲基吡唑合成。多氟重氮烷烃作为底物时,也可以中等产率得到相应多氟烷基取代的吡唑。重氮化合物也可以通过原位生成法制备。除此之外,作者还将该方法应用于抗菌剂penthiopyrad的合成。
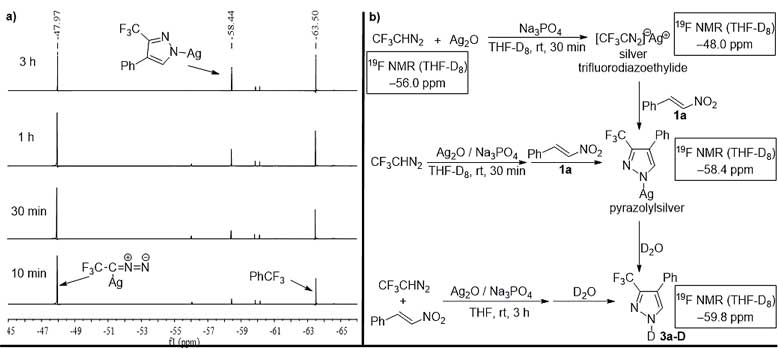
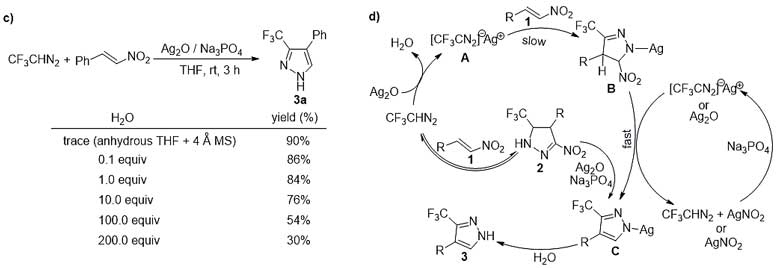
作者进一步研究了该反应的机理,通过氟谱跟踪实验,他们发现随着时间的推移,体系中出现了两个新的特征峰(‒48.0 和 ‒58.4 ppm)。他们通过对照实验及核磁波谱结构分析,确证这两个新的特征峰分别对应三氟重氮乙基银(‒48.0 ppm)以及吡唑银(‒58.4 ppm)中间体。作者还发现随着反应体系中水含量的增加,反应的产率逐渐降低,因此,过量的水对该反应是不利的。基于此,作者提出了该反应可能的机理,首先三氟重氮乙烷与氧化银作用生成三氟重氮乙基银中间体A,随后与硝基烯烃反应生成中间体B,该步骤是反应的决速步,中间体B一旦生成,就会在碱的作用下立刻消除一分子亚硝酸生成吡唑银中间体C,进一步水解得到目标产物3。虽然反应形成中间体2非常缓慢,但经过该中间体转化为目标产物的历程也不能排除。
这一成果近期发表在Angew. Chem. Int. Ed. 上。
该论文作者为:Zhen Chen, Yan Zheng, and Jun-An Ma
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Use of a Traceless Activating and Directing Group for the Construction of Trifluoromethylpyrazoles: One-Pot Transformation of Nitroolefins and Trifluorodiazoethane
Angew. Chem. Int. Ed., 2017, 56, 4569-4574, DOI: 10.1002/anie.201700955
导师介绍
马军安
http://www.x-mol.com/university/faculty/13330
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号