Nat. Chem.:光启动的精准四嗪生物正交化学
近年来,一系列新兴的生物正交化学方法陆续涌现,并被广泛应用于生物学和医学研究。其中,四嗪生物正交反应的反应速率高,生物相容性好,是最常用的生物正交化学工具之一。不过在生物体内,如何进行高时间和空间精准度的四嗪正交反应,目前仍处于探索阶段。可见光具有无创伤性,通过调节光照的范围和强度可实现精准时空调控,是优选的外源性刺激因子。目前已有光控四嗪生物正交反应见诸报道(J. Am. Chem. Soc., 2016, 138, 5978; Angew. Chem. Int. Ed., 2019, 58, 15876; J. Am. Chem. Soc., 2022, 144, 1647),但这些反应需要外源性催化剂或者紫外光照,限制了其在生物活体内的应用范围。
近日,美国加州大学圣地亚哥分校Neal Devaraj教授实验室在光调控的生物正交化学反应研究上取得了重要进展。以此前对于二氢四嗪/四嗪氧化还原反应的研究(J. Am. Chem. Soc., 2015, 137, 8876)为基础,创新性地用光笼(photocage)基团修饰二氢四嗪,合成种类多样的光笼二氢四嗪化合物(四嗪前体)。这种光笼四嗪前体在可见光照射下可脱笼,然后被空气中氧气氧化成四嗪,进而和亲二烯烃进行传统四嗪生物正交反应(图1)。该策略实现了对四嗪正交反应的高精度时空调控,作者利用这种可见光启动的四嗪在活细胞内精准调控生物活性分子,实现靶向标记、改造和递送目标生物分子。作者相信,这种光启动的四嗪化学以及由此启发的其他精准生物正交化学未来应用前景可期。相关成果近日发表在Nature Chemistry 上,第一作者为刘陆平博士(现为北京协和医学院药物所研究员、天然药物活性物质与功能国家重点实验室课题组长)。
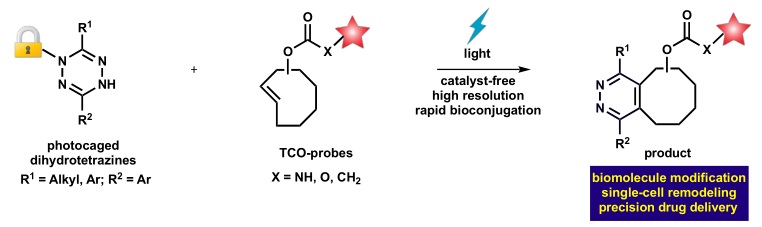
图1. 光启动的四嗪生物正交反应。图片来源:Nat. Chem.
光笼二氢四嗪的合成
作者首先探索和优化了光笼二氢四嗪的合成路线(图2a)。通过使用四川大学吴昊星课题组发展的谷胱甘肽有机催化的四嗪化合物合成方法(Angew. Chem. Int. Ed., 2019, 58, 1106, 点击阅读详细),作者获得了标准底物不对称四嗪化合物2a。然后,通过二氧化硫脲还原得到的二氢四嗪,用光保护基团1-(2-硝基苯基)乙基氨基甲酸酯基修饰后,最终以65%的收率获得期望的光笼二氢四嗪1a。作者紧接着探索了光启动下从光笼二氢四嗪1a原位生成四嗪化合物2a。如图2b所示,405 nm 发光二极管(LED)光照2分钟后,94%的1a光笼基团可以脱除,并以74%的收率获得了2a。实验研究结果表明,这种光启动的原位合成生物正交四嗪基团,并没经过稳定的二氢四嗪中间体。基于前人的研究,作者假设了一个带负电的活泼中间体(图2b)。
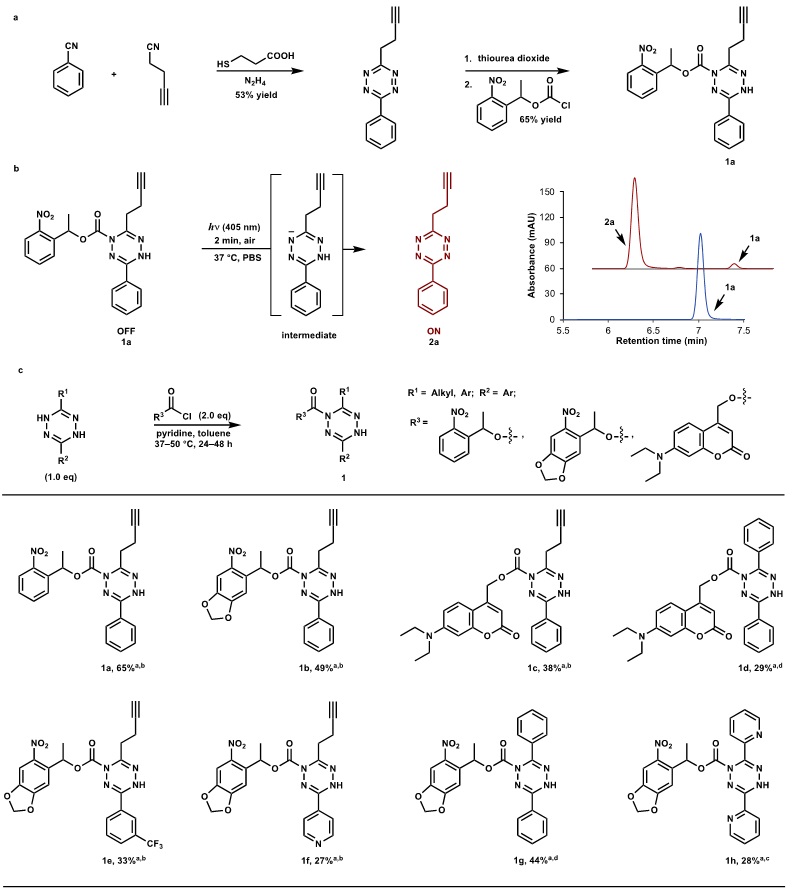
图2. 光笼二氢四嗪合成和底物范围研究。图片来源:Nat. Chem.
在最优条件下,作者对光笼二氢四嗪化合物的底物范围进行了考察。如图2c所示,作者成功地将其他红移的光笼基团例如6-硝基胡椒基(425 nm LED光可脱除)和7-二乙氨基-4-甲基香豆素(450 nm LED光可脱除)用于保护二氢四嗪1a,获得了含有不同光保护基团的四嗪前体(1a-1c)。在特定LED光照条件下,能够以58-74%的收率转化为四嗪2a。同时作者进一步研究了不同基团取代的二氢四嗪,获得了种类多样的光笼二氢四嗪化合物(1d-1h)。值得一提的是,缺电子取代基吡啶也能很好地兼容该反应(1h)。二吡啶基取代的四嗪化合物和反式环辛烯烃的环加成反应非常迅速,反应速率超过106 M-1 s-1。但是二吡啶基取代的四嗪化合物因其固有的缺电子特性,在生物活体内非常不稳定,容易被降解。相比较之下,光笼二氢二吡啶基取代的四嗪1h非常稳定,同时光启动下原位生成含缺电子取代基的四嗪(60%收率),并具有很好的生物相容性。这种原位生成生物正交四嗪基团的策略具有广泛的应用前景。
光启动四嗪的应用展示
为了展示该反应的实用性,作者还进一步合成了光笼二氢四嗪修饰的磷脂,用于标记细胞膜。通过可见光启动的光笼二氢四嗪-磷脂与反式环辛烯烃-荧光分子之间的生物正交反应,实现了选择性单个活细胞高分辨成像(图3)。该光启动的四嗪正交反应为膜蛋白分子、脂类等生物分子的标记和示踪等研究提供了新方法。
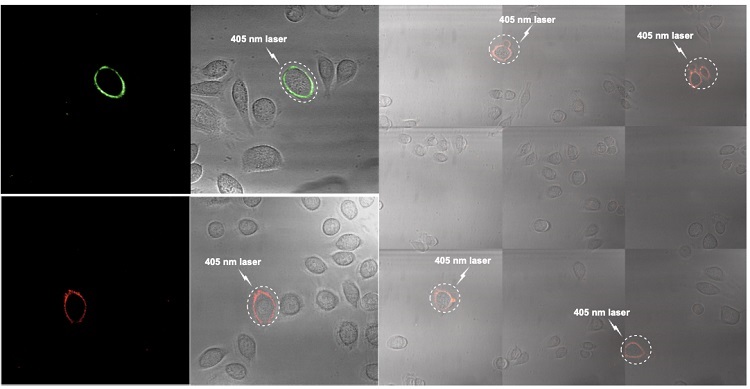
图3. 选择性单细胞高分辨成像。图片来源:Nat. Chem.
2020年,美国生物技术公司Shasqi进行了四嗪和反式环辛烯烃修饰的抗癌药物前体之间“点击−释放(click to release)”药物疗法的1期临床试验,这也是首次在患者体内进行生物正交化学反应,具有里程碑意义。在本研究中,作者利用可见光启动光笼二氢四嗪(1c)和反式环辛烯烃修饰的抗癌药物多柔比星(doxorubicin, Dox)前体(3c)之间的点击−释放正交反应用于递送药物,实现光控抗癌药物的释放(图4a)。这种点击−释放光动力疗法可选择性地杀死癌细胞(图4b),使癌症药物治疗更加安全有效,同时也为其他药物前体的精准递送提供了新途径。
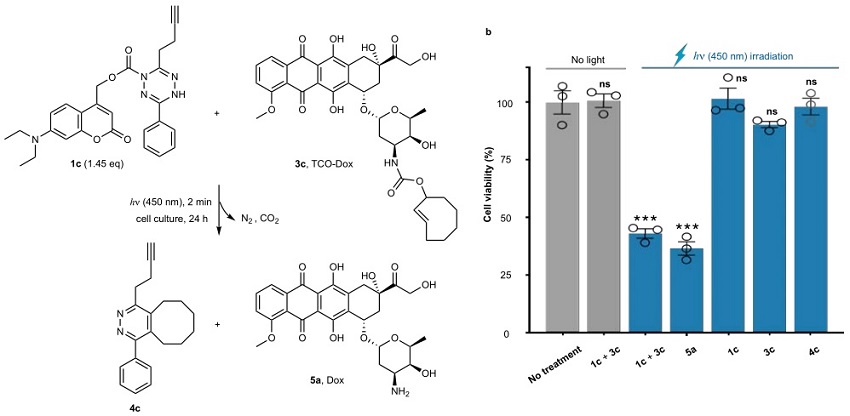
图4. 光控药物释放。图片来源:Nat. Chem.
小结
Neal Devaraj教授团队通过巧妙设计,合成了种类多样的光笼二氢四嗪化合物,在可见光照射下这些化合物可原位激活生成四嗪,从而实现对四嗪正交反应的高精度时空调控。光笼二氢四嗪化合物和光照均对活细胞没有明显毒性,生物相容性好,可以在活细胞内精准调控生物活性分子,实现靶向标记、改造和药物递送。可以预见,这种光启动的精准四嗪生物正交化学策略在生命科学与医学的多个领域都有广阔的应用空间。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Light-activated tetrazines enable precision live-cell bioorthogonal chemistry
Luping Liu, Dongyang Zhang, Mai Johnson, Neal K. Devaraj
Nat. Chem., 2022, DOI: 10.1038/s41557-022-00963-8
作者简介
刘陆平博士:2022.05至今北京协和医学院 药物所 研究员;2018.01–2022.04 美国加州大学圣地亚哥 化学生物学专业 博士后(导师:Neal Devaraj教授);2013.08–2017.10 德国马克斯–普朗克煤炭研究所 有机化学专业 博士(导师:Benjamin List 教授 );2010.09–2013.06 兰州大学 生物化学与分子生物学专业 硕士(导师:王锐 教授);以第一作者在Nature Chemistry,J. Am. Chem. Soc. 等国际知名刊物上发表论文。刘陆平课题组研究方向:1. 生物药物和分子探针的研发;2. 新型生物正交化学的开发和应用;3. 生物相容性催化化学。
刘陆平课题组得到北京协和医学院、中国医学科学院药物研究所、天然药物活性物质与功能国家重点实验室等大力支持,常年招收事业单位编制职工、博士后、科研助理,欢迎热爱科研的有志青年加入!有意者请联系刘老师(lpliu@imm.ac.cn)。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!









































 京公网安备 11010802027423号
京公网安备 11010802027423号