配体促进的碳硼烷亲核取代及重排反应
碳硼烷是一类由碳、硼和氢原子组成的多面体,具有3D芳香性。其独特三维立体结构使其在药物、配体设计和功能材料等领域有广泛应用。例如作为癌症化疗的硼中子捕获试剂,在金属有机领域作为多功能配体,及在有机光电功能材料中作为功能砌块。近年来,碳硼烷的选择性官能团化己成为该领域的研究热点之一。
碳硼烷-氨基酸或-核苷衍生物可以作为硼中子捕获治疗的候选化疗药物,或作为配体用于过渡金属催化。然而,通过B-H活化策略合成B-胺基化碳硼烷的方法仍非常局限。目前已知的途径包括羧基导向过渡金属催化的B(4)-H胺基化及酰胺基化(图1a),氨气作为氮源、Ir-催化的B(3)-H胺基化反应(图1b),以及最近陈学年教授团队报道的Pd-催化的B(9)-H胺基化反应(图1c)。
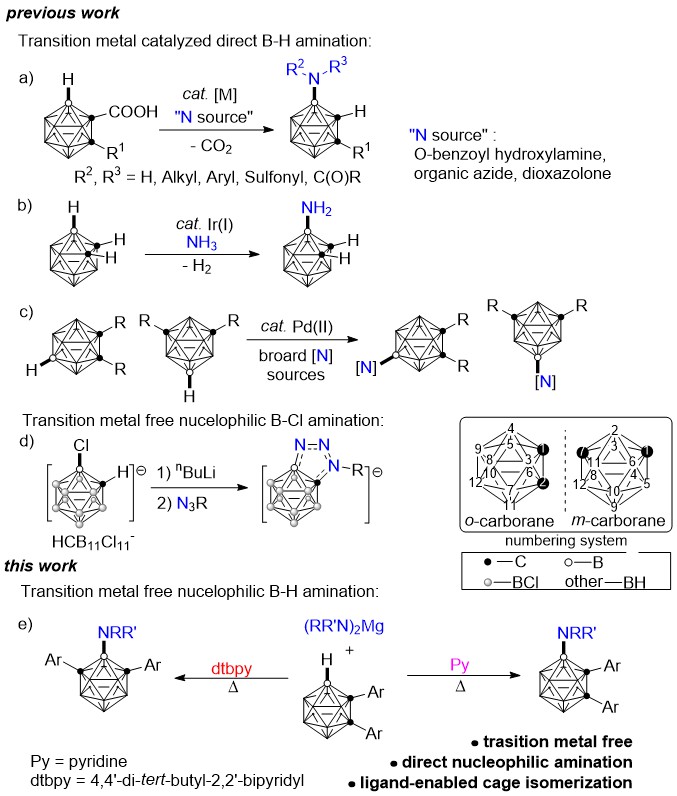
图1. 碳硼烷B-胺基化
作为苯的3D类似物,碳硼烷B-H易发生亲电取代反应,并且遵循以下反应顺序:B(9,12)-H > B(8,10)-H > B(4,5,7,11)-H >> B(3,6)-H。然而,苯和碳硼烷的亲核芳香取代反应并不常见。近期,香港中文大学谢作伟院士团队发现格氏试剂可以与碳硼烷发生亲核取代反应,实现不同硼位点的选择性烷基化及芳基化(Angew. Chem. Int. Ed. 2017, 56, 8642−8646; J. Am. Chem. Soc. 2018, 140, 16423−16427)。此外,[HCB11Cl11]−中的B-Cl键也可通过分子内亲核取代反应来构筑B-N键。近日,谢作伟院士团队报道了无过渡金属参与、吡啶类配体促进的1,2-二芳基-邻-碳硼烷与二胺基镁的直接芳香亲核取代反应,区域专一性地高效合成了一系列B(4)-胺基化邻-碳硼烷衍生物。值得一提的是,大位阻的双齿联吡啶配体(dtbpy)促使碳硼烷笼在温和条件下发生重排,生成B(2)-胺基化间-碳硼烷衍生物。相关成果发表在Angewandte Chemie International Edition 上(图1e)。
在最优条件下,作者对1,2-二芳基-邻-碳硼烷和二胺基镁的适用范围进行了考察。实验结果未显示出明显的电子效应,不同的吸电子和给电子取代基都能兼容。然而,位阻效应却很明显,较小位阻的二胺基镁将会降低反应选择性。
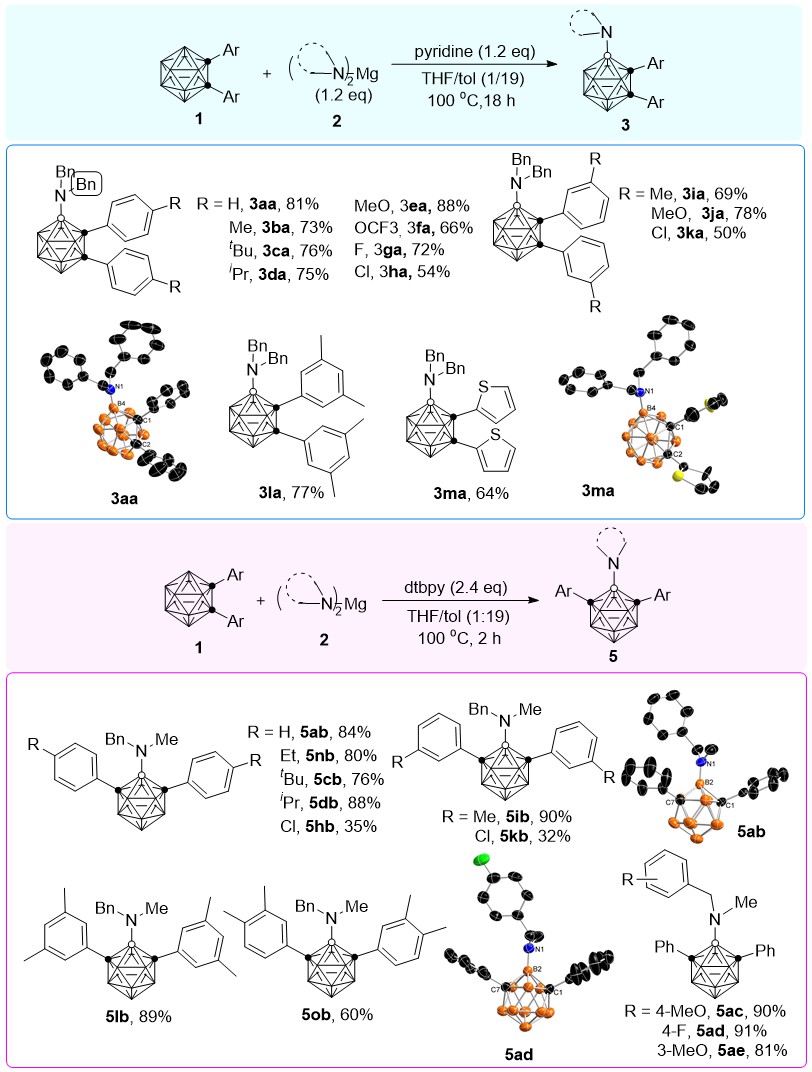
图2. B-胺基-邻/间-碳硼烷的合成
作者对亲核取代反应的具体过程进行了DFT计算。结果表明,反应经过了分步的B-N键形成/B-H键断裂的过程,其中Mg-H键形成/笼子闭合过程是决速步骤。
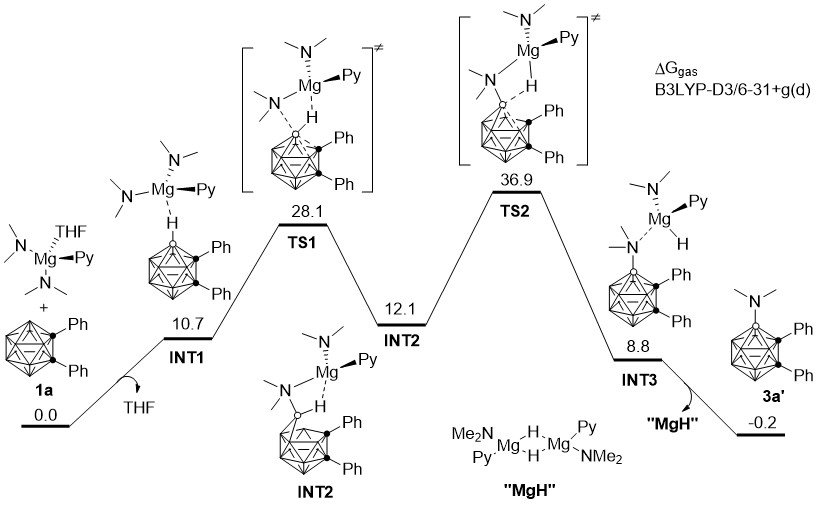
图3. B(4)-H亲核反应过程能量图
为了探究重排反应的机理,作者进行了对照实验。结果表明,镁络合物、双齿配体(dtbpy)和反应温度在笼子异构化过程中均至关重要。根据文献报道及本文实验结果,作者推测重排经过了三角形面旋转(TFR)的异构化过程。
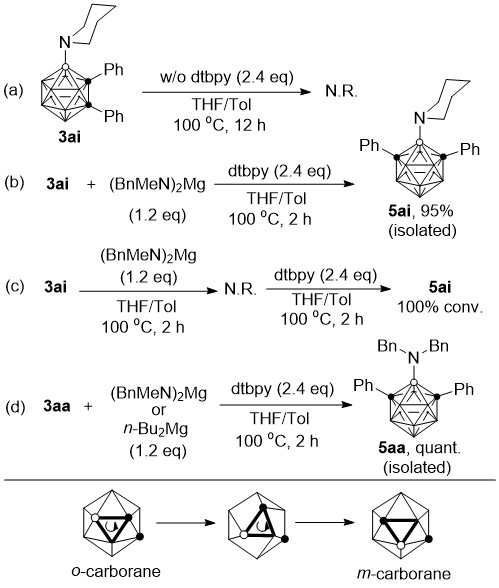
图4. 控制实验及可能的重排机理
碳硼烷笼硼的直接亲核胺化反应,为邻、间-碳硼烷的选择性胺化提供了一种新的方法,拓展了亲核反应策略在碳硼烷官能化领域的应用范畴。
这一成果近期发表在Angewandte Chemie International Edition。文章的第一作者是香港中文大学研究助理教授张洁。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

N-Ligand-Enabled Aromatic Nucleophilic Amination of 1,2-Diaryl-o-Carboranes with (R2N)2Mg for Selective Synthesis of 4-R2N-o-Carboranes and 2-R2N-m-Carboranes
Jie Zhang, Zuowei Xie
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202202675
谢作伟课题组主页:
http://www.cuhk.edu.hk/research/xie_lab/
https://www.x-mol.com/groups/zwxie
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!






















































 京公网安备 11010802027423号
京公网安备 11010802027423号