“不走寻常路”,PNAS报道三维索烃合成的动力学控制
自1828年德国化学家弗里德里希•维勒(Friedrich Wöhler)首次人工合成尿素的近200年以来,有机化学家们开发了大量的合成方法学用以构筑结构复杂的新分子,这些分子的构建一般仅涉及共价键的生成和断裂。与仅由共价键组成的经典分子不同,机械互锁分子(Mechanically Interlocked Molecules, MIMs)是一类近几十年里新兴的分子,其结构特征是两个及以上分子部件通过机械键(Mechanical Bond)连接。由于MIMs的分子部件之间能够发生相对运动,因而这类分子被广泛地用于设计和制造人工分子机器,并在材料学、分子电子学等多个学科显现出重要的应用前景。
在各类MIMs中,索烃(Catenane)吸引了众多超分子化学家的研究兴趣。虽然早在上世纪60年代就有人工合成索烃的报道,但受限于当时合成策略的低效率,索烃的相关研究一直进展缓慢。直到1983年,法国科学家Jean-Pierre Sauvage教授创造性地使用过渡金属离子作为模板,第一次实现了索烃的高效制备,随后J. Fraser Stoddart教授(亦是本文通讯作者之一)发展了以供体-受体作用为模板合成索烃的新策略,极大拓展了MIMs的多样性和功能性。Sauvage和Stoddart教授的突破性工作使索烃等MIMs的研究得到复兴,并推动了人工分子机器的设计和合成等开创性研究,两位教授也因此与Bernard L. Feringa一起获得了2016年的诺贝尔化学奖。
常见的索烃分子通常由多个在拓扑上为二维的大环构成,能够方便地大量制备。然而,当索烃的分子部件变为在拓扑上是三维的分子笼时,其合成则变得较为困难。这是因为三维索烃形成过程中,随着反应位点增多,很容易发生连接点间的错配。在过去的二十多年里,人们探索出了利用过渡金属-配体间的配位化学和动态共价化学(Dynamic Covalent Chemistry, DCC)的两类合成三维索烃的方法,这两类方法所依赖的可逆成键反应赋予了反应过程强大的“自我检查”和“自我纠错”能力,从而得到热力学上最稳定的产物(图1,蓝线所示反应路径)。虽然理论上,通过动力学控制可以得到非热力学最稳定的三维索烃(图1,红线所示反应路径),但相关研究几乎是一片空白。
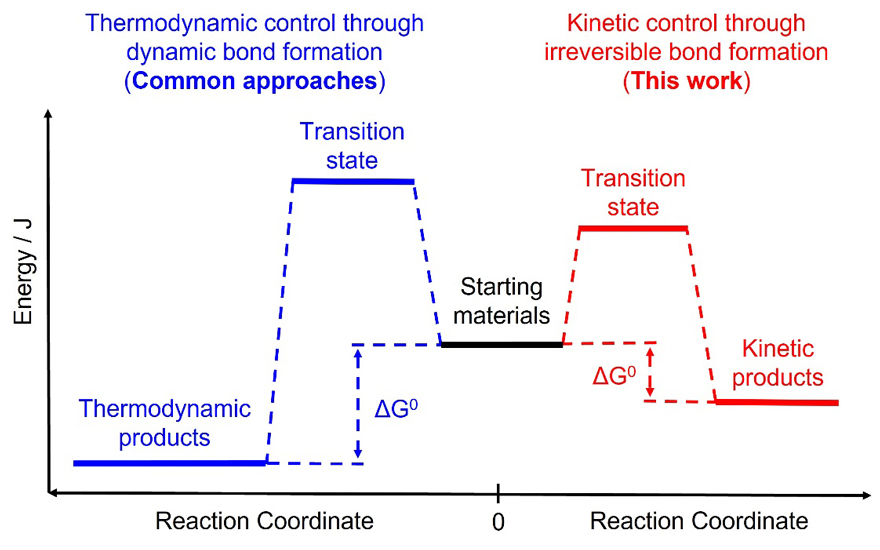
图1. 热力学(蓝色)和动力学(红色)控制下合成三维索烃的反应路径及能量分布图。图片来源:Stoddart课题组
近日,美国西北大学J. Fraser Stoddart课题组与浙江大学郭庆辉课题组、李昊课题组以及美国西北大学Michael R. Wasielewski课题组合作,使用不可逆的成键反应,首次在动力学控制下实现了非热力学最稳定三维索烃的合成,为该类分子的合成提供了新思路。
作者首先设计合成了两个含三芳基均三嗪的底物,即TPPT和TBPT(图2),由于三芳基均三嗪可以采取近乎平面的构象,有利于通过形成分子间的[π•••π]相互作用而实现三维索烃的构建。通过大量的条件筛选,作者发现使用TBAI作为催化剂,在极性溶剂乙腈中可以分别以23%和13%的收率得到两个三维索烃26+和36+。除此之外,还以41%的分离收率得到分子笼13+。然而,在所有筛选的条件下,均未得到正电荷相距最远的三维索烃46+(26+、36+和46+三种索烃为同分异构体,结构差别在于六个正电荷分布的相对位置)。
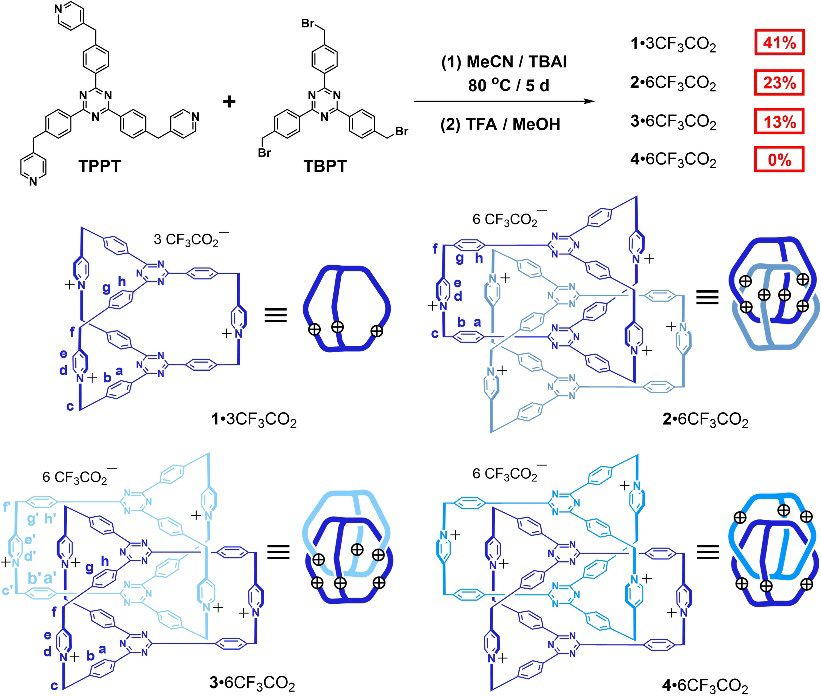
图2. 三维索烃26+和36+的合成。图片来源:Proc. Natl. Acad. Sci. USA
接下来,作者使用多种技术手段对三维索烃26+和36+的结构进行了表征。X射线晶体结构(图3)表明,26+和36+为一对异构体,均由两个相同的分子笼构成。其中三维索烃26+的正电荷相距很近,全部指向分子内侧;而三维索烃36+的正电荷相距稍远,其中一部分正电荷指向分子内侧,另一部分则指向分子外侧。由于相邻更近的正电荷间存在更强的库仑斥力,26+的内平面间距(3.5 Å)略大于36+的内平面间距(3.4 Å)。
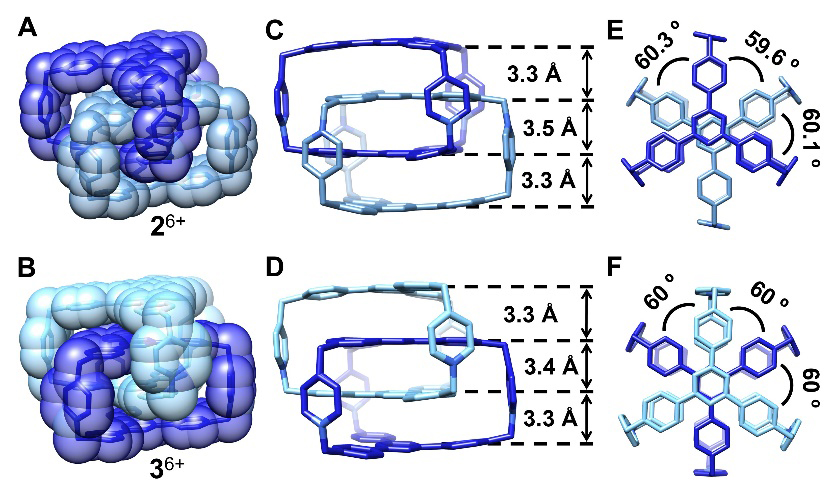
图3. 三维索烃26+和36+的单晶结构。图片来源:Proc. Natl. Acad. Sci. USA
然而,随后的密度泛函理论(DFT)计算结果显示,分离得到的三维索烃26+和36+均不是热力学最稳定的产物,未分离得到的三维索烃46+具有最低的相对能量,这与热力学控制下三维索烃合成中的产物分布截然不同。为了阐明这一反常现象背后蕴含的机理,作者假定:反应首先生成单个的分子笼13+,由于13+具有高度为7.0 Å的空腔,因而在高温下以[π•••π]相互作用作为驱动力允许底物TBPT进入其空腔,形成反应中间体[Suit[3]ane•TBPT]3+,随后TPPT从中间体的底部或者顶部接近,最终生成26+和36+(图4,实线所示反应路径)。另一方面,由于TPPT的尺寸比TBPT更大,位阻效应使得TPPT无法进入13+的空腔,导致中间体[Suit[3]ane•TPPT]3+难以生成,因而无法得到三维索烃46+(图4,虚线所示反应路径)。
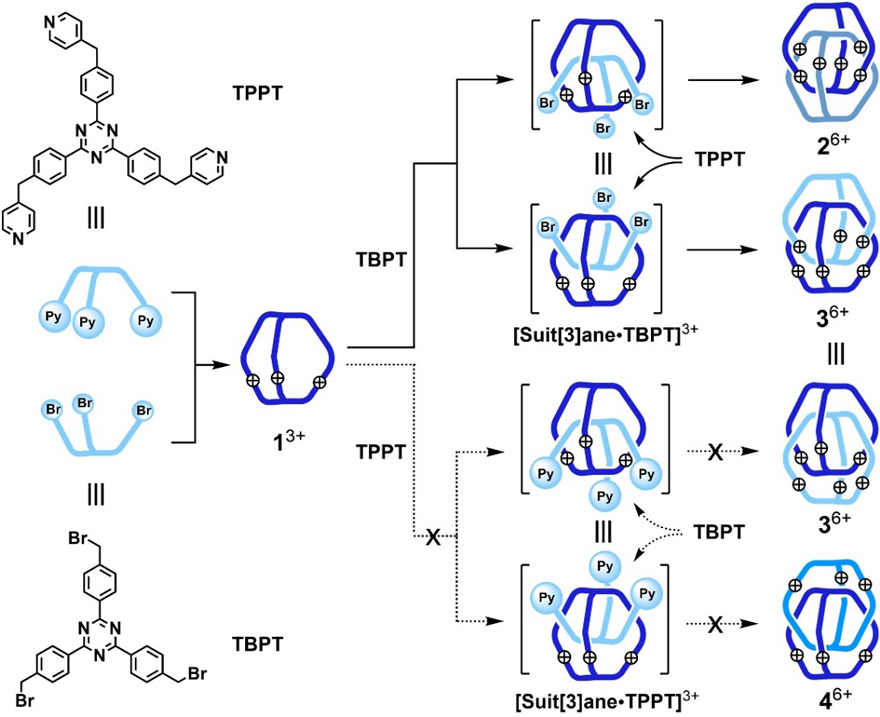
图4. 假定的反应机理。图片来源:Proc. Natl. Acad. Sci. USA
为了证明假定的反应机理,作者首先尝试对反应中间体[Suit[3]ane•TBPT]3+进行分离(图5A)。分子笼13+和底物TBPT混合后高温搅拌,粗产物经反相柱层析分离,高分辨质谱(HRMS)分析确认了中间体[Suit[3]ane•TBPT]3+的存在。然而,由于该中间体在室温下即可快速水解,因而其化学结构无法通过核磁共振(NMR)波谱学等技术手段进一步确认。随后,作者对活性中间体进行了捕获实验(图5B)。高活性且易水解的[Suit[3]ane•TBPT]3+与吡啶反应后,转变为一个稳定的衍生物[Suit[3]ane•TPyPT]6+,其化学结构可以通过NMR以及HRMS得到确认。这些实验结果均有力地支持了假定的反应机理。
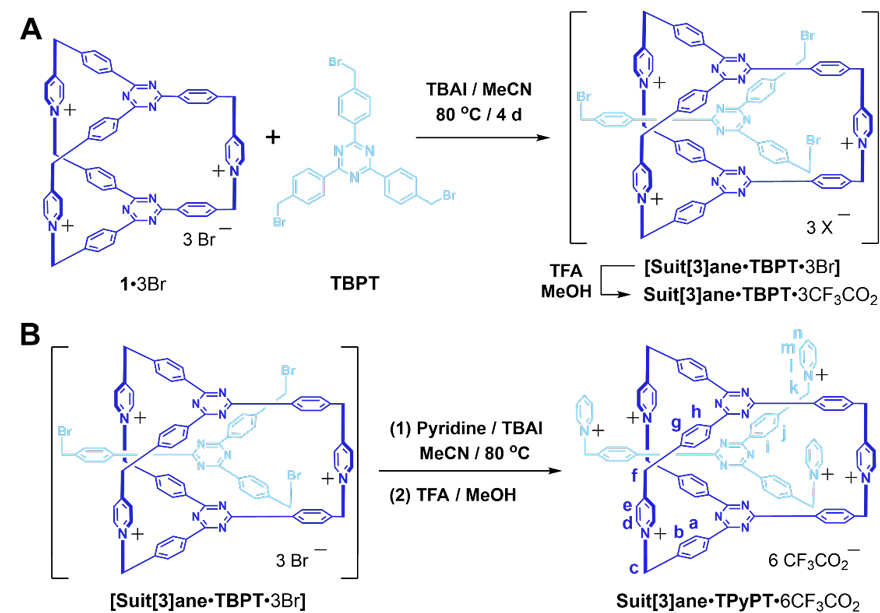
图5. 中间体的分离及捕获。图片来源:Proc. Natl. Acad. Sci. USA
总的来说,这项工作通过精巧的底物设计,利用中间体生成过程中基于尺寸差异的超分子识别作用,专一地形成一种套烷(Suitane)中间体,进而实现了基于不可逆成键反应合成三维索烃的动力学控制,突破了以往利用动态成键策略制备三维索烃的思维限制。相关工作以Research Article形式发表在Proceedings of the National Academy of Sciences of the United States of America(PNAS)上。浙江大学郭庆辉研究员和美国西北大学J. Fraser Stoddart教授为该文章的共同通讯作者,美国西北大学博士后吴勇博士为该文章的第一作者。该研究得到了美国西北大学、浙江大学杭州国际科创中心、浙江大学上海高等研究院繁星科学基金和国家基金委的资助与支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Syntheses of three-dimensional catenanes under kinetic control
Yong Wu, Qing-Hui Guo*, Yunyan Qiu, Jacob A. Weber, Laura Bancroft, Yang Jiao, Hongliang Chen, Bo Song, Wenqi Liu, Yuanning Feng, Xingang Zhao, Xuesong Li, Long Zhang, Xiao-Yang Chen, Hao Li, Michael R. Wasielewski, J. Fraser Stoddart*
Proc. Natl. Acad. Sci. USA, 2022, 119, e2118573119, DOI: 10.1073/pnas.2118573119
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!






























 京公网安备 11010802027423号
京公网安备 11010802027423号