有机氟化学家Tobias Ritter教授与他的Nature、Nature Chem.
今天的主人公是一位青年才俊——德国马克斯普朗克煤炭研究所的Tobias Ritter教授(点击查看介绍)。Tobias Ritter教授1975年出生于德国,1999年硕士毕业于布伦瑞克工业大学,期间在美国斯坦福大学Barry M. Trost教授实验室待了一年并完成硕士论文;2004年博士毕业于瑞士苏黎世联邦理工学院(ETH Zürich),师从Erick M. Carreira教授;毕业后在加州理工学院从事了两年博士后工作,师从Robert H. Grubbs教授。2006年,Ritter进入哈佛大学成为一名助理教授,随后逐步升为副教授和教授。2015年,Ritter进入德国马克斯普朗克煤炭研究所,任职有机合成教授。
Tobias Ritter教授在有机化学领域尤其有机氟化学领域做出了卓越的成果,发表了一系列顶级的论文。他的课题组致力于开发新颖的化学反应,在有机合成、金属有机化学、复杂分子合成及机理的研究等领域做出了大量的贡献。下面笔者和大家聊聊Tobias Ritter教授发表在Nature 及Nature Chemistry 上的论文、评论和综述。

Tobias Ritter教授。图片来源:Max-Planck-Institut für Kohlenforschung
2009年,Ritter教授首次报道[1] 了钯催化7,8-苯并喹啉导向的C-H键活化反应,钯催化剂经由Pd(III)物种,反应中生成Pd-Pd双核络合物中间体(图1)。该发现改变了人们对钯催化C-H键活化反应机理的认识,也为双核钯催化剂的研究提供了思路。
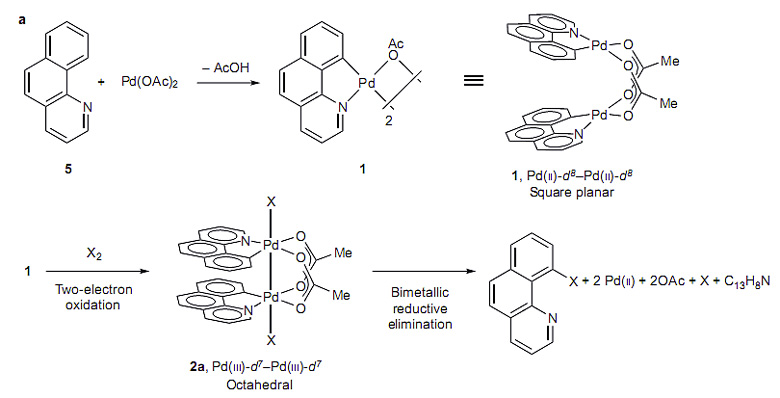
图1. C-H键活化反应经由双核钯中间体的机理。图片来源:Nature Chem.
2010年,Ritter教授在Nature 期刊[2] 对Cho等在Science 期刊[3] 的工作进行了评论。传统向芳香环中引入三氟甲基的方法大多反应条件非常苛刻,局限性大,使其发展受到了很大的阻碍。Cho等人发展了一种简便普适的钯催化氯代芳香烃三氟甲基化反应的方法,具有非常好的底物适用性,该方法在复杂分子的修饰应用中具有广阔的前景。Cho等人找到反应的平衡点,寻找出合适的反应条件使活性钯中间体兼具良好的反应活性与稳定性(图2)。

图2. 钯催化氯代芳香烃三氟甲基化反应的机理。图片来源:Nature
2011年,Ritter教授等人在Nature 期刊[4] 对有机氟化学领域的一些重大突破进展进行了综述评论。对导向基团引导的C-H键氟化反应、钯催化的芳基三氟甲磺酸酯的氟化反应、银催化的有机锡试剂的氟化反应、铜或钯催化的卤代芳香烃的三氟甲基化反应、羰基α位的不对称氟化及三氟甲基化等反应进行了总结和展望。
同年,Ritter教授课题组在Nature Chemistry [5]首次报道了1D钯金属线,在溶液中由于存在金属-金属相互作用的缘故,其长度可达750 nm。研究表明可通过改变配体分子使钯膜具有不同的导电性能,该研究有助于深入了解如何通过改变配体分子的结构来控制金属线的导电性能这一基本问题。
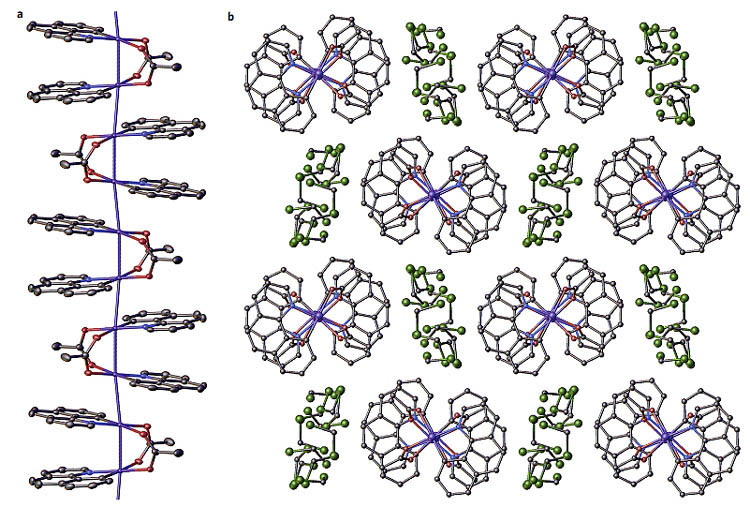
图3. Pd(III)金属丝的X-射线单晶衍射。图片来源:Nature Chem.
2016年,Ritter教授将以往报道的酚类底物的氟化反应进一步拓展为合成18F标记的氟代芳香烃。该方法通过酚类底物与PhenoFluor反应生成氟化产物。反应机理与经典的亲核取代不同,对于传统的亲核取代反应,对位有供电子基团取代的芳香环无法发生亲核取代反应(图4c)。而对于该氟化反应,对甲氧基苯酚反应性良好,氟化产物的产率高达82%。他们推测反应经由以下过渡态(图4a)。该氟化策略可用于将酚类底物转化成18F标记的底物,用作PET技术的探针。该工作发表于Nature[6]期刊(点击阅读详细)。
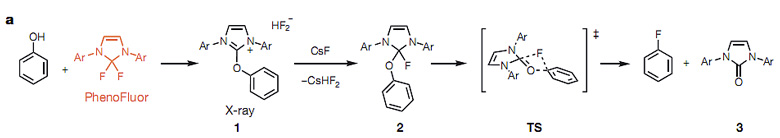
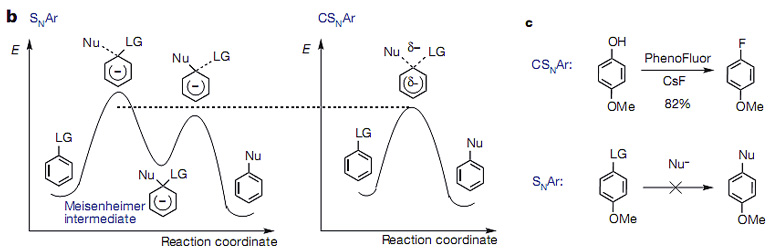
图4. 酚羟基的氟化策略。图片来源:Nature
同年,Ritter教授在Nature Chemistry [7]报道了电荷转移导向的氟代芳香烃对位C-H键的选择性取代反应。传统芳香环的取代反应具有较好邻位选择性或间位选择性,但是缺乏普适的策略用于对位选择性取代反应。作者推测,在自由基转移的状态下,高能自由基会在芳香环上发生自由基的电荷转移,进而导致高区域选择性。随后他们通过实验验证了这一猜想(图5),并开发出Pd-Ru(bipy)3(PF6)2-Selectfluor反应体系用于氟代芳香烃的对位选择性胺化反应(点击阅读详细)。

图5. 电子亲和能与氟代芳香烃对位选择性取代反应的关系。图片来源:Nature Chem.
Tobias Ritter教授还在Nature Chemistry [8] 期刊对Erik Sorensen等人在Angew. Chem. Int. Ed. 的发表的工作[9] 进行了评论,并对相关的氟化反应进行了总结。Erik Sorensen等人报道了新颖的非活化C(sp3)-H键氟化的方法,在铀催化剂的作用下,反应在可见光条件下即可进行(图6)。正如Ritter教授所说,虽然该方法存在很大的底物局限性,却为人们研究非活化C(sp3)-H键官能化开辟了新的局面。
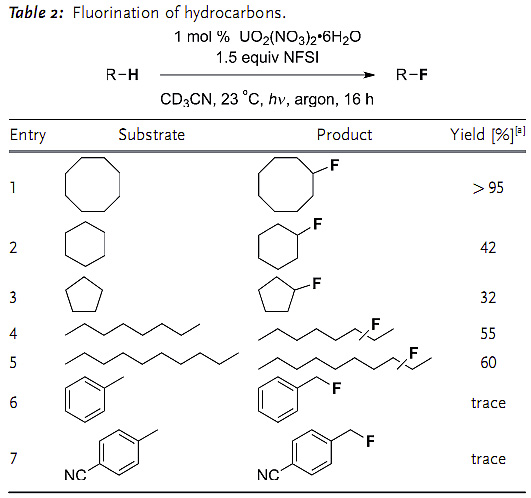
图6. 铀催化的非活化C(sp3)-H键氟化。图片来源:Angew. Chem. Int. Ed.
今年,Ritter教授结合自己过去十年来对18F在PET技术研究的深切体会,在Nature Chemistry [10]对该领域进行了总结和展望(图7)。他指出通过现代有机氟化学来推进PET技术的关键是识别和弥补放射性示踪领域发展存在的缺口,当前缺乏合适的研究基础设施将新方法与放射性示踪剂生产用于临床测试及研究,将18F广泛应用于PET技术还有很长的路要走。
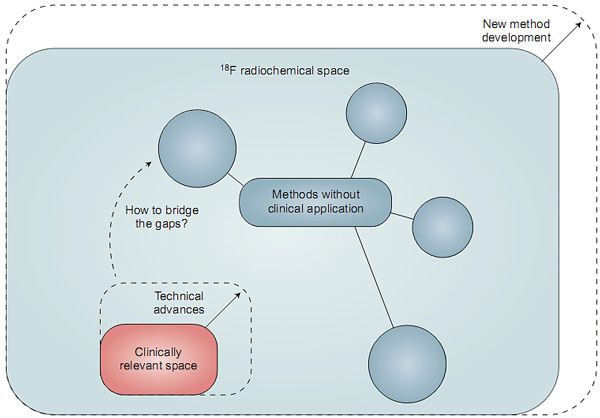
图7. 18F用于PET技术研究的概况图。图片来源:Nature Chem.
参考文献
[1] Nature Chem., 2009, 1, 302-309.
[2] Nature, 2010, 466, 447-448.
[3] Science, 2010, 328, 1679-1681.
[4] Nature, 2011, 473, 470-477.
[5] Nature Chem., 2011, 3, 949-953.
[6] Nature, 2016, 534, 369-373.
[7] Nature Chem., 2016, 8, 810-815.
[8] Nature Chem., 2016, 8, 822-823.
[9] Angew. Chem. Int. Ed., 2016, 55, 8923-8927.
[10] Nature Chem., 2017, 9, 1-3.
Tobias Ritter教授简介
http://www.x-mol.com/university/faculty/1391
在哈佛大学的课题组主页
https://ritterlab.fas.harvard.edu/
在德国马普煤炭研究所的课题组主页
http://www.kofo.mpg.de/en/research/organic-synthesis
(本文由Chem-Stone供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号