笼式模块化多肽-AIEgen探针深度下调PD-L1用于肿瘤免疫治疗
近年来,免疫治疗的兴起为癌症的治疗提供了新的选择。细胞程序性死亡-配体1(PD-L1)/程序性死亡受体1(PD-1)免疫检查点的发现有力地推进了免疫治疗的进展。然而,当前针对PD-L1靶点的阻断策略(比如抗体)常常出现免疫耐受的情况,这可能是由于肿瘤细胞高表达PD-L1所致。为此,中国地质大学(武汉)的娄筱叮教授(点击查看介绍)团队设计了一种基于模块化多肽-AIEgen探针,并与miR-140形成自组装纳米粒子用于深度下调肿瘤细胞的PD-L1表达,从而实现增强的免疫治疗。
作者们首先设计了一种笼式的模块化多肽,它由笼式GO203多肽和组织蛋白酶B(CB)酶响应肽组成。然后通过点击反应将笼式模块化多肽与AIE光敏剂(PyTPA)进行共价连接,从而构建出GCP探针。通过氢键作用力和电荷吸引,GCP与miR-140组装成稳定的纳米粒子GCP/miR-140。GCP/miR-140在进入细胞内部后,在CB酶的解组装下释放出笼式GO203肽和miR-140。接着,笼式GO203肽被肿瘤细胞内高水平的GSH所还原,暴露出活性位点CQC序列,进一步与MUC1蛋白相互作用,下调MUC1的表达水平,进而下调PD-L1蛋白水平。同时,释放出来的miR-140与PD-L1 mRNA相结合,通过降解PD-L1 mRNA,直接下调PD-L1蛋白的表达水平。最后,利用PyTPA的光动力性能杀死肿瘤细胞,并促进TAAs的释放。免疫细胞在识别这些抗原后进一步增殖活化,并趋向肿瘤,从而增强免疫细胞对肿瘤的识别和杀伤。本研究结果证明通过深度下调肿瘤细胞PD-L1表达,将有利于提升免疫治疗的效果,为克服免疫治疗的低应答提供了一种新思路。
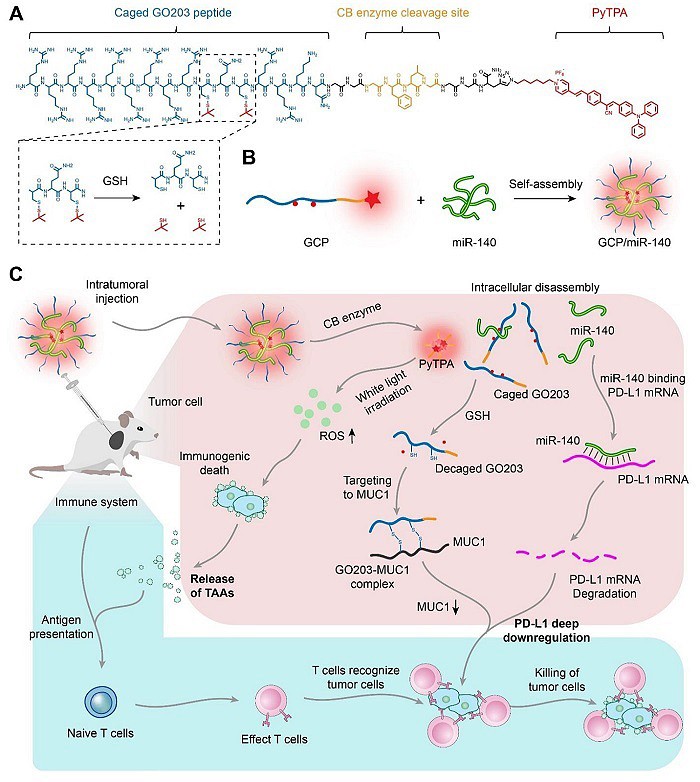
图1. GCP/miR-140的制备与作用机理。图片来源:Angew. Chem. Int. Ed.
这一成果近期以VIP文章发表在Angew. Chem. Int. Ed.上。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Deep Downregulation of PD-L1 by Caged Peptide-Conjugated AIEgen/miR-140 Nanoparticles for Enhanced Immunotherapy
Jun Dai, Jing-Jing Hu, Xiaoqi Dong, Biao Chen, Xiyuan Dong, Rui Liu, Fan Xia, and Xiaoding Lou
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202117798
娄筱叮教授简介

娄筱叮,中国地质大学(武汉)材料与化学学院任教授、博导。2012年在李振教授的指导下获得武汉大学有机化学博士学位。随后进入香港科技大学唐本忠教授团队任助理研究员。2013-2016年就职于华中科技大学化学与化工学院担任讲师、副教授(期间2016.04-2016.10作为访问学者,在加州大学圣塔芭芭拉分校物理系交流)。2017年加入中国地质大学(武汉)。
国家重点研发计划青年项目首席科学家,国家优秀青年科学基金获得者,中组部万人领军青年拔尖人才。现任全国青联委员、中青科协理事。主持包括国家重点研发计划在内的省部级项目10项。围绕复杂生物样本中靶标物质高特异性检测,取得了一系列有特色的学术成果。在SCI收录刊物上发表/接收SCI论文136篇。相关研究成果已被国际知名刊物引用5000余次,H因子为41。获得国家授权发明专利7项,应邀撰写英文学术专著1部,章节2章。
Email:louxiaoding@cug,edu.cn
https://www.x-mol.com/university/faculty/49854
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!






















































 京公网安备 11010802027423号
京公网安备 11010802027423号