Science:油和水为什么不能混合?
油和水不能混合,这算是人人皆知的常识了。就算二者放在一起剧烈摇晃或者搅拌,纯靠人力充其量只能形成不稳定的乳液,静置之后很快就会分离。

油水混合。图片来源于网络
油和水为什么不能混合?这个问题其实涉及到对于疏水性的深入理解。
如果借助超声设备,在输入能量足够的情况下,在水中会形成尺寸小于1微米的油滴,并会持续存在数周乃至数月。这让科学家们很迷惑,在没有任何稳定剂存在的情况下,微小的油滴如何能够相对稳定的存在于水中?
更奇怪的还在后面。早期的实验发现,当置于电场中时,这些微小的油滴会向正极移动。也就是说,水中的油滴表现出负的zeta(ζ)电位,混合中性的油和中性的水居然会产生带负电的油滴 [1-2]。这虽然从一定程度上解释了微小油滴在水中的稳定性,不过,毫不奇怪的是,这些电荷的来源引起了激烈的争论。
这一现象曾被解释为油滴表面吸附了OH–,然而,OH–的吸附并没有得到光谱证实。同时,理论研究也表明,OH–是一种小的、不可极化的离子,倾向于水合而不是吸附在界面处,疏水界面处的OH–更处于热力学极不稳定状态。那么,水中油滴表面为什么会有负电荷?疏水油滴-水的界面,究竟是什么样子?

水分子(包含H+和OH–)模拟。图片来源:Chem. Rev.[1]
近日,瑞士洛桑联邦理工学院(EPFL)Sylvie Roke和意大利国际理论物理中心Ali Hassanali等研究者联合,在Science 杂志上发表论文,他们利用偏振振动和频散射(sum-frequency scattering,SFS)光谱研究了分散在重水(D2O)中的十六烷油滴(~200 nm),实验观测结果与分子动力学模拟相吻合,证实了水分子与烷基氢形成了“不正确”的界面C–H•••O氢键,导致了水至油的电荷转移,揭开了疏水油滴表面负电荷的来源秘密。
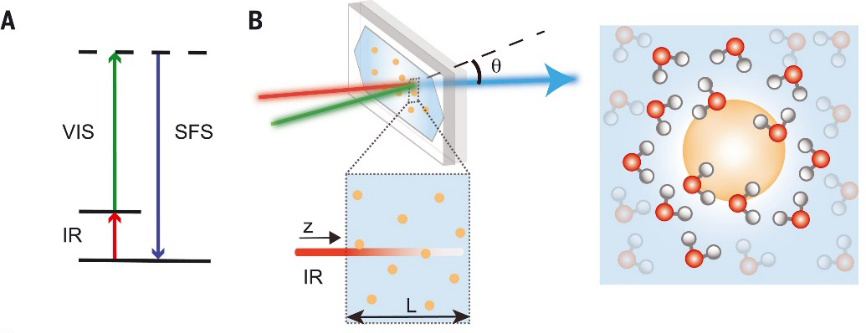
SFS测试及油-水界面示意图。图片来源:Science
研究者比较了空气-水界面和油-水界面的SFS光谱,从光谱强度分析,油-水界面的H键网络比空气-水界面更强。更明显地,空气-水界面的O-D键的振动峰位于2745 cm−1,而油-水界面的峰值红移了~100 cm−1(灰色区域)。研究者推测,如此大的移动,说明了油滴表面的负电荷来自界面处不对称的氢键分布,并可以用电子密度的转移机制来解释。
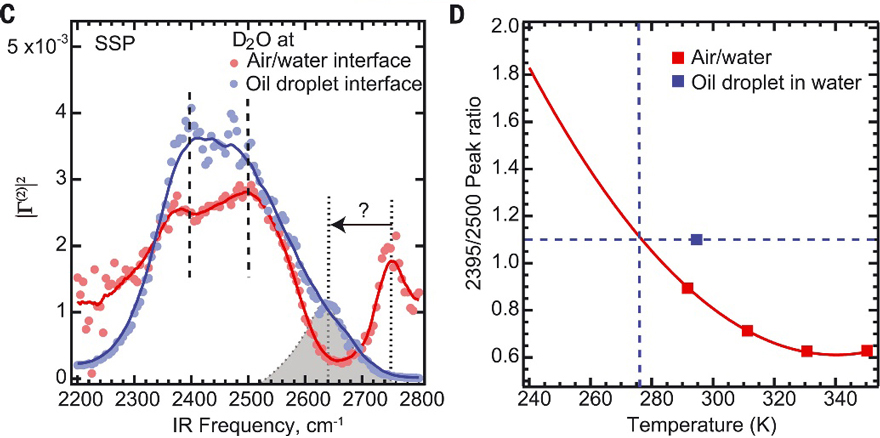
SFS光谱表征。图片来源:Science
一个峰位置的红移,是如何推出这个结论的呢?这要从水分子的对称性说起。水分子具有一个C2旋转轴和两个相互垂直的对称面,属于C2v对称结构,存在C2v对称伸缩振动(C2v-ss),和反对称伸缩振动(C2v-as)。但如果水分子中的两个O–H基团由于氢键或其他相互作用而不对称,则存在C∞v伸缩振动,且测量的相对信号强度取决于分子取向和对称性。
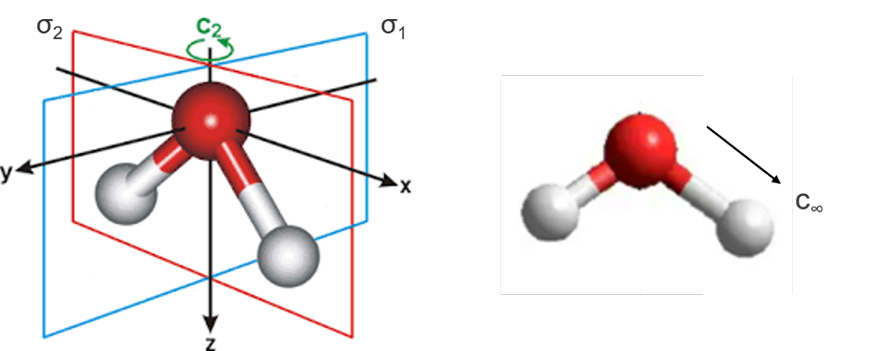
水分子对称性
考虑到所有可能的分子倾角,研究者分析了具有这些不同对称性的界面振动模式。图中的红色、绿色和蓝色区域分别代表了重水中O–D键的C2v-ss振动(约2200~2550 cm−1),C∞v振动(约2550~2745 cm−1)和C2v-as振动(大于2745 cm−1)。因此,油-水界面峰的红移,表明更多的水分子呈现C∞v对称性,两个O–D键处于不同的状态。又因为这些分子位于油-水界面处,电荷只能从水的O–D键转移到十六烷的C–H键,因为后者是接受电子密度的唯一可能。峰的展宽也进一步说明了油和水之间强烈的电荷转移相互作用。对油滴表面SFS光谱分析及计算,也得到了相同的结论。此外,分子动力学模拟与实验结论相吻合。
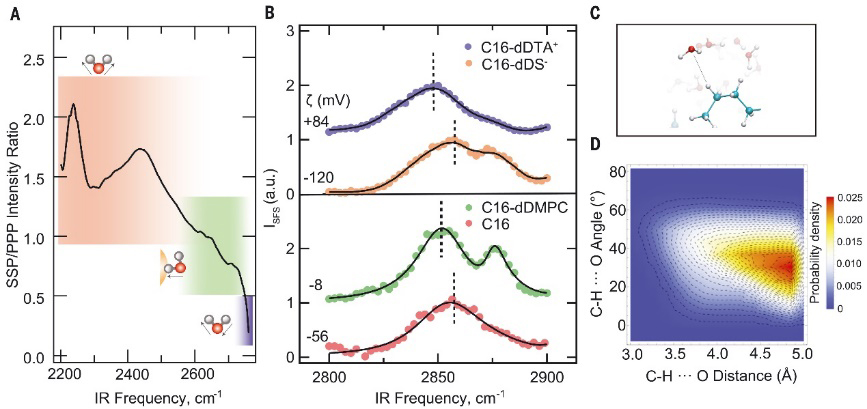
油-水界面C–H•••O氢键分析。图片来源:Science
也就是说,界面C–H•••O氢键导致水分子至十六烷分子的电荷转移,是十六烷油滴表面带负电荷的原因,电荷的存在又为亚微米大小的油滴提供了一定的稳定性。利用这一模型进行模拟计算,两界面表面电荷密度约为-0.015 e nm-2,与电泳实验结论保持一致。
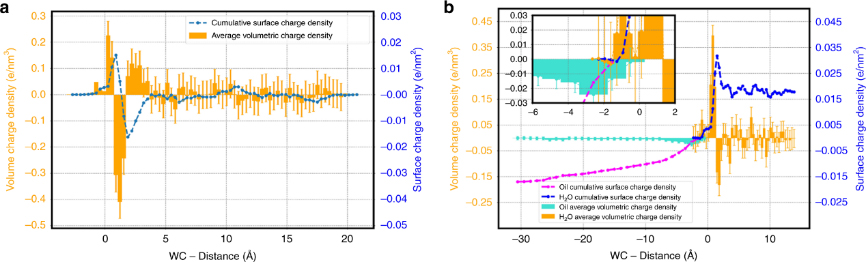
表面电荷密度计算。图片来源:Nat. Commun. [3]
水是我们这个星球上生命体存在的关键分子,是最寻常又最不寻常的液体之一。冰在融化时密度增加,水在压力下粘度降低,如此种种“反常”的性质经常和氢键有关。本文对水中油滴表面负电荷来源的解释,有助于更好地研究微小油滴的稳定性,也有助于我们从根本上去理解常常挂在嘴边的“疏水性”。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Charge transfer across C–H⋅⋅⋅O hydrogen bonds stabilizes oil droplets in water
Saranya Pullanchery, Sergey Kulik, Benjamin Reh, Ali Hassanali, Sylvie Roke
Science, 2021, 374, 1366-1370, DOI: 10.1126/science.abj3007
参考文献:
[1] N. Agmon, et al. Protons and Hydroxide Ions in Aqueous Systems. Chem. Rev. 2016, 116, 13, 7642-7672, DOI: 10.1021/acs.chemrev.5b00736
[2] J. C. Carruthers, The electrophoresis of certain hydrocarbons and their simple derivatives as a function of pH. Trans. Faraday Soc. 1938, 34, 300–307, DOI: 10.1039/TF9383400300
[3] E. Poli, et al. A. Charge transfer as a ubiquitous mechanism in determining the negative charge at hydrophobic interfaces. Nat. Commun. 2020, 11, 901. DOI: 10.1038/s41467-020-14659-5
(本文由小希供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号