2021年Science十大“年度突破”,“AI预测蛋白质结构”居首
日前,Science 公布了该杂志评选出的2021年十大“年度突破(2021 Breakthrough of the Year)”,其中排名首位的是人工智能(AI)在生命科学领域的应用——“Protein structures for all”,即,科学家使用基于AI的软件根据氨基酸序列准确预测了大量蛋白质的三维(3D)结构。

1972年,美国生物化学家Christian Anfinsen因在核糖核酸酶氨基酸序列与生物活性构象之间关系的相关研究中做出的贡献而获得诺贝尔化学奖,他在发表获奖感言中提出了一个愿景,他希望“有一天,能够仅根据氨基酸序列来预测任何蛋白质的 3D 结构”。蛋白质的重要性毋庸置疑,如果能够获得蛋白质的准确3D结构,不仅可以加深对基础生物学的理解,并有希望发现新的药物靶点,帮助开发更有效、更安全的药物。不过,人体内就有数十万种蛋白质,依靠传统的实验方法,比如X-射线晶体学以及新兴的NMR、冷冻电镜(cryo-EM),解析蛋白质3D结构的速度远跟不上实际需要。为了加速这一过程,科学家们在上世纪70年代就开始建立计算机模型,来预测给定氨基酸序列的蛋白质的折叠过程。2018年,谷歌旗下DeepMind公司开发的AI软件预测程序AlphaFold横空出世,将软件预测蛋白质结构推上了一个新的高度。2020年,DeepMind公司推出了下一代的AlphaFold2,该程序表现得更加出色,预测精度已经与实验方法相当。今年,AI预测蛋白质3D结构更是获得突飞猛进的进展。7月,Baker等人的 AI 程序RoseTTAFold 已经预测出了数百种蛋白质的结构,这些蛋白质都属于一类常见的药物靶点(Science, 2021, 373, 871-876)。一周后,DeepMind 的科学家更是利用AI程序预测了人体中发现的35万种蛋白质的结构(Nature, 2021, 596, 590–596)。要知道,这个数量已经占到了所有已知人类蛋白质的 44%。在接下来的几个月里,他们预计他们的数据库将增长到惊人的 1亿蛋白质(来自各种物种),几乎是当前已知总数的一半。科学家们表示,下一步的工作是预测蛋白质如何相互作用,这将是更有挑战性的工作。目前,AlphaFold2和RoseTTAFold的代码都可以公开获取,所有感兴趣的研究者都可参与。最后补充一句,研究SARS-CoV-2的科学家们也正在使用AlphaFold2来模拟奥密克戎毒株刺突蛋白突变的影响。

其他年度突破(“Runners-up”)涉及古DNA、可控核聚变、COVID-19新药、火星研究、粒子物理、基因编辑疗法等多个领域,分别为:
化石中的DNA研究(“Ancient soil DNA”)
可控核聚变的进展(Fusion's day in the Sun?)
可治疗COVID-19的新药问世(“Powerful pills for COVID-19”)
创伤后应激障碍(PTSD)疗法(“A psychedelic PTSD remedy”)
人工抗体治疗多种传染性疾病(“Artificial antibodies tame infectious diseases”)
“洞察号”探测器在火星上的发现(“NASA lander uncovers the Red Planet's core”)
粒子物理学标准模型的新发现(“At last, a crack in particle physics' standard model?”)
基因编辑疗法的新进展(“CRISPR fixes genes inside the body”)
体外培养动物胚胎助力早期发育研究(“Embryo 'husbandry' opens windows into early development”)
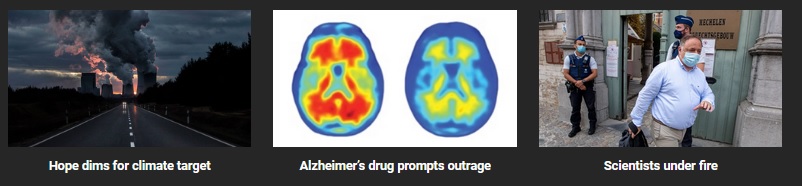
此外,Science 也列出了今年的“年度负面新闻(Breakdown of the year)”:
格拉斯哥气候变化大会让人失望(“Hope dims for climate target”)
美国FDA批准的阿尔茨海默氏症新药引发争议(“Alzheimer's drug prompts outrage”)
COVID-19大流行引发的政治分歧,让公众对科学家表现出前所未有的敌意,包括线上和线下的恐吓、抗议甚至死亡威胁(“Scientists under fire”)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号