中国药科大学孔令义团队JMC:用于治疗BRCA野生型三阴性乳腺癌的PARP/EZH2双靶点抑制剂
孔令义教授(点击查看介绍)课题组一直从事基于天然产物的创新药物研究。前期,该团队对天然产物睡茄内酯类化合物Withangulatin A经过结构修饰改造,通过多轮的构效关系研究,发现了一个通过共价键结合在硫氧还蛋白还原酶(TrxR)的498号硒代半胱氨酸残基的候选化合物(J. Med. Chem., 2020, 63, 11195)。近期,该团队再次在J. Med. Chem.发表了最新研究成果,报道了用于治疗BRCA野生型三阴性乳腺癌的PARP/EZH2双靶点抑制剂。
乳腺癌是世界上最常见的癌症之一,三阴性乳腺癌(Triple-negative breast cancer, TNBC),即雌激素受体(Estrogen Receptors, ERs)、孕激素受体(Progesterone receptors, PRs)和人表皮生长因子受体2蛋白(Human epidermal growth factor receptor 2 protein, HER-2)均为阴性,占所有乳腺癌的12-20%。TNBC预后差,复发率高,生存率低,其病理特点决定了其治疗的复杂性。目前TNBC的治疗方案仅限于高毒性化疗方案。因此,开发治疗TNBC的潜在靶向药物是药物化学家面临的重要挑战之一。一项III期临床试验(NCT020006222)表明PARP抑制剂Olaparib对BRCA突变的晚期乳腺癌包括TNBC具有显著疗效,为TNBC的靶向治疗提供了一种可能,但是仍有80%的BRCA野生型TNBC患者不能从中获益。
该团队通过将PARP和EZH2抑制剂的关键药效团拼接,设计了化合物1。随后通过系列的构效关系研究,进行结构优化,最终得到候选化合物5a。酶水平研究表明化合物5a对PARP-1和EZH2均有较好的抑制活性。对两种野生型BRCA的TBNC细胞MDA-MB-231和MDA-MB-468的细胞活性研究结果表明,化合物5a相对于Olaparib的抑制活性分别提高了约15倍和80倍,甚至优于Olaparib和Tazemetostat/GSK126(EZH2抑制剂)联合用药。
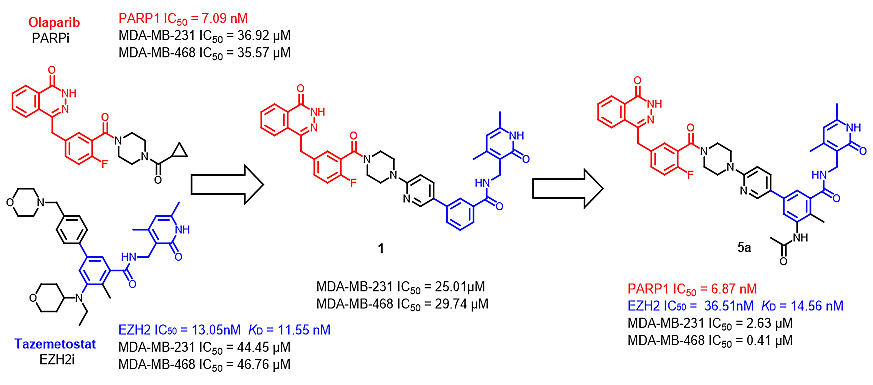
BRCA与PARP为一对合成致死(Synthetic lethality)对,通过引入EZH2抑制剂片段,使PARP抑制剂对BRCA野生型细胞敏感,从而间接达到合成致死效应——当今比较先进的一种治疗癌症的策略和方法,这也是该研究的一个关键的创新。该研究表明, PARP和EZH2双靶点抑制剂有进一步被研发成用于TNBC治疗药物的潜力。

中国药科大学的王成博士为文章的第一作者,孔令义教授和王小兵教授为文章的通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Discovery of First-in-Class Dual PARP and EZH2 Inhibitors for Triple-Negative Breast Cancer with Wild-Type BRCA
Cheng Wang, Lailiang Qu, Shang Li, Fucheng Yin, Limei Ji, Wan Peng, Heng Luo, Dehua Lu, Xingchen Liu, Xinye Chen, Lingyi Kong*, and Xiaobing Wang*
J. Med. Chem., 2021, DOI: 10.1021/acs.jmedchem.1c00567
导师介绍
孔令义
https://www.x-mol.com/university/faculty/210955
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号