应用进化动力学结合病毒学研究,追踪新冠病毒起源和进化特征 | Infectious Diseases of Poverty
标题:Characterization of SARS-CoV-2 worldwide transmission based on evolutionary dynamics and specific viral mutations in the spike protein
期刊:Infectious Diseases of Poverty
DOI:10.1186/s40249-021-00895-4
微信链接:点此阅读微信文章
近日,海军军医大学流行病学教研室曹广文教授课题组在Infectious Diseases of Poverty 上发表研究论文Characterization of SARS-CoV-2 worldwide transmission based on evolutionary dynamics and specific viral mutations in the spike protein。该研究利用进化动力学的理论和方法,证实在全球疫情早期,中国分离的病毒仅由单一基因型构成,并对病毒随后在全球变异和传播的规律进行了描述。
该研究使用GISAID公共数据库中的病毒序列,利用生物信息学方法,客观分析了疫情早期各国SARS-CoV-2的差异。基于病毒序列特征描述其在不同时间和空间的基因型分布是进化动力学的核心内容,通过大规模生物信息学分析和模拟运算,该研究发现,在疫情初期,欧洲和美洲的部分国家分离到的病毒包含多种基因型;而在中国境内发现并分离的病毒为其中的一种(如下图中C组所示)。同时文中总结了一些证明了欧洲、美洲一些国家在武汉疫情之前就已存在SARS-CoV-2的文献报道,结合该研究中的发现,提出SARS-CoV-2从野生动物“溢出”到人类这一过程并非最初发生在中国。
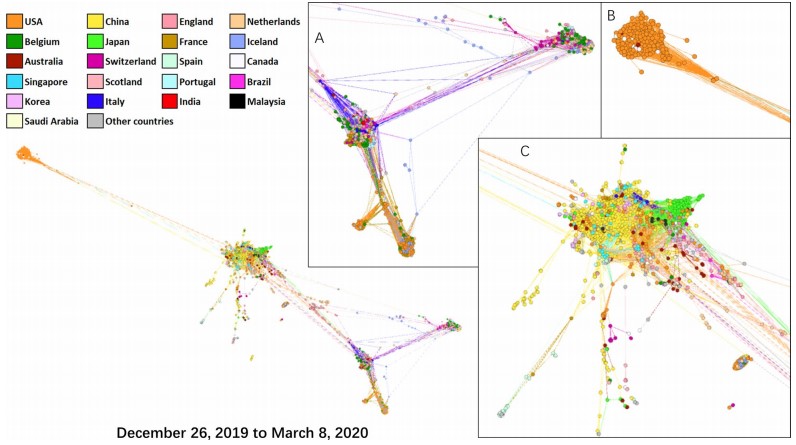
Fig.3 Network graphic of SARS-CoV-2 isolates worldwide during 26 December, 2019 and 8 March, 2020.
研究者基于对自然来源的SARS-CoV-2类似病毒进行重组等分析发现,SARS-CoV-2并非由已知的其他冠状病毒经过大片段的重组而来;SARS-CoV-2与其他冠状病毒的差异平均分布在病毒基因组各个位置。这与自然病毒的进化规律一致,可以支持SARS-CoV-2并非“人造病毒”这一观点。
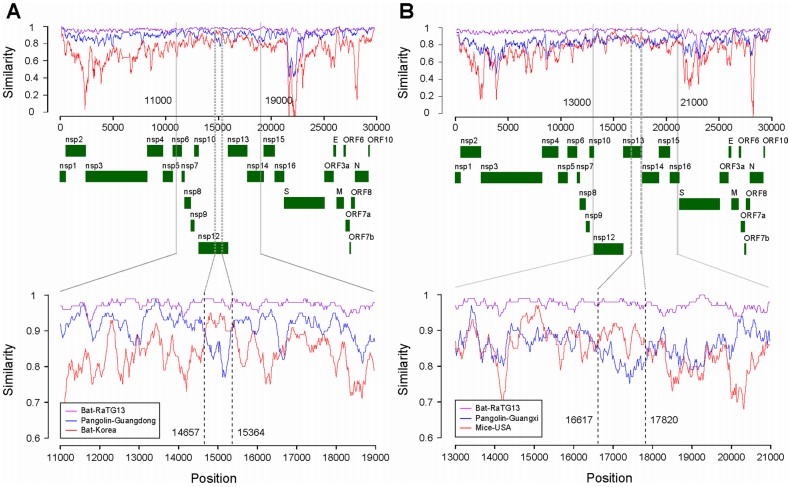
研究还总结了SARS-CoV-2的一些重要突变毒株在全世界各国的流行情况,并验证了变异病毒的刺突蛋白与宿主ACE2(Angiotensin converting enzyme II)受体的亲和力变化。首先通过生物信息学方法预测在棘突蛋白受体结合域(receptor-binding domain, RBD)可能改变病毒与受体结合能力变化的突变,通过数据库查询这些突变在世界各国的分布情况,发现预测的毒株成为了当地的优势毒株。在生物学实验中发现突变的病毒确实可以导致其与受体结合能力的改变,从而可能促进病毒的生存与传播。除了生物信息学分析,通过实验研究进行病毒学验证,也是该研究的亮点之一。
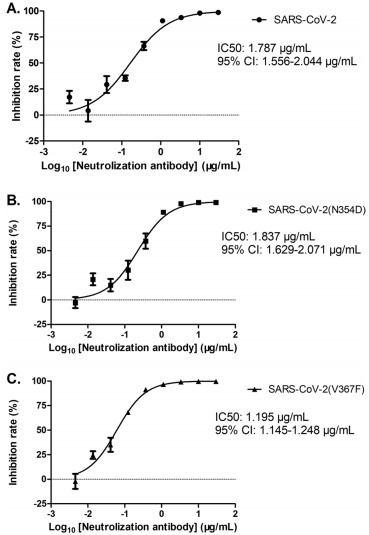
Fig.6 The effect of SARS-CoV-2 spike protein mutations on the reactivity to the neutralizing antibody.
综上,在进化压力下,SARS-CoV-2从自然传播到人类生活环境这一事件可能同时发生在多个国家;相同地理区域内,病毒株的同质化可能是由各国之间的旅行禁令引起;病毒学研究提示,SARS-CoV-2的进化可能通过改变病毒与ACE2受体的结合能力从而影响病毒的传播能力,一些突变还会导致SARS-CoV-2免疫逃逸和病毒复制能力的改变从而影响病毒的致病能力。
Infectious Diseases of Poverty
doi:10.1186/s40249-021-00895-4
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号