具有开壳双自由基特征的稠环芳烃(二)
在上一篇文章中,我们详细讨论了在溶液中合成的基于六元环的双自由基稠环芳烃(点击阅读原文)。本文将着重讨论在溶液中合成的基于非六元环(五、七元环)的双自由基稠环芳烃。众所周知,石墨烯是由sp2碳原子连接而成的六元环网状结构,具有半金属性、零带隙的性质,这使得石墨烯很难被直接应用于电子器件中。缺陷的引入不仅可以打开石墨烯的带隙,而且还能改变其光学、电学以及磁学的性质,这使得人们对具有缺陷的石墨烯(图1)产生了浓厚的兴趣。但是,目前大多数的工作集中于理论模型的计算以及在二维材料中的表征,同时大多数引入的缺陷随机且不可控。因此,合成具有明确缺陷结构的石墨烯片段(稠环芳烃或者纳米石墨烯)并对其进行详细的物理、化学表征有助于我们更好的理解石墨烯中缺陷对其电子性质的影响,从而进一步探索结构与性质之间的关系。不过,正如上一篇文章所介绍的,具有双自由基特征的分子表现出极高的反应活性,极其不稳定,这使得合成具有缺陷结构的双自由基分子充满挑战。本文将带大家回顾过去十几年间一些具有开创性的工作。
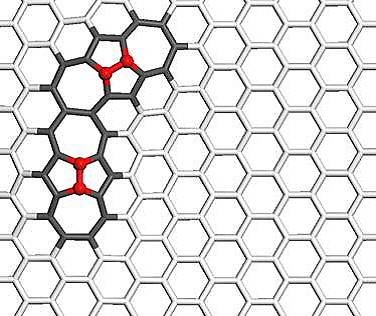
图1. 具有缺陷结构的石墨烯。图片来源:Phys. Rev. B, 2010, 81, 155444
1. 茚并芴体系(Indenofluorenes)
茚并芴体系由于包含非六元环的结构且具有20个π电子,根据休克儿规则,这类分子可被看作是一类独特的反/亲芳香性体系。同时,基于茚与芴两个单元不同的连接方式,如图2所示,该体系具有五个同分异构体(分子1-5)。另外,从它们对应的共振结构来看,每种同分异构体的双自由基结构中都包含3个芳香六隅体。这其中分子1和5获得了两个额外的芳香苯环,而分子2、3、4则都只获得一个,因此根据Clar芳香六隅体规则可以合理地推测分子1和5有较高的双自由基指数(y)同时表现出双自由基的性质特征(如宽的核磁氢谱峰以及电子顺磁共振信号峰等),分子2-4则表现出较低的y值或闭壳结构。
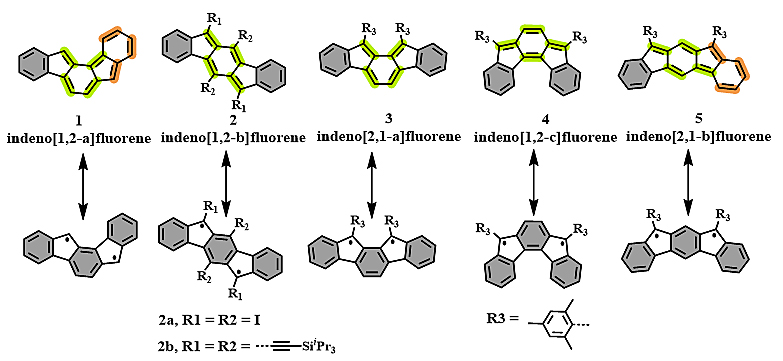
图2. 茚并芴体系的同分异构体以及对应的双自由基共振结构。
根据理论模型计算结果分析,分子1及其衍生物的基态为三线态,从而具有非常高的反应活性,因此至今尚未被报道出来。而对分子2的研究最早开始于1991年,由Klaus Mullen团队在合成梯形共轭聚合物的路线中得到了该分子(Polymer, 1992, 33, 2443)。随后Swager团队通过环炔的分子内环化合成了一种对空气不稳定的分子2a(J. Org. Chem., 1994, 59, 1294),其R1取代基的位置容易被氧化成二酮结构。直到2011年,来自俄勒冈大学的Haley团队通过在R1、R2位置引入大位阻保护基团(三异丙基乙炔基)得到了非常稳定的反芳香性分子2b(Angew. Chem. Int. Ed., 2011, 123, 1159)。茚并芴其他的同分异构体分子3和4分别被来自大阪大学的Tobe团队(Angew. Chem. Int. Ed., 2011, 50, 6906)和Haley团队(Org. Lett., 2013, 15, 1362)制备并分离得到,同样地,大位阻保护基团(均三甲基苯基)的引入增加了这两个反芳香性分子的稳定性。通过实验及理论计算证明,上面三种被成功合成出来的茚并芴同分异构体在基态均显示出闭壳醌式结构。如:晶体结构分析中观察到明显的键长交替的特征,无ESR信号峰以及核磁氢谱无宽峰被观察到等。这也与Clar六隅体规则的初步预测一致。
与上述三种异构体不同的是,分子5的双自由基共振结构中获得了两个额外的芳香六隅体,由此可以推断此分子可能会展现出双自由基的性质特征。2013年,Tobe团队成功合成了分子5(Angew. Chem. Int. Ed., 2013, 52, 6076),通过理论计算得到其自由基指数为0.68,同时作者通过变温核磁氢谱,ESR以及Uv-vis光谱的表征,进一步证明了分子5的基态具有双自由基单线态的特征。如图3所示当温度为30 ℃时,核磁氢谱中无信号峰,这是因为在该温度下分子由单线态激发到了三线态分子,但随着温度的降低,分子又慢慢的从三线态回到了单线态,因此信号峰逐渐又显现了出来。
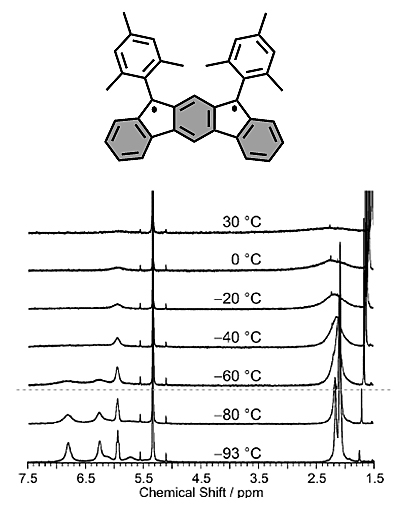
图3. 分子5的变温核磁氢谱。图片来源:Angew. Chem. Int. Ed., 2013, 52, 6076
2. 茚并芴的π扩展体系
如果对茚并芴的核进行π扩展,会对它的光电性质产生怎样的影响,是否会表现出双自由基特征?2012年,Haley团队首先报道了芴并芴体系(fluorenofluorenes)的第一个同分异构体fluoreno[4,3-c]fluorene(5,图4,Org. Lett., 2012, 14, 2426),它可看作indeno[1,2-b]fluorene(2,图2)的π扩展类似物,该分子吸收光谱显示出与indeno[1,2-b]fluorene几乎类似的特征吸收峰,同时结合变温核磁氢谱以及EPR的实验结果表明,该分子展示出闭壳层的醌式结构特征。随后在2017年,该团队合成并分离了芴并芴的另一种同分异构体fluoreno[3,2-b]fluorene(6,图4,Org. Lett., 2017, 19, 5312)。同样地,实验结果表明分子6的萘核依然表现出醌式结构的特征,如明显的单双键交替。同时Tobe团队也对indeno[2,1-b]fluorene进行了共轭延伸,制备得到了分子fluoreno[2,3-b]fluorene(7,图4,J. Org. Chem., 2017, 82, 1380),通过共振结构可以看出,分子7的双自由基结构获得了额外的一个芳香六隅体以及芳香萘环,因此可以大致判断该分子具有开壳的双自由基特征。实验结果表明,相较于分子fluoreno[4,3-c]fluorene,fluoreno[2,3-b]fluorene具有更高的自由基指数(y= 0.68 vs. y= 0.772),这也与其更大的π共轭体系吻合。
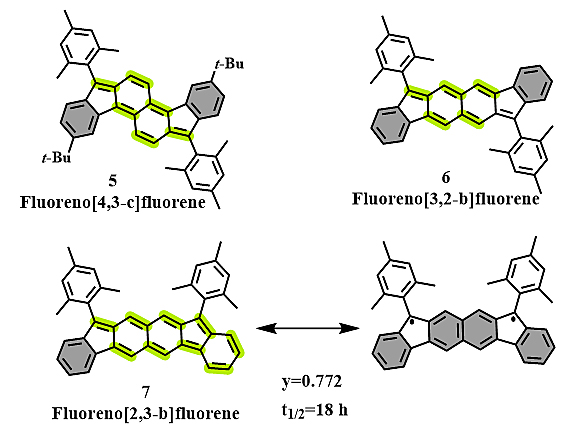
图4. Haley和Tobe等人报道的fluoreno[m,n-x]fluorene分子。
随后,Haley团队继续对萘核进行扩展,于2016年报道合成了diindeno[b,i]anthracene (DIAn)衍生物(8,图5,Nat. Chem., 2016, 8, 753),相比于芴并芴分子5和6的闭壳醌式结构,分子8的理论计算和实验数据证明,该分子的自由基指数为y= 0.62,且具有相当高的稳定性:溶液状态中半衰期为两个月,而在固体状态中愈加稳定。这项工作也为研究稳定的稠环芳烃自由基提供了重要的参考价值。分子8中引入的两种大位阻保护基团(TIPS和mesityl基团)有三个重要的作用:(1)蒽核上的TIPS基团可以有效防止蒽核的降解;(2)位于五元环顶点的mesityl基团对具有高电子自旋密度的位点提供动力学保护;(3)两个大位阻的基团可以控制傅克反应位点的选择性,使反应发生在碳3、7号位,而不是更富电子的碳1、5号位。
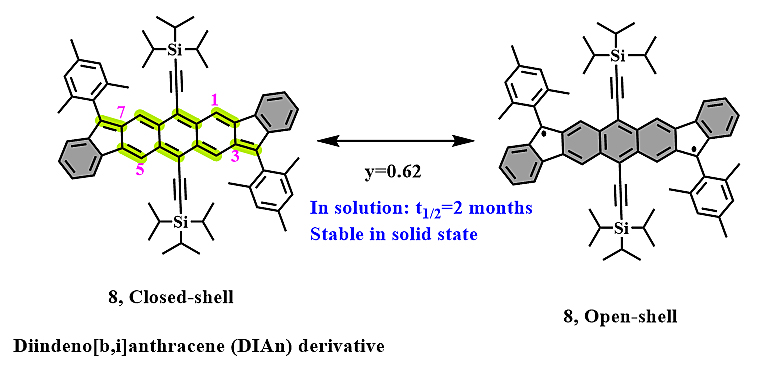
图5. Haley等人报道的DIAn分子。
除了对茚并芴体系内核的扩展,Haley课题组也对外围的苯环进行了替换和扩展。如将indeno[1,2-b]fluorene的外围的苯环用苯并噻吩取代,得到了anti-IDBT和syn-IDBT(8和9,图6,Chem. Sci., 2016, 7, 5547),研究显示,相比于indeno[1,2-b]fluorene,苯并噻吩取代后的两个分子的反芳香性显著增加,但仍然显示闭壳的结构特征。
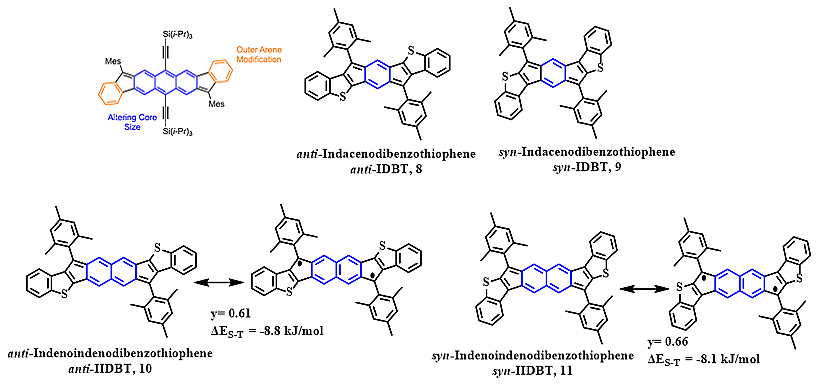
图6. Haley等人报道的苯并噻吩衍生物分子。
紧接着在2018年该团队对anti-IDBT的核s-indacene进行扩展,合成并分离了anti-IIDBT(10,图6,Nat. Chem., 2018, 10, 1134)。理论计算表明anti-IIDBT的自由基指数为0.61,意外的是这与DIAn衍生物分子的自由基指数(y= 0.62)非常接近,但两者的ΔES-T却相差甚远:DIAn: -4.9 kJ/mol, anti-IIDBT: -8.8 kJ/mol。为了解释这个反常的现象,该团队采用了双电子的自由基模型进行讨论:
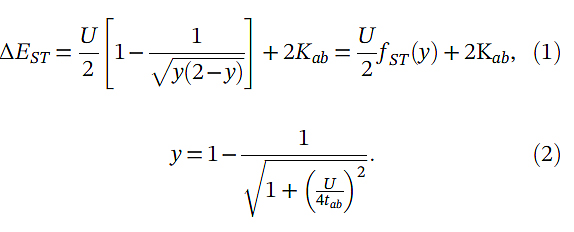
其中,U代表代表电子之间的排斥,tab代表能量共振,而Kab在该体系下可以忽略不计。通过对这两个影响因素进行分析,就可以解释为什么anti-IIDBT具有如此高的ΔES-T:硫原子上的孤对电子与自由基中心存在强的相互排斥作用。另外,多个实验测试结果也证明了理论预测的数据:变温核磁氢谱中,将温度升到125 ℃时,分子anti-IIDBT芳香区的峰才开始变宽;超导量子干涉仪(SQUID)的信号峰也在400 K以上时才慢慢出现,并通过Bleaney-Bowers方程算得ΔES-T为-8.0kJ/mol,基本与理论计算的结果相吻合。
通过改变分子的顺反构型是否能做到精确调控ΔES-T?Haley课题组在2020年继续报道了syn-IIDBT分子(11,图6,J. Am. Chem. Soc., 2020, 142, 1548),理论计算表明该分子的自由基指数为0.66,高于anti-IIDBT,ΔES-T为-8.1 kJ/mol,低于anti-IIDBT。这种差异大致可以从两方面来理解:(1)anti-IIDBT中自由基与硫原子之间为线性共轭,有利于电子之间的相互作用,而syn-IIDBT为交叉共轭,电子之间的相互作用稍弱;(2)anti-IIDBT的自由基共振结构中,只有一个结构的自由基中心远离硫原子,而syn-IIDBT则有两个。因此相比于分子anti-IIDBT,分子syn-IIDBT的电子之间相互排斥作用较小,进而存在y和ΔES-T的差异。
既然苯并噻吩与内核的连接方式可以影响到参数U,从而引起自由基指数和ΔES-T的改变。因此Haley团队设想是否也能通过设计不同的分子来影响参数tab(或键级BO),同样也能做到精确调控分子的自由基指数和ΔES-T。于是在2020年,该团队合成了一系列的DIAn衍生物(12-14,图7,J. Am. Chem. Soc., 2020, 142, 20444)。可以看出,从分子12至14,随着键级(分子中标为红色的键)的增大,相应的自由基指数也随之增大。同时随着这三个分子共轭长度的增加,使得电子云可以比较好的离域到整个分子的末端苯环,从而使得参数tab下降,根据方程1和2,其相应的自由基指数会升高,而ΔES-T则会随之下降。
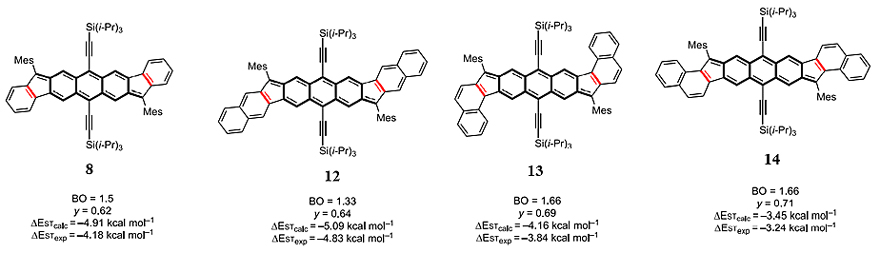
图7. Haley等人报道的DIAn衍生物分子。
3. 基于七元环的自由基体系
相比于五元环体系,七元环在合成上的难度更加具有挑战性,因此,到目前为止有且只有两例基于七元环的具有开壳双自由基性质的分子。如图8,冯新亮团队在2019年报道了首例在溶液中合成的基于七元环的双自由基分子15(J. Am. Chem. Soc., 2019, 141, 12011),从其自由基形式的共振结构可以看出,获得了三个额外的Clar芳香六隅体,因此可以初步推断该分子具有开壳双自由基的特征,同时,通过SQUID以及EPR等测试结果也表明分子在一定温度范围内表现出磁性,证明了其双自由基的性质。由于分子15极其不稳定,半衰期仅为2 h,要想获得单晶数据也极其困难。因此,该团队又在金(111)表面上制备得到了分子16,并通过隧道扫描电镜确定了其结构,理论计算表明,该分子具有极高的双自由基指数(0.92)。
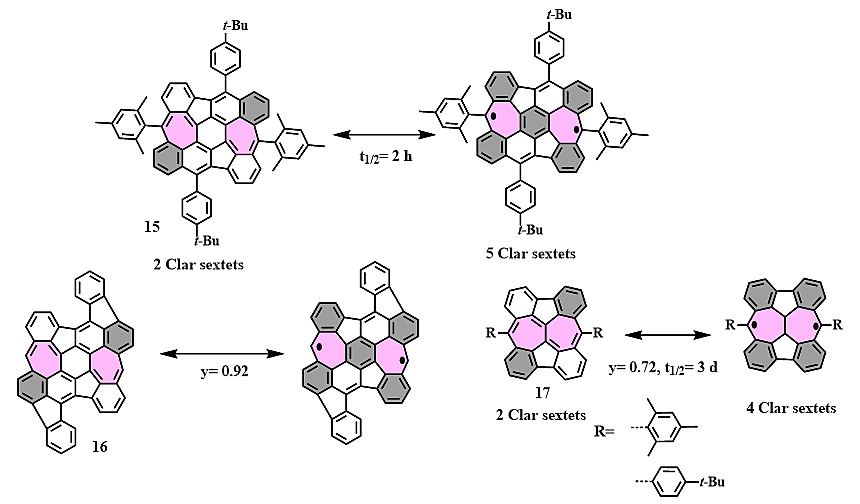
图8. 冯新亮团队和Yasuda团队分别报道的基于七元环的双自由基分子。
同一年,大阪大学的Yasuda课题组报道了另一例高度对称的基于七元环的双自由基分子17(J. Am. Chem. Soc., 2019, 141, 10165),其双自由基特征也可根据Clar六隅体规则大致推断出来。相对于分子15,分子17自由基指数较低,因此具有一定的稳定性(半衰期为3天)。分子结构也可由单晶数据准确地证明,同样地,其双自由基的特征性质也由SQUID和EPR数据得到了验证。
(本文由Finisher供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
具有开壳双自由基特征的稠环芳烃 2021-06-22
-
基于二茚并吡嗪骨架的稳定三线态基态共轭双自由基 2020-12-01
-
具有“柔性”构型的双芴基卟啉双自由基 2018-01-29
-
稳定的[4,3]peri-acene双自由基分子:合成、结构和电子性质 2020-12-28
-
具有双自由基特征和金属导电性的石墨烯纳米带分子的合成与性能研究 2017-04-20


































 京公网安备 11010802027423号
京公网安备 11010802027423号