宋秋玲教授课题组JACS:首例不对称催化合成轴手性芳基硼化合物
手性有机硼化合物是有效构建光学活性分子的重要合成中间体,因此手性有机硼化合物的合成受到了化学家们高度的关注。近年来,合成化学家们发展了一系列高效的合成反应,包括不对称硼氢化、不饱和键的不对称加成、C-H 硼化等来构建手性有机硼化合物。然而,目前所有报道的例子都仅限于中心手性有机硼化合物的构建。与成熟的中心手性硼化学相反,以 C-B 键为主轴的轴手性化学发展缓慢,具有极大的挑战。这一挑战的主要原因可能源于长的Csp2-B键 (1.58Å) 所引起的低旋转势垒,而常见的联芳基化合物Csp2-Csp2键的键长仅约1.46Å;因此对于以C-B键为主轴的轴手性化合物而言,增加反应底物位阻则会导致反应不易进行,而位阻小则易于消旋。轴手性骨架常见于手性配体或有机催化剂、天然产物、药物以及材料等领域,其合成也因此受到化学家的持续关注,发展不对称催化来合成C-B 键轴手性化合物将大大增加轴手性化合物的种类,并有可能带来有机硼化合物新的功能和性质,因此具有重要的意义。
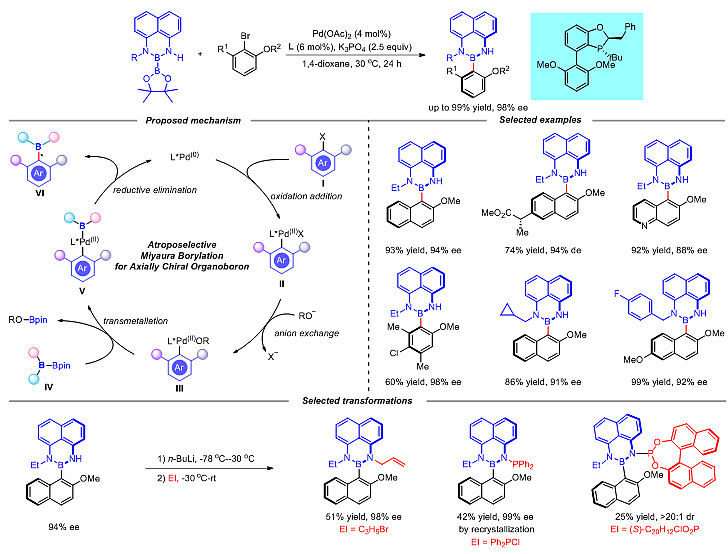
Miyaura 硼化反应由 Miyaura在1995 年发现并命名,是芳基卤化物和联硼酸频那醇酯(B2pin2)之间的偶联反应,也是构建芳基硼化合物的一种广泛而有效的方法。受该反应的启发,宋秋玲教授(点击查看介绍)课题组通过合理地设计出非对称联硼试剂,利用不对称Miyaura硼化反应高效、高对映选择性地构建了以C-B键为主轴的轴手性芳基硼化合物,首次实现了以不对称催化的方法合成以C-B 键为主轴的轴手性化合物。该反应的可能机理是:芳基卤化物I与手性 Pd(0)氧化加成得到手性芳基钯中间体II。随后,芳基钯中间体发生阴离子交换产生中间体III。然后,中间体 III 和非对称联硼试剂 IV 经转金属过程得到中间体V,最后经还原消除得到轴手性芳基硼 VI 并再生手性 Pd(0) 催化剂。该反应具有广泛的底物范围、高产率和高对映选择性。通过该方法合成的轴手性芳基硼化合物可以进一步转化,并能很好地保持其高对映纯。
相关研究结果发表在化学领域权威期刊Journal of the American Chemical Society,论文的通讯作者为宋秋玲教授,第一作者为福州大学化学学院杨凯博士,硕士研究生毛彦菲、徐杰、王昊、何勇和李汪洋做了重要贡献。该研究工作得到了福州大学和国家自然科学基金的大力支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Construction of Axially Chiral Arylborons via Atroposelective Miyaura Borylation
Kai Yang, Yanfei Mao, Jie Xu, Hao Wang, Yong He, Wangyang Li, and Qiuling Song*
J. Am. Chem. Soc., 2021, DOI: 10.1021/jacs.1c04345
导师介绍
宋秋玲
https://www.x-mol.com/groups/song_qiuling
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号