ACS编辑良择 | 利用传统及单分子表征方法研究杂交链式反应的功能化和信号转化效率

每天,ACS遍布全球的期刊编辑们从ACS的众多期刊中选出一篇新近发表的文章,限时免费开放给所有读者。这些被特别选出的文章所探讨的最新研究成果将因其免费开放而使更广大的科研受众获益。
英文原题: Study on the Functionalization and Signaling Efficiency of the Hybridization Chain Reaction Using Traditional and Single Molecular Characterizations

通讯作者: Bingling Li (李冰凌) , State Key Lab of Electroanalytical Chemistry, Changchun Institute of Applied Chemistry, Chinese Academy of Sciences, China; Department of Chemistry, University of Science and Technology of China, China
作者: Chunmiao Yu (于春淼), Yesheng Wang (王叶盛), Ruiping Wu (吴瑞萍), Zhentong Zhu (祝振童), Bingling Li (李冰凌)
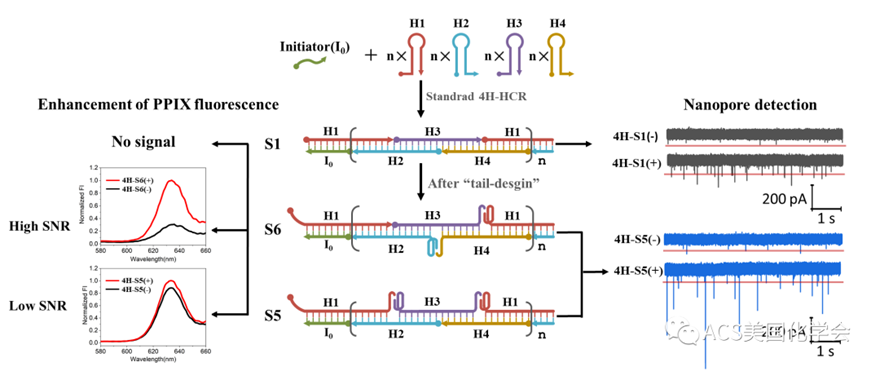
近日,中科院长春应化所李冰凌团队以"四发卡型核酸—杂交链式反应(4H-HCR)"为模型,系统研究了不同表征方法下杂交链式反应(HCR)的几种"底物加尾设计"及其组装效率、信噪比之间的联系和规律。该工作为HCR反应的高效设计、清晰表征和应用拓展提供了有效的指导方向,也为其他核酸组装反应的合理设计和性能优化提供了潜在的研究思路。
信号放大反应在生命分析中起着至关重要的增敏作用。在过去的几十年间,科学家们相继发明出一系列无需蛋白质酶即可在恒温条件下进行循环放大的核酸组装反应(即核酸分子线路或无酶等温放大反应),成为核酸组装和分析领域的研究热点。其中,一种代表性核酸分子线路—杂交链式反应通过短片段的单链DNA触发几种发卡型底物间发生循环置换反应,最终形成链状的DNA双螺旋串联体,可以同时实现尺寸和数目上的信号增敏。经过不断的创新设计和功能探索,目前HCR已经具有多样化的反应路线、信号输出方式和应用场景。检测靶标也由核酸扩展至蛋白质、小分子、金属离子和肿瘤细胞等。尽管如此, HCR中仍存在一些有待解决的性能和表征问题,大大制约了其实际应用。例如,在各种创新设计中, HCR的发卡底物末端往往需要延伸出一段不参与反应的寡核苷酸(称为发卡尾巴),用作信号探针或提供更好的识别和扩增功能。而实验表明,一旦在HCR中采用了这样的"发卡加尾设计",就可能面临组装难度升高或信噪比(SNR)降低的风险,使得整个反应变得难以控制,设计和应用。
为系统探索HCR底物发卡尾巴和组装效率/信噪比之间的关联和规律,作者在文章中设计了以四个发夹型核酸为底物的HCR反应模型(4H-HCR),并通过多样化的"加尾设计"(在一个或多个发夹末端附加额外的尾巴序列),最终形成图1和S1所示的10种不同组装反应的链状产物,命名为S1-S7 (其中S2和S6分别包括简单分型:S2’和S6’, S6’’)。理论上,在4H-HCR组装完成后,S5, S6和S7产物上两条相邻的尾巴可以组合成一个完整的G-四链体悬挂结构,该结构是无酶分子线路中广泛使用的信号探针,可以通过增强某些卟啉衍生物(如PPIX)的荧光发射强度(示意图1),为HCR组装与否提供判断依据。
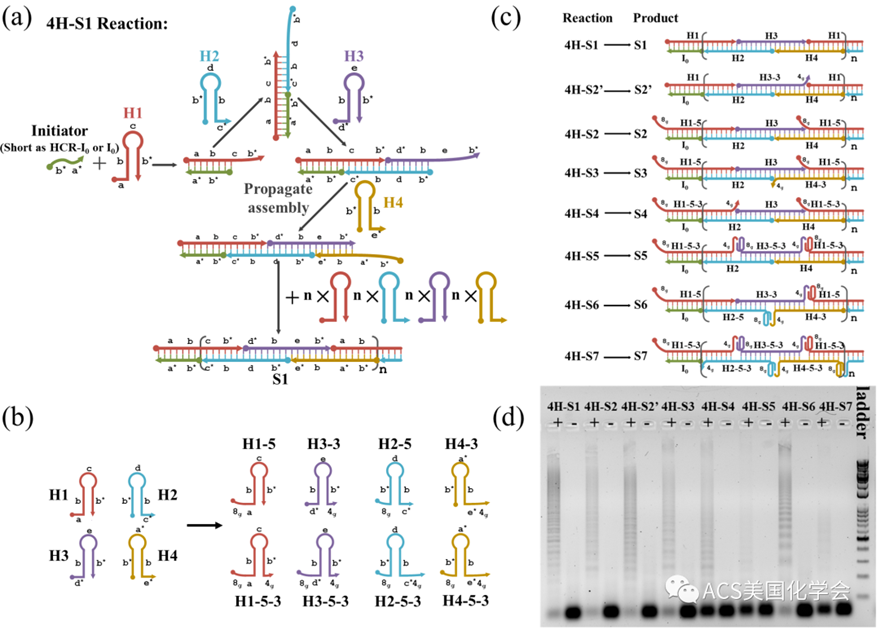
图1. 4H-HCR反应路径 (a)及具有不同"加尾设计"的反应模型 (b),对应产物 (c) 和反应产物的琼脂糖凝胶电泳表征 (d)。
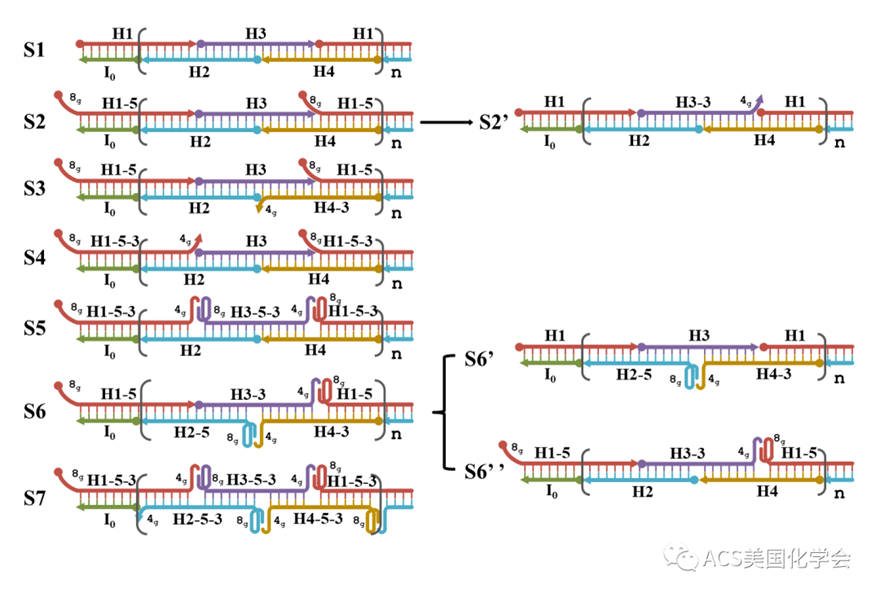
图S1.设计的所有4H-HCR对应的产物结构。
作者首先利用传统的琼脂糖凝胶电泳,对有无单链DNA引发剂的S1-S7 HCR体系进行了系统表征,揭示了HCR发卡"加尾设计"和组装效率之间的大致规律(rule-set)。结果表明尾巴的存在确实会抑制HCR的组装效率,抑制程度与四个发卡底物尾巴总数及尾巴碱基数正相关(图1d)。产生这种组装抑制现象的一个重要原因是在每一步HCR组装发生后,未参与HCR反应的尾巴会,产生一个自由摆动的负电排斥力场,一定程度地阻碍或延缓下一个发卡底物的靠近和结合。由此可以进一步推测,在尾巴总数一定的情况下,一个双尾发卡底物(一个发卡5’端和3’端均携带尾巴)产生的负面作用较两条单尾发卡底物(一个发卡5’端或3’端携带尾巴)更为显著;过多引入双尾底物甚至会完全抑制整个组装反应,这一推测也得到了实验的验证(图1d, S7)。同时需要强调的是,文中G-四链体结构的形成是依赖K+环境的,因此在含有K+的缓冲条件下,双尾发卡的两条尾巴自身即可组装成稳定的G-四链体结构,由此产生致命的"自锁效应",也会完全抑制整个组装反应(图2c, S5)。
作者随后又通过荧光光谱,对S5, S6和S7这三种有望形成G-四链体悬挂的HCR反应进行了PPIX荧光增强表征。该结果进一步证实了复杂的 "加尾设计" 不仅抑制HCR的组装效率,还会降低G-四链体/PPIX荧光信噪比。在这几种设计中,只有仅含单尾发卡底物的S6及其分型(S6’和S6’’)展现出了理想的荧光信噪比(图3),可用于传感器等功能化应用。由此可见,为保障HCR反应的组装效率和较高的信噪比,"加尾设计"应极为小心,应充分考虑发卡底物尾巴数目及碱基数,以及自身是否存在二级组装,尽量避免过多引入双尾发卡以及自锁结构。
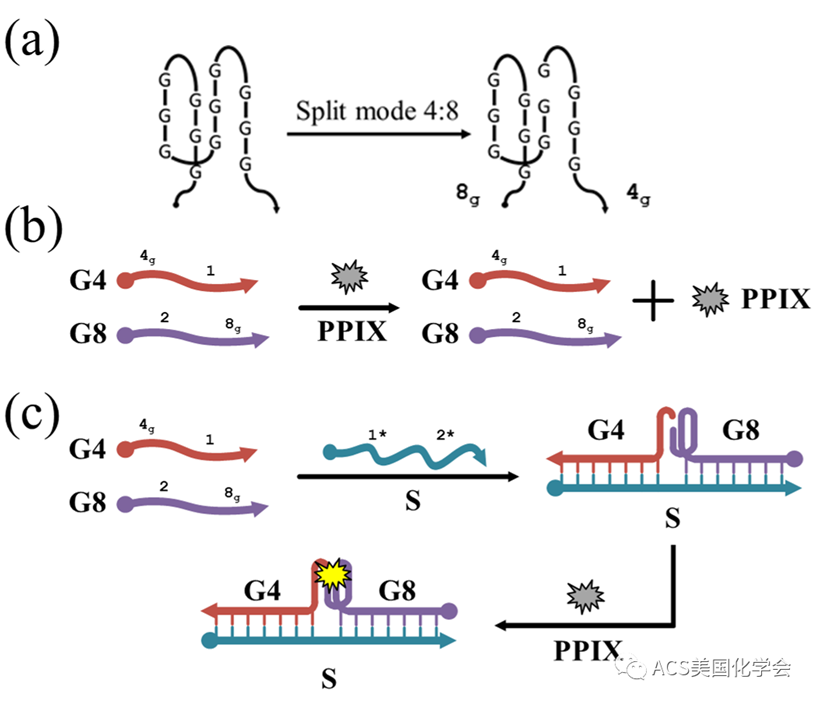
示意图1. G-四链体拆分模式 (a) 和诱导组装后PPIX荧光增强过程 (b和c)。
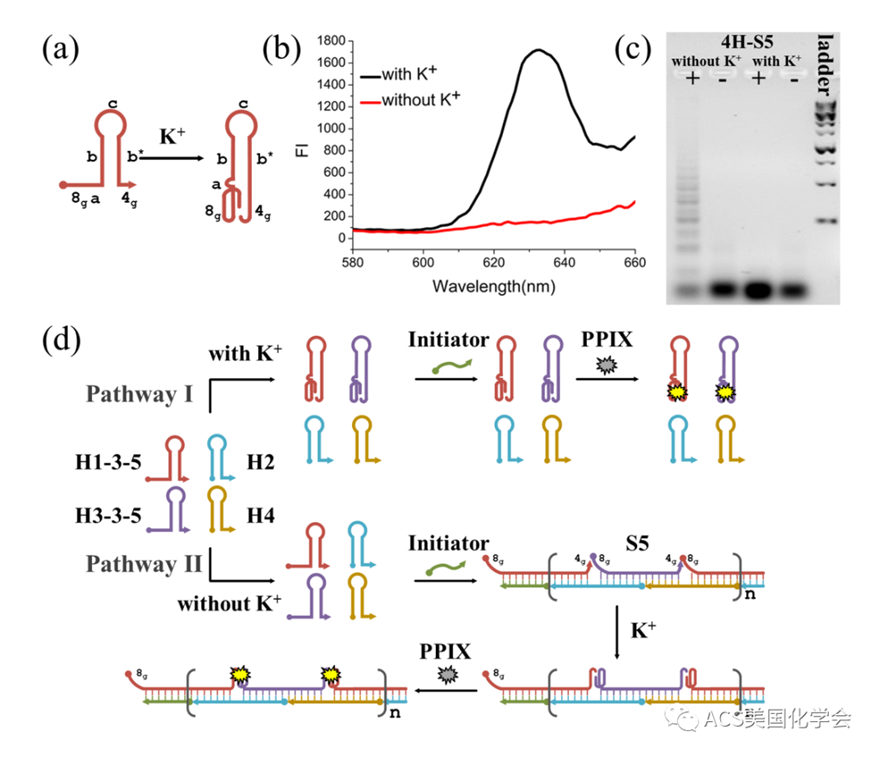
图2. S5发卡底物 (H1-5-3) 在K+存在下的"自锁效应" (a-c) 以及4H-HCR组装路径 (d)。
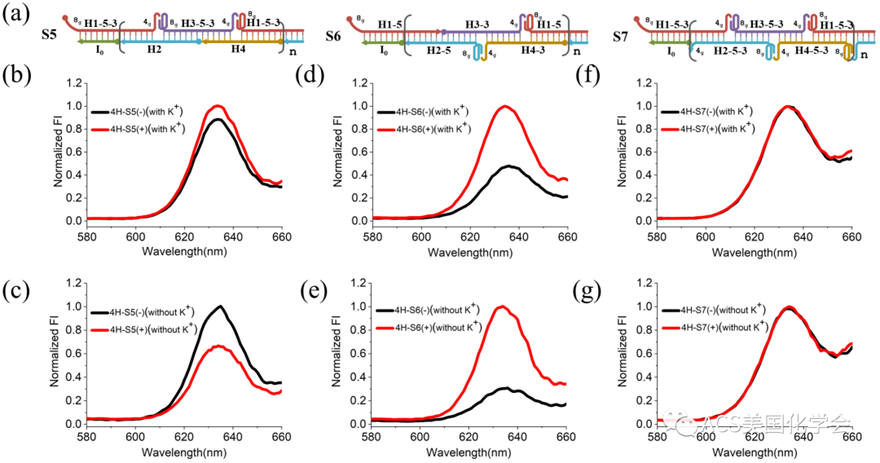
图3. 4H-S5、 4H-S6以及4H-S7反应产物的 G-四链体增强的PPIX荧光表征结果。
作者还发现即便某些设计在优化后可以呈现较好的HCR组装效率,但依然面临着表征难、信噪比低的尴尬情况。例如,使用G-四链体荧光增强信号无法表征不含任何"加尾设计"的S1组装反应,也无法判断存在"自锁效应"的S5组装是否形成(图2c, 图3, S5)。为此,在文章的最后一个部分,作者创新地引入了固态纳米孔单分子检测技术,将其作为HCR组装反应和G-四链体悬挂的一种"抗失败、互惠型"信号读出方式。一方面,当链状组装产物穿过玻璃纳米孔道时,会在基线上产生显著的电流阻塞信号;而组装前的发卡底物,则因为尺寸过小而不会引起电流变化。这一现象可直接用于指示任意HCR反应是否存在有效的组装产物(图4c,4d),因此也同样适用于荧光信号无法表征的S5组装体(图4f,4g)。另一方面,G-四链体悬挂可显著增加HCR产物的有效半径(如S5和S6),过孔引起更大的体积排阻,从而产生更明显的穿孔电流,因此可作为新型的增敏探针,大幅提升纳米孔检测信噪比和分辨率(图4g,图5)。
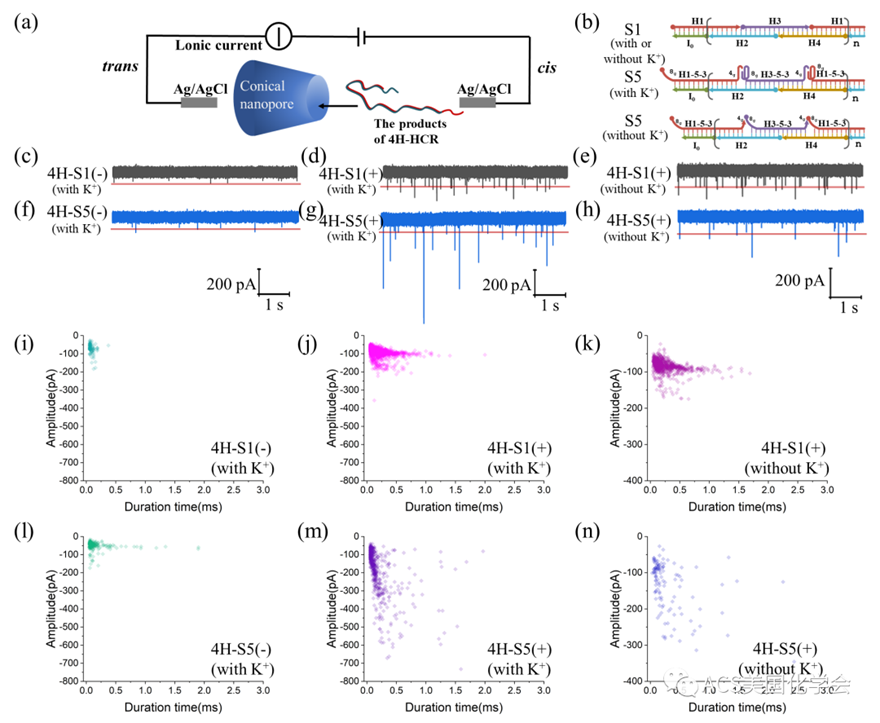
图4. 4H-S1和4H-S5反应产物的固态纳米孔表征结果。
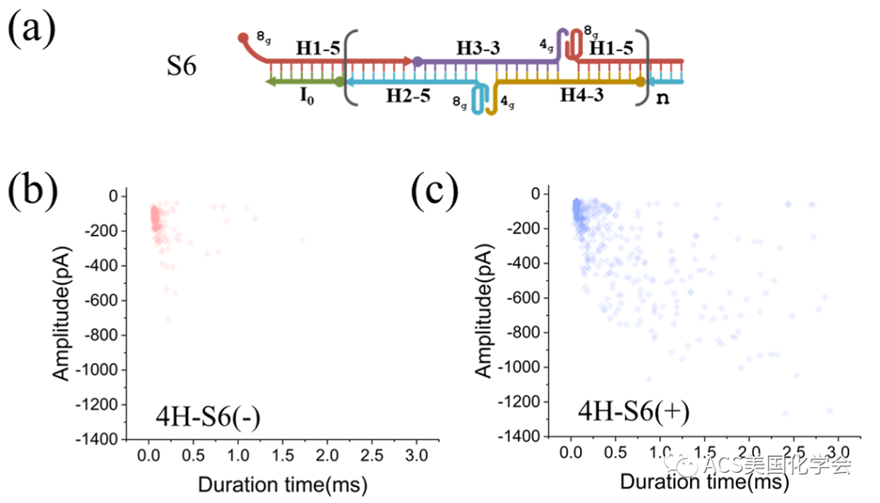
图5. 4H-S6反应产物的固态纳米孔表征结果。
综上,文章以4H-HCR组装和G-四链体悬挂为模型,系统研究并剖析了不同表征方法下HCR的几种"底物加尾设计"及其组装效率、信噪比之间的联系和规律。该工作可为HCR反应的高效设计、清晰表征和应用拓展提供有效的指导方向;也为其他核酸组装反应的合理设计和性能优化提供了潜在的研究思路。值得强调的是,虽然上述结论和规律具有普适的指导意义,但"加尾设计"引起的组装抑制幅度还无法量化,会根据序列和HCR发卡环-茎比的不同而变化。
本研究的相关结果已发表于 ACS Applied Bio Materials。本项目得到了 National Natural Science Foundation of China(国家自然科学基金)的支持。

ACS Applied Bio Materials, 2021, 4, 4, 3649-3657
Publication Date: March 30, 2021
https://doi.org/10.1021/acsabm.1c00136
Copyright © 2021 American Chemical Society

ACS Applied Bio Materials 创刊于2018年7月,仅在线出版,12期/年,已被 Web of Science (Emerging Sources Citation Index),Scopus 等数据库收录,旨在为读者及作者提供生物相关功能材料的设计及其应用的突破性与原创性研究,是将材料学、工程学、生物学、医学及化学知识融合于重要的生物应用的前沿期刊。
涵盖研究领域包括生物材料、生物医用材料、生物能源、生物催化、生物电子、生物污损与防污材料、仿生材料、生物分子成像/传感、药物传递/靶向、自修复材料、抗菌/抗微生物及抗癌生物材料等。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号