Hetidine型C20-二萜生物碱(+)-Talassimidine和(+)-Talassamine的不对称全合成
C20-二萜生物碱主要分离提取于毛茛科乌头属、翠雀属、飞燕草属和蔷薇科绣线菊属(Spiraea)植物,具有多环刚性骨架和复杂的氧取代类型,从而具有丰富的生物活性(图1)。Hetidine型C20-二萜生物碱talassimidine和talassamine是由Nishanov于1991年首次分离以及由王锋鹏教授于2007年再次分离。
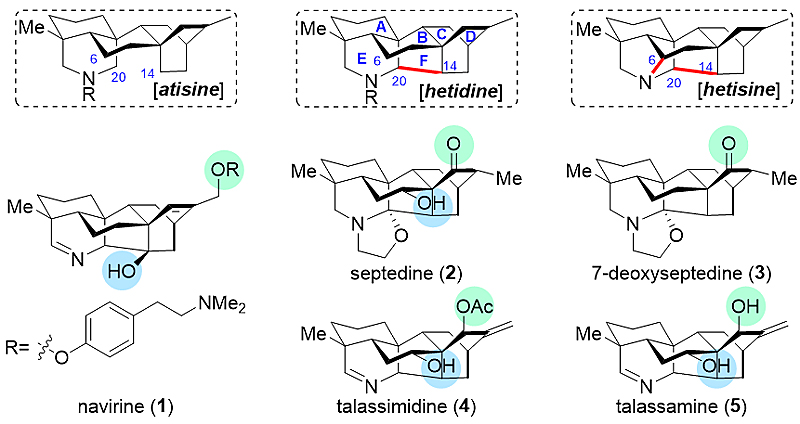
图1. 代表性的C20-二萜生物碱骨架和hetidine型C20-二萜生物碱分子
重庆大学药学院张敏教授(点击查看介绍)团队长期致力于具有重要生物活性和复杂多环骨架的天然产物的全合成研究。该团队于2018年以银催化的异于常规区域选择性的[3+2]偶极环加成反应构建四环骨架中间体14和以SmI2介导的自由基去芳香化反应构建剩余环系,完成了hetisine型C20-二萜生物碱spirasine IV/XI消旋体的首次全合成工作(Angew. Chem. Int. Ed., 2018, 57, 937)。近日,张敏团队通过不对称的[3+2]环加成反应实现了相同四环中间体的不对称构建,并以去芳香化环丙烷化和环丙烷开环为关键反应,完成了hetidine型C20-二萜生物碱(+)-talassimidine和(+)-talassamine的首次不对称全合成。
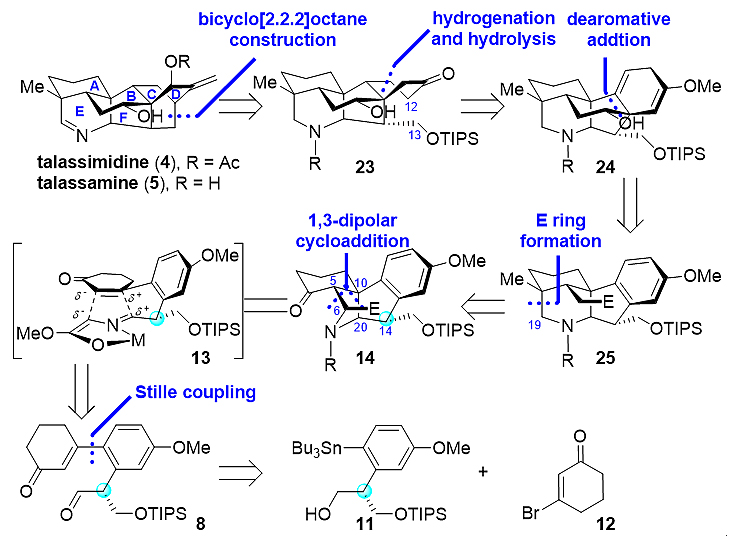
图2. hetidine型C20-二萜生物碱的逆合成分析
基于hetidine型C20-二萜生物碱的结构特征,作者提出了如图2所示的逆合成分析。与文献中常用的Diels-Alder反应构建桥环[2.2.2]辛烷骨架不同的是,作者拟通过分子内aldol反应构建该桥环,从而可为天然产物取代基的引入留下可供转化的官能团;B环的构建和羟基的选择性引入则可通过化合物25衍生的环丙烷中间体的立体选择性开环实现,化合物25则可溯源到四环中间体14。在前序工作中,作者使用消旋的四环中间体14为关键中间体完成了hetisine型二萜生物碱消旋体的全合成。因此,实现四环中间体14的不对称合成,则可实现hetisine和hetidine两种类型二萜生物碱的不对称合成。

图3. Hetidine型C20-二萜生物碱(+)-talassimidine和(+)-talassamine的不对称合成路线
如图3所示,作者从商品化的26为起始原料,通过手性辅基策略,实现了关键前体30的手性合成。随后,通过羟基氧化、亚胺酯制备和偶极环加成的反应条件的筛选,实现了ee值保留的非对映选择性[3+2]偶极环加成反应,从而完成了四环中间体14的不对称合成。随后通过Rh催化的金属卡宾对芳环的去芳香化环丙烷化和环丙烷的SN2型开环反应,实现了B环的构建和极具挑战性的C7-OH的组装。该环丙烷开环策略也适用于在C7位引入其它官能团(如:Cl、I),从而有望应用于天然产物类似物的合成。最终,作者以26和27步的总步骤完成了hetidine型C20-二萜生物碱(+)-talassimidine和(+)-talassamine的首次不对称全合成。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Asymmetric Total Synthesis of Hetidine-Type C20-Diterpenoid Alkaloids: (+)-Talassimidine and (+)-Talassamine
Quanzheng Zhang, Zhao Yang, Qi Wang, Shuangwei Liu, Tao Zhou, Yankun Zhao, and Min Zhang*
J. Am. Chem. Soc., 2021, 143, 7088–7095, DOI: 10.1021/jacs.1c01865
导师介绍
张敏
https://www.x-mol.com/university/faculty/18698
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号