Angew. Chem.:发展比率型荧光生物传感器揭示活细胞内长链脂肪酰基辅酶A代谢的动态调控
长链脂肪酰辅酶A(Long chain Acyl-CoA)是脂质合成、降解和重塑的关键中间体,同时也是细胞内信号传导、离子通道和代谢酶的重要调节剂。此外,长链脂基化(棕榈酰、豆蔻酰等)修饰是一类广泛存在的蛋白质翻译后修饰,该修饰赋予蛋白质特殊的结构和功能,对蛋白调节、信号传导以及癌症的发生具有重要作用。然而,针对长链Acyl-CoA的活细胞检测尤其是动态监测始终是一项具有挑战性的难题,一直以来制约着该类分子亚细胞分布和功能调控研究。
近日,北京大学药学院王晶(点击查看介绍)团队和华中师范大学化学学院杨光富(点击查看介绍)团队合作,利用遗传编码的荧光蛋白传感器技术实现了对长链Acyl-CoA的时空特异性和实时动态监测。该技术通过将循环重排的荧光蛋白cpYFP与来源于大肠杆菌(E. coli.)的长链Acyl-CoA结合蛋白FadR融合表达。当长链Acyl-CoA与该融合蛋白结合后,会诱导蛋白构象变化,从而产生相应的荧光信号。通过进一步蛋白工程进化,该团队获得了对长链Acyl-CoA具有极好的荧光稳定性、选择性和敏感性(亚微摩尔)的生物荧光传感器:LACSer。
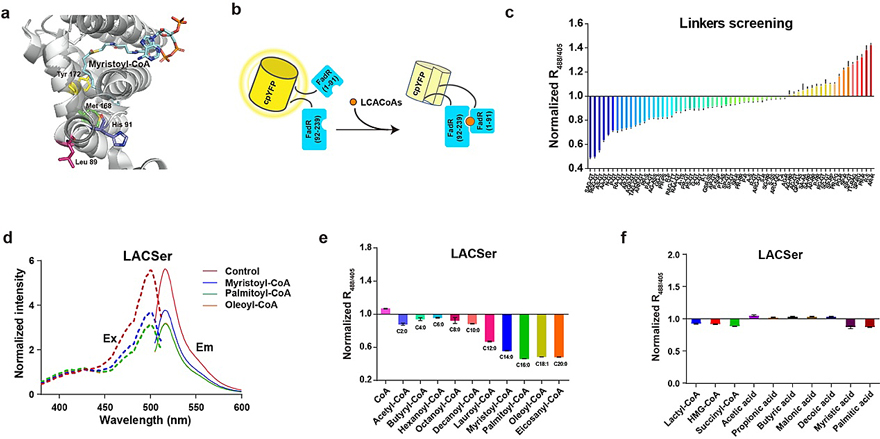
随后,该团队通过引入适当的信号肽与传感器融合,构建得到LACSer的突变体,从而实现了对活细胞内亚细胞区室中的长链Acyl-CoA的比率定量,为实时动态研究活细胞中细尺度的长链Acyl-CoA分布奠定了坚实基础。与此同时,该团队还将LACSer用于研究ACSL酶功能失活后是如何差异性地降低胞质和线粒体长链Acyl-CoA的水平,以及长链Acyl-CoA结合蛋白(ACBP)的功能缺失后是如何影响长链Acyl-CoA在细胞质和线粒体之间的转运。
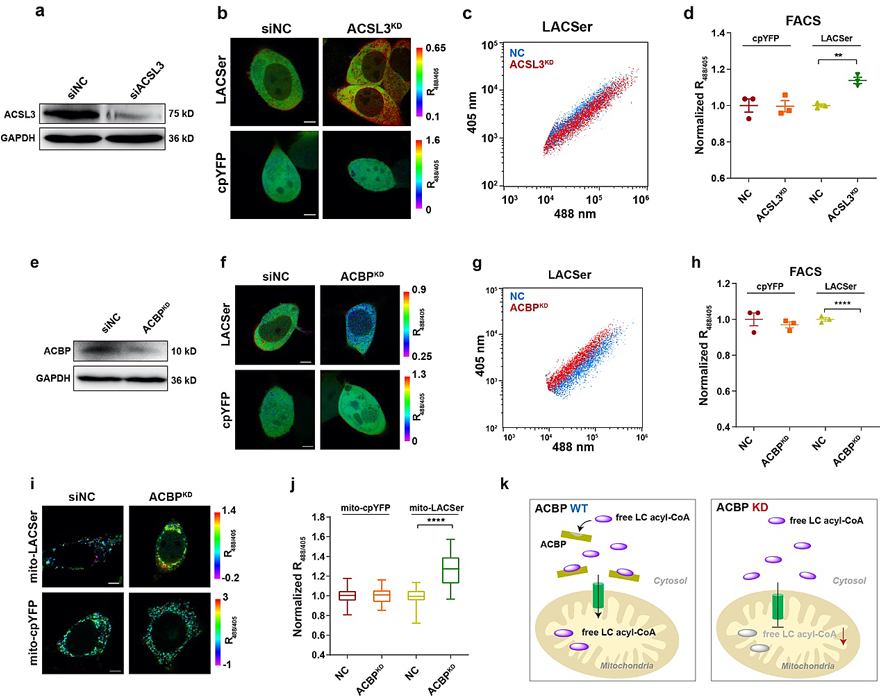
该项研究表明,LACSer传感器可以实现时空精确检测活细胞中内源长链Acyl-CoA水平的动态变化,为细胞内代谢和调控机制研究提供了独特的创新性工具,并为监测长链Acyl-CoA的细胞内合成/利用以及在能量产生与信号转换功能研究打开了大门。该研究不仅有助于进一步加深对脂质代谢的理解,而且可以极大地扩展在代谢工程以及药物开发甚至临床成像中的应用。
这一成果发表在最新的Angew. Chem. Int. Ed.上。该工作得到科技部重点研发计划和国家自然科学基金委等支持。文章的第一作者是北京大学药学院-华中师范大学联合培养博士研究生王尉波和北京大学药学院硕士研究生魏庆鹏。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Ratiometric Fluorescent Biosensor Reveals Dynamic Regulation of Long-Chain Fatty Acyl-CoA Esters Metabolism
Weibo Wang, Qingpeng Wei, Jiayuan Zhang, Meiqi Zhang, Chuchen Wang, Renyu Qu, Yuan Wang, Guangfu Yang* and Jing Wang*
Angew. Chem. Int. Ed., 2021, DOI: 10.1002/anie.202101731
导师简介

王晶,博士,北京大学药学院研究员、博士生导师、天然药物及仿生药物国家重点实验室PI。2009年博士毕业于中国科学院上海有机化学研究所。2009-2014年进入美国芝加哥大学化学系&霍华德休斯医学院(HHMI)从事博士后研究。2016年任职北京大学药学院并入选中组部高层次人才。研究领域:通过化学生物学手段研究小分子对生物大分子的调控机制和开发相应的分子靶向探针。至今以第一作者或通讯作者身份在Nat. Chem.、Nat. Biotechnol.、Angew. Chem. Int. Ed. 等国际重要学术期刊上发表多篇学术论文。
https://www.x-mol.com/university/faculty/59478
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号