NUS吴杰课题组Nat. Chem.:连续流合成与固相合成相结合实现小分子药物的自动化合成与衍生
连续流合成(continuous-flow synthesis)与釜式合成(batch synthesis)相比,连续流合成具有很多优点,例如传热传质效率高、过程可重复性好、过程本质安全、易放大生产从而实现从实验室规模到工业生产规模的有效转化等。连续流合成可将多步反应串联,从而实现药物分子“端-到-端”(End-to-End)合成(Angew. Chem Int. Ed., 2019, 58, 7678–7681; Angew. Chem. Int. Ed., 2015, 54, 983–987),省略掉中间产物的分离提纯,具有非常诱人的工业前景。此外,得益于其反应参数易于精准控制的特点,连续流合成技术与自动化技术相辅相成:两者相结合已被应用于小分子药物的自动化合成(Science, 2015, 347, 1221–1226, 点击阅读详细;Nature, 2020, 579, 379–384, 点击阅读详细;Org. Process Res. Dev., 2020, 24, 2064−2077),反应条件和反应参数的自动化筛选和优化(Science, 2018, 361, 1220–1225, 点击阅读详细;Science, 2018, 359, 429–434, 点击阅读详细)以及与人工智能相结合,实现合成路线智能设计-机器人组装反应装置-自动化合成的“三位一体”应用(Science, 2019, 365, 10.1126/science.aax1566)。正是由于连续流生产能够减少药物生产中的人为差错,提高药品质量,越来越多的制药业开始采用连续流生产技术(Science, 2017, 356, 1144–1150, 点击阅读详细)。
然而当连续流合成应用于药物小分子“端-到-端”合成时,也存在着诸多限制:连续流反应器中进行的多步连续反应,类似于反应瓶中进行的一锅反应,必须对所有合成步骤进行通盘考虑,保证上下游反应溶剂、试剂、产物的兼容。其同时面临反应器压力不断累加,各步保留时间尺度不一致,反应产生固体堵塞可能性增大等问题。即使引入在线分离装置(例如液/液或者气/液)(图1a)或将反应试剂装载于固定床并内嵌在连续流系统(图1b)的策略可以一定程度上缓解上述限制,但是仍然无法从根本上解决多步反应体系的兼容性问题,从而限制了自动化合成中的反应种类和反应步数。多步反应体系中反应溶剂,试剂多样化的兼容性是实现自动化药物合成的最大瓶颈。为此,新加坡国立大学(NUS)吴杰(点击查看介绍)课题组提出了将连续流合成与固相合成(solid-phase synthesis,SPS)相结合的策略:将起始底物固定于树脂并放置于柱式反应器中,将每一步的反应液依次通过反应器进行流动反应,反应完成后进行溶剂洗涤和置换,随后进行下一步反应。基于固相合成中的拟稀释效应(pseudo dilution effect),这种即连续又各步反应互不干扰的方式可以确保对每一步反应进行独立设计和优化,从而从根本上避免了溶剂或者试剂不兼容的问题(图2a),为自动化多步合成开拓了更为广阔的领域。

图1. 多步连续流合成的两种在线分离模型:a) 在线两相膜分离装置;b) 应用固定床固定反应试剂。图片来源:Nat. Chem.

图2. SPS-FLOW 自动化合成系统设计开发和应用:a) 固相合成与连续流合成结合构建SPS-FLOW自动化合成系统;b) SPS-FLOW自动化合成系统的开发流程以及应用于药物小分子及其衍生物合成。图片来源:Nat. Chem.
为了验证这种策略的可行性,吴杰课题组与新加坡国立大学化工学院Khan Saif课题组合作,以用于检查点激酶(CHK)抑制剂Prexasertib为合成目标:首先在反应瓶中实现了该分子的液相合成(solution-batch synthesis)(图3a),在对合成路线中的第三、四、五步的反应参数进行微调后,实现了反应瓶中的固相合成(solid-batch synthesis)。在加入溶剂洗涤和氩气吹扫(为了实现更彻底的溶剂置换)步骤之后,得到了用于自动化连续流合成(SPS-flow synthesis)的化学配方文件(chemical recipe file)(图3b)。根据配方文件的要求搭建了由两台泵、四台自动阀门、一台搅拌器、一根可容纳2克树脂的反应柱和溶剂试剂储存单元组成的自动合成系统(长 88 cm×深56 cm×高56 cm)(图4),并且基于LabVIEW 开发了一套自动化控制程序。在将各步骤的溶剂和试剂准备就绪后,此系统在连续工作32小时后,以65%的重结晶总产率得到了HPLC纯度高于99.9%的Prexasertib三氟乙酸盐635mg。相较于之前的连续流自动化合成系统,开发过程中限制因素减少,设计灵活度增加,所使用的仪器数量大大减少,对复杂化工的依赖度降低,自动化控制更容易实现。整个合成流程包括六步,其中第三步Claisen缩合用到的敏感试剂LDA也能很好的兼容于多步体系当中,即便第二步反应后会用到甲醇洗涤。
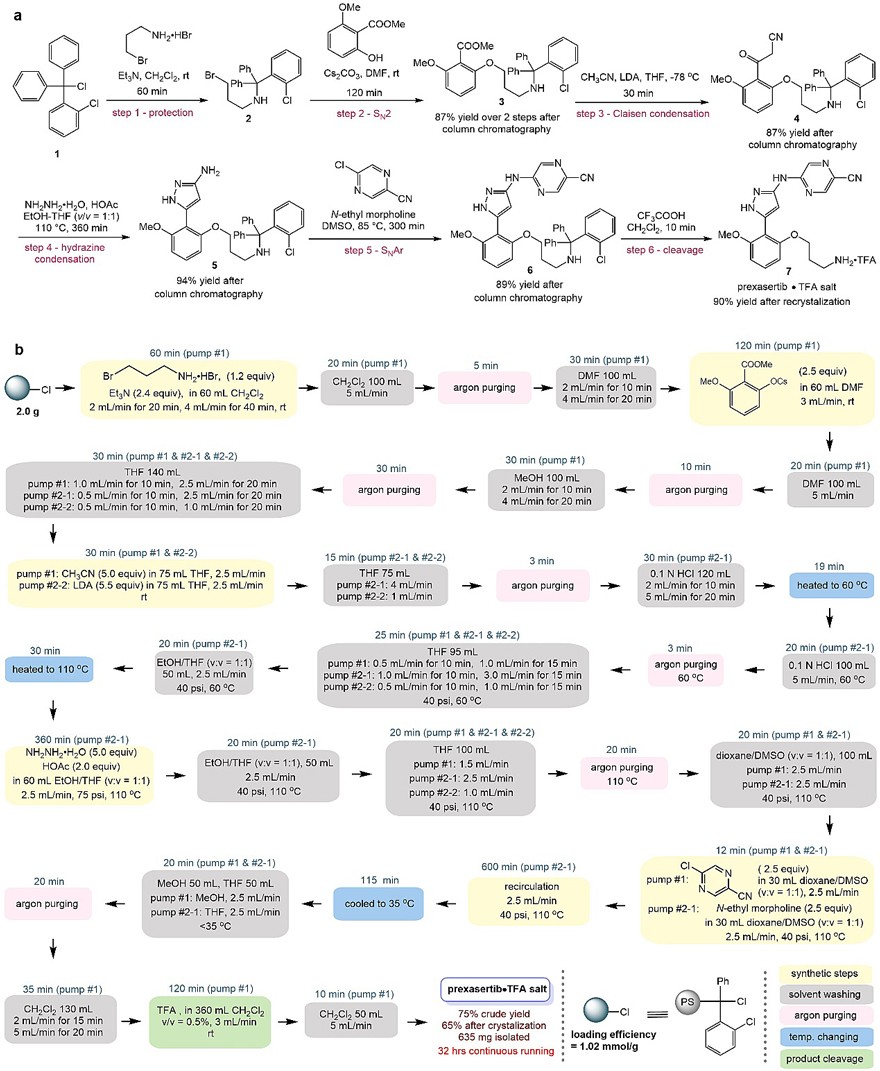
图3. a) Prexasertib的反应瓶中的液相合成路线;b) 自动化合成的化学配方文件。图片来源:Nat. Chem.

图4. SPS-FLOW 自动化合成系统装置构成。图片来源:Nat. Chem.
各步独立运行互不牵制的设计,允许对每一步反应进行调整和替换而又不影响其他步骤,也避免了大规模改变或者完全重置反应系统,这就为药物先导化合物的衍生筛选和优化带来一大利好:既可以对先导化合物进行后期修饰,也实现了“按键式合成”的前期修饰,避免了冗繁的从头合成(de novo synthesis)。在不增加系统开发成本的前提下拓宽了可供筛选和优化的化合物范围,强化了开发此系统的投入产出比。为了展示这一利好,其研究团队实现了23个类似物的完全自动化合成:后期修饰中将第五步SNAr反应的试剂用五氟吡啶替代,得到了类似物8(52% 产率);在将第五步替换成酰胺偶联后得到了类似物9-17(54-70% 产率),替换成还原胺化后得到了类似物18(43% 产率);替换成N-Triflation后得到了类似物19(45% 产率)。前期修饰中将第二步SN2反应替换成Mitsunobu反应后得到了类似物20-29(13-63% 产率);并且Prexasertib也可以通过Mitsunobu反应获得(57% 产率);将第一步和第二步替换成点击反应后则可以得到类似物30(49% 产率)(表1)。
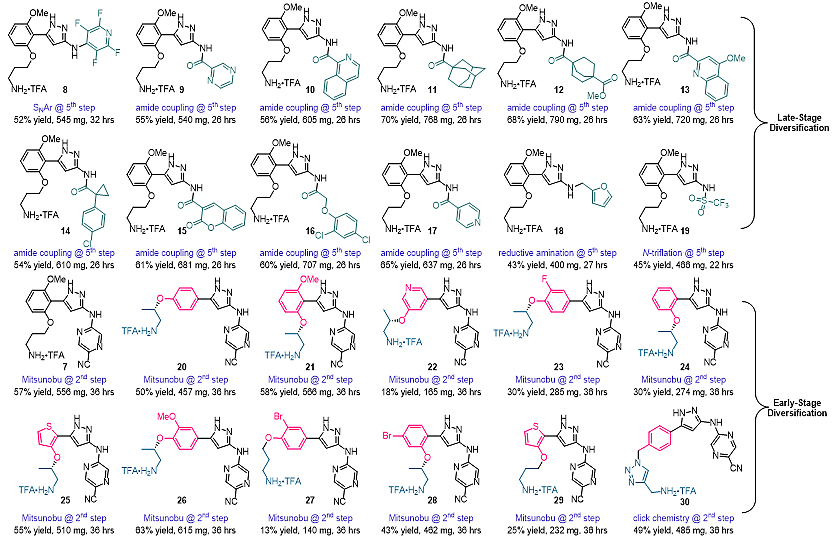
表1. SPS-FLOW 自动化合成系统应用于Prexasertib衍生物合成。图片来源:Nat. Chem.
总结
新加坡国立大学吴杰课题组开发的SPS-FLOW自动化合成系统结合了连续流合成和固相合成的优点,实现了药物小分子Prexasertib的自动化合成。各反应步骤单独设计,独立运行,突破了“端-到-端”连续流合成“牵一发而动全身”的限制。控制参数减少,自动化开发过程直接易实现,大大拓宽了自动合成的反应类型和步数。开发的系统适用于对药物先导化合物进行“按键式”前期和后期修饰(23个类似物),拓宽了药物先导化合物筛选和优化的选择范围,节省药物开发中先导化合物优化所需的人工和时间。
相关成果发表在Nature Chemistry 上,新加坡国立大学博士后刘晨光为本文的第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Automated synthesis of prexasertib and derivatives enabled by continuous-flow solid-phase synthesis
Chenguang Liu , Jiaxun Xie, Wenbin Wu, Mu Wang, Weihao Chen, Shabana Binte Idres, Jiawei Rong, Lih-Wen Deng, Saif A. Khan, Jie Wu
Nat. Chem., 2021, DOI: 10.1038/s41557-021-00662-w
导师介绍
吴杰
https://www.x-mol.com/university/faculty/49776
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
化学科研从“自动化”到“智能化”的六十年 2019-08-25
-
新加坡国立大学吴杰博士课题组近年来工作进展 2018-10-16
-
上《Science》封面的"超级机器",小分子合成的革命? 2015-04-10
-
Nature:全自动“径向合成”,开启合成化学的“互联网+”? 2020-04-06
-
“即插即用”技术如何让化学合成“大众化”?请看这篇Science 2018-10-21
-
解放化学家?Science报道自动化反应机器,每天反应超1500个 2018-02-07
-
礼来Science:如何在CGMP规范下安全高效地制备千克级抗癌药? 2017-07-06
-
Development of a novel, automated, robotic system for rapid, high-throughput, parallel, solid-phase peptide synthesisSLAS Technology: Translating Life Sciences Innovation (IF 2.5) Pub Date : 2023-01-14 ,DOI:10.1016/j.slast.2023.01.002Krisztina Kiss, Soma Ránky, Zsuzsanna Gyulai, László Molnár


































 京公网安备 11010802027423号
京公网安备 11010802027423号