怎么解决FLT3抑制剂耐药性,药物化学家这样回答
急性髓性白血病(AML)是一种造血干细胞恶性肿瘤,其主要表现为骨髓造血系统功能紊乱,造血干细胞过度生长增殖,同时分化和凋亡过程受阻。据统计,AML患者的5年总生存期不到50%,而且AML的发病率随着年龄的增长而增加。
目前,Fms-like tyrosine kinase 3(FLT3)抑制剂在治疗急性髓性白血病方面取得了初步积极的临床疗效,但患者在接受FLT3抑制剂治疗后很快产生耐药性,导致临床响应期短,治疗效果差。其产生耐药性的机制是复杂多样的,且目前临床上仍缺乏有效的治疗手段以克服耐药性。因此,本文系统总结了FLT3抑制剂产生耐药性的原因以及目前解决耐药性的方法,希望能够对新型克服耐药性疗法的开发有所启示。

图1. FLT3发展的关键时间点。
FLT3抑制剂产生耐药性的机制主要包括on-target和off-target两种形式(表1)。On-target机制主要是由于携带有FLT3-ITD突变的患者发生获得性FLT3-TKD突变,如D835V、F691L等突变形式。这种机制主要是削弱了FLT3抑制剂与FLT3激酶的有效结合力,降低了抑制剂对FLT3的抑制能力,从而导致耐药性的发生。Off-target机制主要包括促生长增殖信号通路的代偿性活化、FLT3配体的上调以及骨髓微环境的保护。
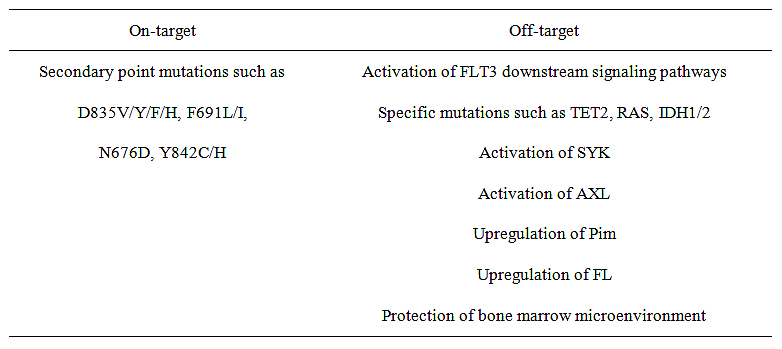
表1. FLT3抑制剂发生耐药性的机制
针对不同的耐药性机制,研究者们开发出了不同的策略以对抗耐药性(图2)。针对on-target机制,作者总结了能够有效抑制耐药突变的新一代FLT3抑制剂的开发思路,其研究主要是基于结构的改造策略,包括避免与突变氨基酸残基的立体碰撞作用、引入额外的作用力以增强与FLT3激酶的结合、合理利用FLT3激酶DFG-out构象中的变构口袋、以及利用FLT3激酶中的亲核性氨基酸残基设计共价抑制剂。
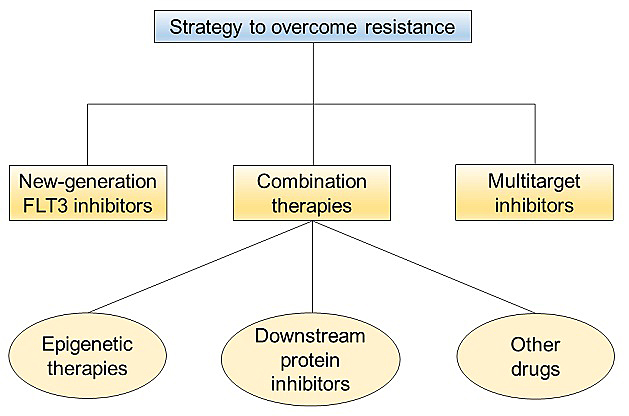
图2. 克服FLT3抑制剂耐药性的主要策略。
针对off-target机制作者总结了结合疗法和多靶点抑制剂在克服耐药性的优势。结合疗法主要是FLT3抑制剂与其他药物同时使用,通过多种机制达到协同抑制肿瘤生长的效果,解决了FLT3抑制剂单药使用发生的药物耐受、响应期短的问题;多靶点抑制剂是通过同时抑制FLT3以及其他的药物靶点,其机制与结合疗法类似,是通过多种机制协同抑制肿瘤细胞生长。同时多靶点抑制剂可以解决结合疗法中复杂的药代动力学性质、难以预测的药物-药物相互作用、病人耐受性差的问题。但其脱靶带来的毒副作用需要被避免。
最后,作者对解决FLT3抑制剂耐药性的问题进行了总结与展望。根据目前的文献报道,针对on-target机制导致的耐药性,I型抑制剂比II型抑制剂有着更加狭窄的耐药谱,如大多数I型抑制剂对发生在活化环上的Asp835突变是耐受的,而II型抑制剂则对此突变无效。同时,变构抑制剂、蛋白水解靶向嵌合体(PROTAC)、分子胶水也许是解决on-target机制导致的耐药性的新方向。另外,尽管针对on-target机制导致的耐药性所开发的新一代FLT3抑制剂发展的如火如荼,但多个获得性点突变,如FLT3-ITD-D835V-F691L突变,也许是未来的又一挑战。结合疗法和多靶点抑制剂用于解决off-target机制导致的耐药性,但结合疗法所面临的复杂的药代动力学性质、难以预测的药物-药物相互作用、病人耐受性差等问题阻碍了它的发展,根据结合疗法设计特异性的多靶点抑制剂也许能够克服这一问题。然而目前的多靶点抑制剂大多处于临床前研究,脱靶带来的毒副作用是其未来需要避免的问题。抗体药物偶联物(ADC)的出现有效增加了药物的靶向性,为多靶点抑制剂带来了新的曙光。此外,研究者还可以从结合疗法与多靶点抑制剂的相互转化受到启发,从而开发出更加有效的AML药物。
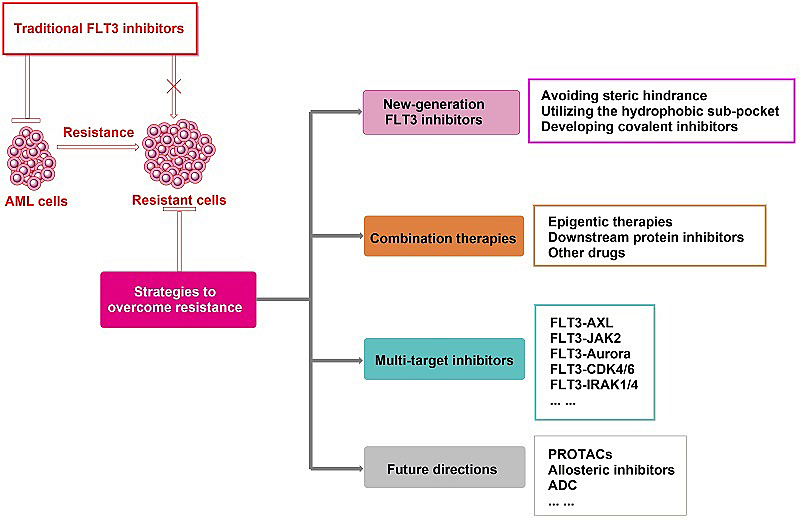
图3. 本文内容概括图。
这一成果近期发表在国际药物化学顶级期刊Journal of Medicinal Chemistry 上,文章的第一作者是中国药科大学博士研究生王志杰。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

FLT3 Inhibitors in Acute Myeloid Leukemia: Challenges and Recent Developments in Overcoming Resistance
Zhijie Wang, Jiongheng Cai, Jie Cheng, Wenqianzi Yang, Yifan Zhu, Hongmei Li, Tao Lu, Yadong Chen, Shuai Lu
J. Med. Chem., 2021, DOI: 10.1021/acs.jmedchem.0c01851
导师介绍
陆涛:中国药科大学教授,江苏省教学名师,副校长。《药学进展》执行主编,《中国药科大学学报》编委。主要研究方向:新药分子设计与合成研究、计算机辅助药物设计、有机合成化学、药物生物统计与计算药学。团队自主研发的抗肿瘤化合物以1.5亿合同价格转让给上海复星医药产业有限公司,目前正在美国、澳大利亚和中国同时开展I期临床研究,主要用于治疗急性髓细胞白血病(AML),2019年11月该药物获美国FDA孤儿药资格认定。
陈亚东:中国药科大学教授,曾获江苏省“青蓝工程”优秀青年骨干教师,江苏省 “青蓝工程”中青年学术带头人。主要研究方向:计算机辅助药物设计、新药分子设计与合成研究、药物生物统计与计算药学。申请国内专利14项,PCT专利3项;在J. Med. Chem., Eur. J. Med. Chem.,J. Chem. Inf. Model.等期刊发表SCI论文80多篇。
卢帅:中国药科大学副教授。已经开展的研究课题包括(1)FLT3 突变体抑制剂研究及其在抗急性髓性白血病中的应用;(2)FLT3/CDK4/6多靶标抑制剂的研究。主持国家自然科学基金青年项目 1 项,江苏省自然科学基金面上项目 1 项。研究方向:小分子抗肿瘤药物的设计与合成、应用 CADD 手段发现、设计并合成新型抗肿瘤药物、药学信息学研究。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号