DNA条形码,私人订制纳米药物!
想象一下未来某天一个病人去医院检查,确诊后医生为了确定适合他/她的纳米药物,就先给他/她注射了小剂量的包含数百种纳米药物的混合液,第二天从病变区取出组织进行检测,随后便确定最适合的纳米药物并进行治疗……听上去似乎有点天方夜谭,但是研究人员的最新研究却正在向着这样的个性化治疗目标迈进,他们利用了一种叫做DNA条形码的技术进行纳米药物的筛选,以期实现个性化治疗。那么DNA条形码是什么呢?事实上,DNA条形码就是一段核苷酸序列,可以通过PCR进行扩增以及基因测序的方法进行解码。通过使用DNA条形码标记纳米药物,研究人员可以找出最佳的治疗药物以及确定不同纳米颗粒的分布。
2016年底,来自以色列理工学院的Avi Schroeder教授课题组在Nature Communications 上发表了一篇有关抗肿瘤纳米药物个性化治疗的研究论文,他们采用了DNA条形码技术对包载不同抗癌药物的脂质体纳米药物的抗癌疗效进行了预测及验证[1]。
目前临床使用的抗癌药物筛选主要通过取出病人肿瘤组织进行体外培养或者移植到免疫缺陷小鼠身上,然后再测试药物敏感性,但是由于肿瘤环境的复杂性,这种方法耗时久、操作复杂、准确率不高。为了解决这些问题,Schroeder等人提出了使用DNA条形码这一技术在单细胞层面来标记、追踪和评估纳米抗癌药物的效果。
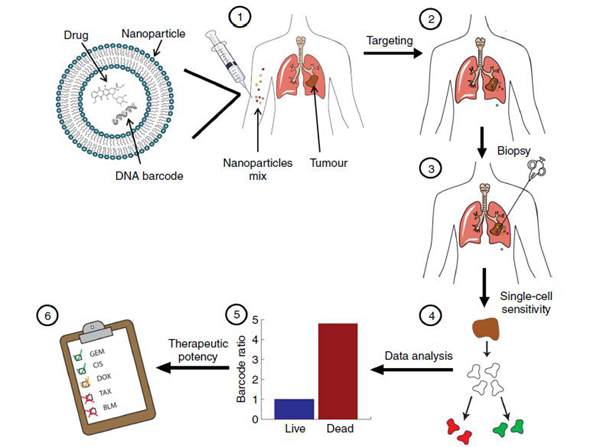
图1. DNA条形码技术预测不同纳米药物抗癌疗效流程图。图片来源:Nat. Commun.
因为脂质体纳米药物已经在临床使用,可以有效富集到肿瘤组织提高药物抗癌疗效,研究人员用脂质体装载不同抗癌药物以及相应的DNA条形码(50-120对碱基对的DNA序列),形成多种100 nm纳米颗粒。他们选择了三种临床使用的治疗三阴性乳腺癌(TNBC)的药物(阿霉素、顺铂、吉西他滨)在小鼠身上进行了验证,一个药物对应一个条形码,形成一个纳米颗粒。通过体外细胞摄取实验,他们发现这种DNA条形码可以在单细胞水平进行检测和定量分析(图2)。
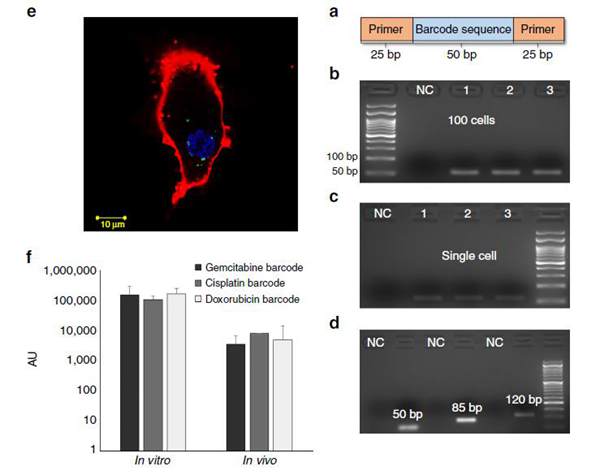
图2. DNA条形码可以在单细胞水平进行检测。图片来源:Nat. Commun.
随后,为了检测这种条形码纳米颗粒是否可以预测抗癌药物的抗癌疗效,他们将3种包载不同药物的脂质体及2个对照组脂质体(一个包载咖啡因、一个不包载化合物)混合在一起,按照低于临床给药剂量的1/1000注射到生长TNBC的小鼠体内,48小时后取出部分肿瘤组织并酶解为单细胞悬液,采用流式细胞术将死细胞、活细胞分开收集并制成细胞裂解液,提取其中的DNA条形码进行扩增并定量检测。
为了定义药物的抗癌疗效,他们将死细胞中含量高的药物定义为疗效好的药物,活细胞中含量高的药物定义为疗效差的药物,以死细胞中的某个DNA条形码含量/活细胞中的该DNA条形码含量定义细胞对药物的敏感性,比值越高表明细胞对该药敏感性越高,亦即该药疗效越好。结果发现吉西他滨对应的DNA条形码在死细胞中的含量远高于在活细胞中的含量,这意味着吉西他滨的抗癌疗效最好(图3)。那么事实上是不是这样的呢?

图3. 使用条形码纳米颗粒预测多种药物的抗癌疗效。图片来源:Nat. Commun.
为了验证条形码纳米颗粒的预测结果是否准确,他们进行了小鼠治疗实验。结果如图4所示,吉西他滨的治疗效果果然是最好的:肿瘤体积、质量均为最小,肿瘤中细胞凋亡数量也最多。这表明DNA条形码纳米颗粒是快速预测抗癌药物抗癌疗效的有效诊断技术,检测所需时间短、操作简单、准确率高。
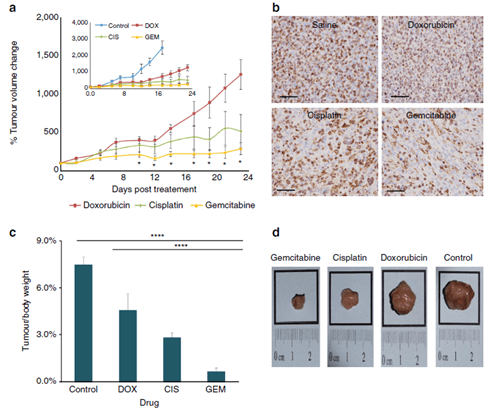
图4. 不同纳米药物的抗癌疗效与预测结果高度吻合。图片来源:Nat. Commun.
Schroeder教授认为这种新技术不仅有助于筛选最佳抗癌药物,还为研究肿瘤对不同药物的耐药性提供了新方法。同时,他也说道:“我的想法更实际:我们的研究能够如何帮助病人呢?目前的研究结果让我很兴奋,但是我们还需要做更多工作将我们的技术发展成为公众唾手可得的产品,但是我相信在不久的将来这项技术一定可以进入临床。”
尽管如此,对于纳米药物而言,药物的体内筛选固然很重要,但是纳米颗粒性质的体内筛选或许更重要,因为纳米颗粒的性质决定了纳米药物在各个组织器官中的富集量,这也就直接决定了药物疗效及副作用。同时,纳米颗粒性质的体内筛选更加繁琐,因为纳米颗粒的组成不仅涉及组成分子的种类不同,还涉及相应分子的分子量、亲疏水链段比例、不同组分比例等等,数量之多,数不尽数!因此要进行体内筛选实在是耗时耗力耗小鼠,筛不起啊。
为此,来自佛罗里达大学、佐治亚理工学院和麻省理工学院的研究人员采用相似的原理和方法成功解决了纳米颗粒体内筛选的问题,实现了快速高通量筛选。他们的实验结果表明利用DNA条形码技术可以在一只小鼠体内同时筛选30种纳米颗粒,快速准确地比较不同纳米颗粒不同时间在不同器官中的富集量,同时实验结果重复性很好,因此极大地节省了筛选所需资源(尤其是实验动物资源),相关研究成果于今年2月发表在PNAS上,通讯作者包括大家熟知的大神Robert Langer教授[2]。
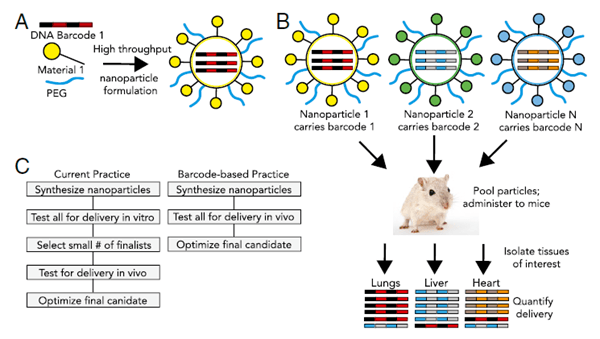
图5. 利用DNA条形码高通量筛选纳米颗粒的流程示意图。图片来源:PNAS
毫无疑问,DNA条形码技术将为纳米药物的发展带来巨大的进展,为药物及纳米颗粒的快速准确筛选带来了希望,允许研究人员在临床给药剂量的1/1000以下水平同时进行多种药物、多种性质纳米颗粒的体内定量研究。如果再结合上微流控纳米颗粒制备技术,纳米颗粒从制备到筛选将不再是问题,这势必将加速纳米药物的开发和优化,促进纳米药物的临床转化。
参考文献:
1. Yaari Z, Da Silva D, Zinger A, et al. Theranostic barcoded nanoparticles for personalized cancer medicine. Nat. Commun., 2016, 7, 13325, DOI: 10.1038/ncomms13325
2. Dahlman J E, Kauffman K J, Xing Y, et al. Barcoded nanoparticles for high throughput in vivo discovery of targeted therapeutics. PNAS, 2017, 114, 2060-2065, DOI: 10.1073/pnas.1620874114
(本文由瀚海供稿)
