DNA组装的光控仿生纳米通道
自古以来自然界遵循着优胜劣汰的准则,生物体在自然环境下经历竞争激烈的生存考验,在自然准则下不断地进化,最终获得适合其所在生存环境的各项功能机制,这些功能机制已臻于完美。向自然学习,研究生命体中的精妙体系用以更好的发展应用是科学研究的永恒主题。近日,中科院理化所江雷院士(点击查看介绍)团队的闻利平研究员(点击查看介绍)和孔祥玉博士利用含偶氮苯的DNA在PET模板上自组装成了一个兼有DNA的生物兼容性以及可修饰性和偶氮苯的光响应性的仿生纳米通道。
生物体系中的纳米通道由蛋白质组成,位于细胞膜上,通过对外界刺激做出打开或关闭的响应行为,从而控制物质迁移,其在生物新陈代谢中扮演着重要的角色。如今,通过仿照生命体中的功能结构,科学家设计出了一系列具有潜在应用前景的特异性响应的智能纳米通道,在传感、分析、药物释放等领域都有重要的基础研究价值。在现有的“刺激-响应”功能纳米器件中,光响应器件因其非接触式的调控机制,以及能将光信号转换成其他有效的信息等特性而引起科学家的特别关注。其中基于通道的光响应门控是一个十分有趣而且有挑战的研究领域,然而要制备一个具有生物兼容而且稳定的光响应纳米通道目前尚鲜有报道。
该团队利用含偶氮苯的DNA在PET模板上自组装形成了一个光响应纳米通道。其中,DNA具有很好的生物兼容性和可修饰性,而偶氮苯的引入更使其兼具光响应性。因此该团队所构筑的功能化的纳米通道能够通过紫外和可见光的辐照刺激来调控离子的跨膜传递特性。
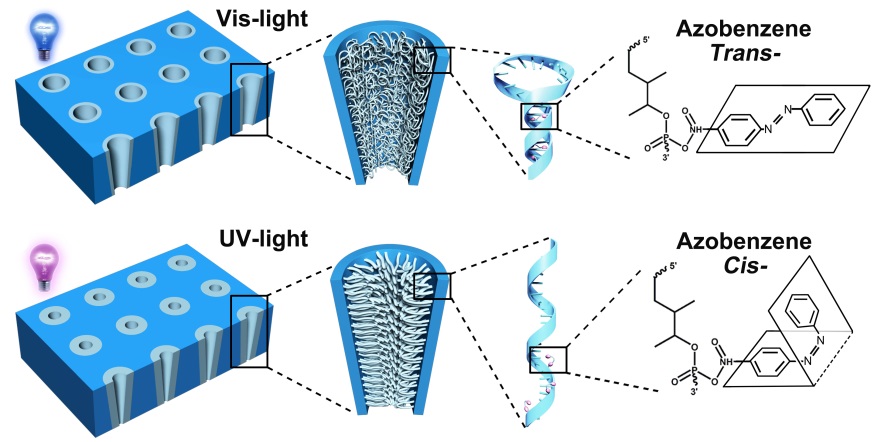
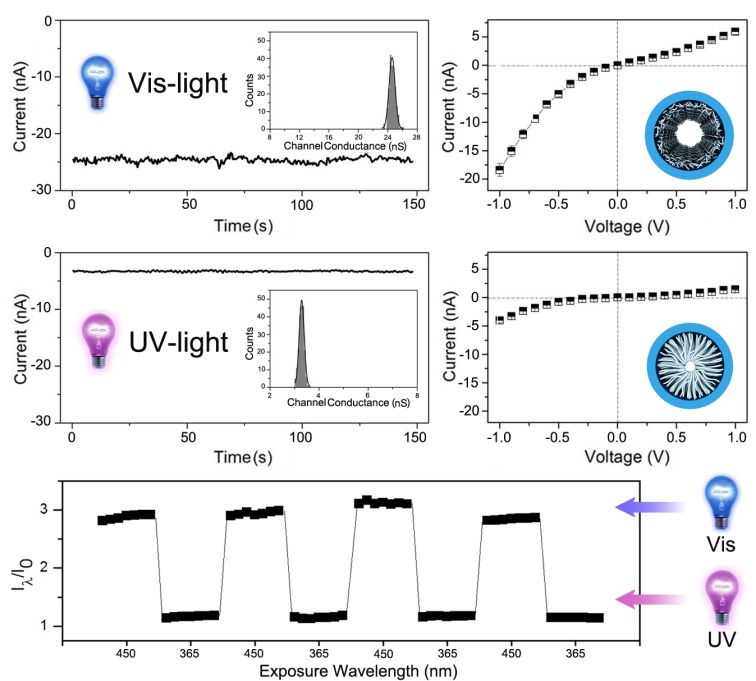
可见光辐照下,偶氮苯分子处于反式平面结构,DNA链呈现发夹结构增加了有效孔径,使得通道处于打开状态,离子电导为24.58±0.02 nS (n=200),而经过紫外光辐照,偶氮苯分子变成顺式非平面结构,DNA链打开,从而减小了有效孔径,使得通道转为关闭状态,此时离子电导减小到3.36±0.01 nS (n=200)。并且这种通过光控调节通道的打开和关闭状态的行为可以稳定的,可逆的进行。此类具有生物兼容性的光控DNA纳米通道开关有望应用于光控药物释放,以及相关生物技术领域。
这一成果近期发表在《Angew. Chem. Int. Ed.》上,文章的第一作者是北京航空航天大学博士研究生李佩和中国科学院化学研究所博士研究生谢柑华。
该论文作者为:Pei Li, Ganhua Xie, Xiang-Yu Kong, Zhen Zhang, Kai Xiao, Liping Wen, and Lei Jiang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Light-Controlled Ion Transport through Biomimetic DNA-Based Channels
Angew. Chem. Int. Ed., 2016, 55, 15637-15641, DOI: 10.1002/anie.201609161
导师介绍
江雷院士
http://www.x-mol.com/university/faculty/15473
闻利平研究员
http://www.x-mol.com/university/faculty/26749
