“一石多鸟”——同时高效转染肿瘤细胞和相关巨噬细胞(TAMs)的非病毒基因载体
在肿瘤靶向的药物/基因递送中,如何靶向和充分利用肿瘤细胞是一般是关注的重点。但是,肿瘤相关巨噬细胞(TAMs)是肿瘤中重要的细胞组分,占有很高的比例,在某些肿瘤中可达到50%。尤其重要的是,TAMs有很强的吞噬能力,将很大一部分经历了“层层屏障”才到达肿瘤内的纳米药物吞噬掉,并通过其强大的消化和酶解作用使得纳米药物失效,这对于易降解的基因药物来说,更是瓶颈难题。因此,若能充分利用TAMs将大大提高纳米药物输送效率。
为此,浙江大学申有青教授(点击查看介绍)、国家纳米科学中心陈春英研究员(点击查看介绍)和刘颖研究员(点击查看介绍)利用酯酶响应的聚合物设计了一种可同时高效转染肿瘤细胞和TAMs的基因输送系统。该输送系统的关键是能够同时实现在肿瘤细胞和TAMs中的快速溶酶体逃逸并在细胞浆中酯酶的水解下快速释放DNA,使DNA能够快速入核进行目的基因的转录和表达。
白细胞介素12(IL12)是一种强大的促炎趋化因子,能够增强细胞毒性T细胞介导的癌细胞杀伤效果,促进TAMs极化为抗肿瘤的M1型。由于缺乏能够有效转染肿瘤以产生足够的IL12的系统基因递送载体,其临床转化应用也受到一定的限制。研究团队利用上述双重靶向肿瘤/TAMs的基因系统输送免疫激活细胞因子IL12基因,可使肿瘤细胞和TAMs都成为生产IL12的“工厂”,从而在瘤内富集高浓度的IL12、有效地激活抗肿瘤免疫反应并重塑肿瘤微环境。例如,转染后肿瘤内M1/M2的比例提高了四倍以上。在三种动物模型中,静脉注射该IL12基因输送系统可以显著延缓肿瘤的生长并使小鼠的生存期增加一倍,全身毒性也非常低。该系统是首个充分利用肿瘤细胞和肿瘤相关巨噬细胞进行系统性高效递送IL12基因的非病毒递送系统。
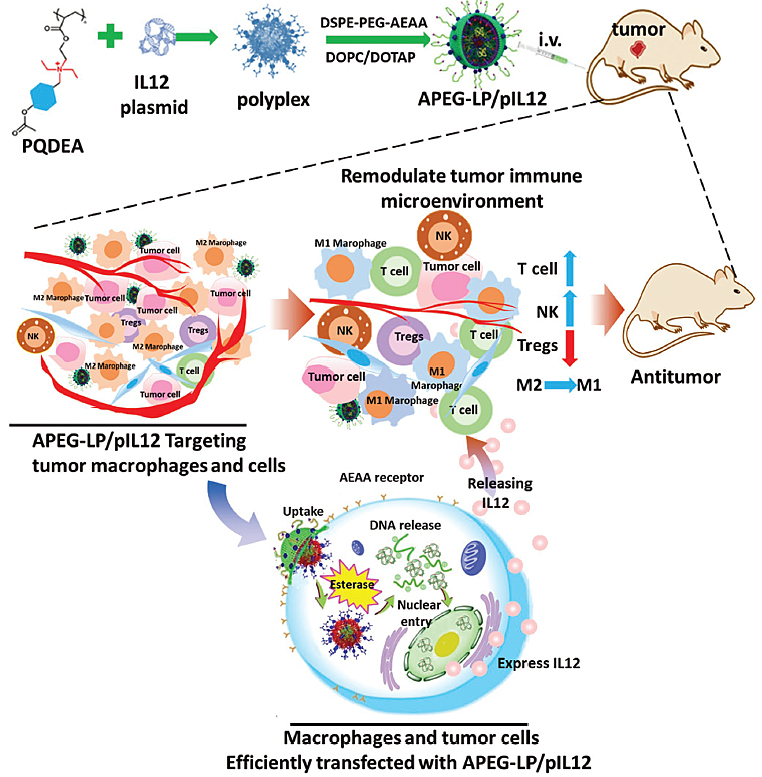
图1. 能同时转染肿瘤细胞和巨噬细胞的非病毒IL12基因递送系统。

图2. 静脉注射的IL12输送系统可将肿瘤内M1/M2的比例提高四倍以上,显著延缓三种动物模型肿瘤的生长并使小鼠的生存期增加一倍。
研究成果发表在国际顶级期刊Adv. Mater.上。国家纳米科学中心特别研究助理邱娜莎为论文第一作者,浙江大学申有青教授、国家纳米科学中心陈春英研究员和刘颖研究员为论文共同通讯作者。该研究得到国家自然科学基金(No. 21704090、51833008)、浙江省重点研究发展计划(2020C01123)和中科院特别研究助理项目 (No. E0D15111)的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Tumor‐Associated Macrophage and Tumor‐Cell Dually Transfecting Polyplexes for Efficient Interleukin‐12 Cancer Gene Therapy
Nasha Qiu, Guowei Wang, Jinqiang Wang, Quan Zhou, Mengyu Guo, Yaling Wang, Xuhao Hu, Huige Zhou, Ru Bai, Min You, Zhen Zhang, Chunying Chen, Ying Liu, Youqing Shen
Adv. Mater., 2020, DOI: 10.1002/adma.202006189
导师介绍
申有青
https://www.x-mol.com/university/faculty/21707
陈春英
https://www.x-mol.com/university/faculty/23167
刘颖
https://www.x-mol.com/university/faculty/23203
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号