设计和合成环约束novobiocin类似物抑制Hsp90,抗癌化疗药物新方向
热休克蛋白90(90 kDa heat shock protein,Hsp90)是一种分子伴侣,可以保证相关蛋白质的正确折叠,对于保持胞内平衡和响应细胞应激至关重要。在癌细胞中,很多Hsp90相关蛋白质(例如HER2、Raf1、Akt、MET、Src、CDK4等)的突变或过度表达,有助于癌细胞的恶性转化和致癌表型维持。抑制Hsp90为同时扰乱多个致癌途径带来了机会。
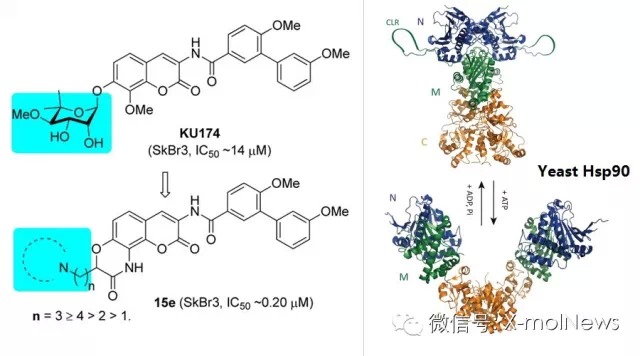
Hsp90的C端抑制剂是一种新的癌症化疗用药,novobiocin是第一个有此类药效的天然产物,但是它抑制肿瘤细胞增殖的活性比较低。与N端抑制剂不同,novobiocin不诱导促生存热休克反应(pro-survival heat shock response)。
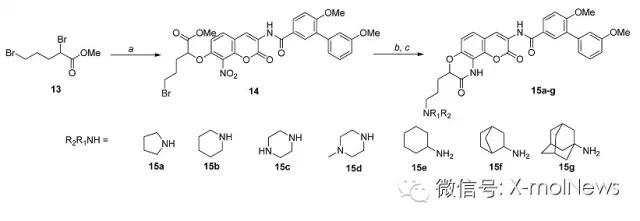
基于结构-活性关系的计算研究,美国堪萨斯大学的科学家们最近报导了环约束(ring-constrained)novobiocin类似物库的设计、合成及评估,更深入地揭示了Hsp90的C端结合位点的特征,为开发高生物活性的Hsp90抑制剂指明了道路。
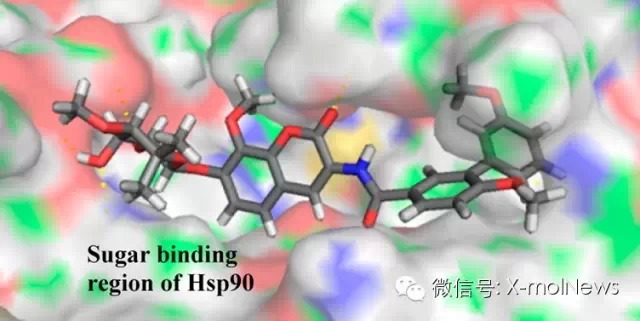
科学家们合成的众多novobiocin类似物,对癌细胞的半抑制浓度(IC50)可以低至μM甚至nM量级,其中一个的IC50为200nM左右。
http://pubs.acs.org/doi/full/10.1021/ml5004475?ref=ec-highlight
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!















































 京公网安备 11010802027423号
京公网安备 11010802027423号