拉链式配对DNA四面体超链接用于miRNA的高灵敏检测
DNA四面体的多能性使该标志性框架成为生物传感与生物器件中引人注目的构建模块。不同于其以往在表界面工程中的广泛应用,近日,南京理工大学的万莹、邓盛元团队通过多种DNA四面体的串联复用,探索了该结构在生物标记和信号传导方面的潜力,有关成果发表在Analytical Chemistry 上。
DNA结构框架的出现提升了变构事件的拓扑格局,不再局限于经典的一维双链杂交和二维发夹配对。借助该优势,化学家们如今已可设计出全核苷酸骨架的人工制品,如复杂的剪纸图案、精致的星形和旋转体等;并进一步实现机器人般的操控,使其按指令以亚纳米级精度运作。在所有奇特的创造中,DNA四面体摒弃了非正则基元(如三联体、Holliday结、G四分体、i-motif等),以极简风格成型;这一高对称柏拉图多面体不仅构造明确而且建构过程倾熵,还兼具几何刚性,后者更赋予了它形状持久性。不单如此,人们还开发出了千变万化的方案来编码棱边或修饰其顶点,将这个精致几何构造转变成一个足以应付各类场景的实用工具。典型如金刚石到四面体的互变异构,使荧光原位杂交(FISH)缔合更紧密、分析更灵敏;而对四面体顶点区的改造可缓解笼面张力,促成开普勒式的嵌套载体,实现毋须转染的控释。
除了上述被广泛报道的在体诊疗应用外,DNA四面体还具有另一特性,即在生理条件下对表面化学的重塑。当异质界面需要有序的氢键网络时,这就显得尤其有用。一方面,单个DNA四面体作为凝聚的阴离子团,通过悬垂、吸附,有效地提高了聚合物的低临界溶解温度(LCST),这有利于维持高分子的自然状态;其次,四面体自身能抵御多种离液剂的水合破坏,其不易压制的表面电位适宜充当难被生物污染、又生物相容的基底。这些优点使DNA四面体成为生物器件的重要组成部分。实际使用中,它以4条单链为原料自动装配,通过3个Au−S键在底面似金字塔般矗立成稳健支架,最终让外延识别获得取向序的一致,这在一定程度上胜过自发倾斜的光刻DNA微阵列;而更大的占位也使捕获探针的“pull-down”效率得以提升,更不需做非特异性吸附防护,总体令DNA四面体够格成为POCT快检的备选基材。
鉴于前人已经对DNA四面体的界面性质做了相当广泛的报道,本工作的着眼点转向其在电化学核酸芯片检测中的示踪和信号传导潜能探索。如图1所示,一对四面体用于夹捕目标分子,其上拉链式循环接驳另一对生物素化四面体,形成聚四面体链,最后以之为模板轭合辣根过氧化物酶。如此保证了载体的同型性、均一单标率和高负载量(图2),促成良好的电子传递链条,从而极大增敏了电催化信号,使对非小细胞肺癌相关miRNA的检测限下探至艾摩尔、动态范围达7个数量级!该设计简易而性能优于传统的杂交链反应扩增(HCR),整体模型综合展示了DNA纳米结构在生物传感中的灵活性和多任务才能,或可充当qPCR及Northern blotting分析技术的补充手段。
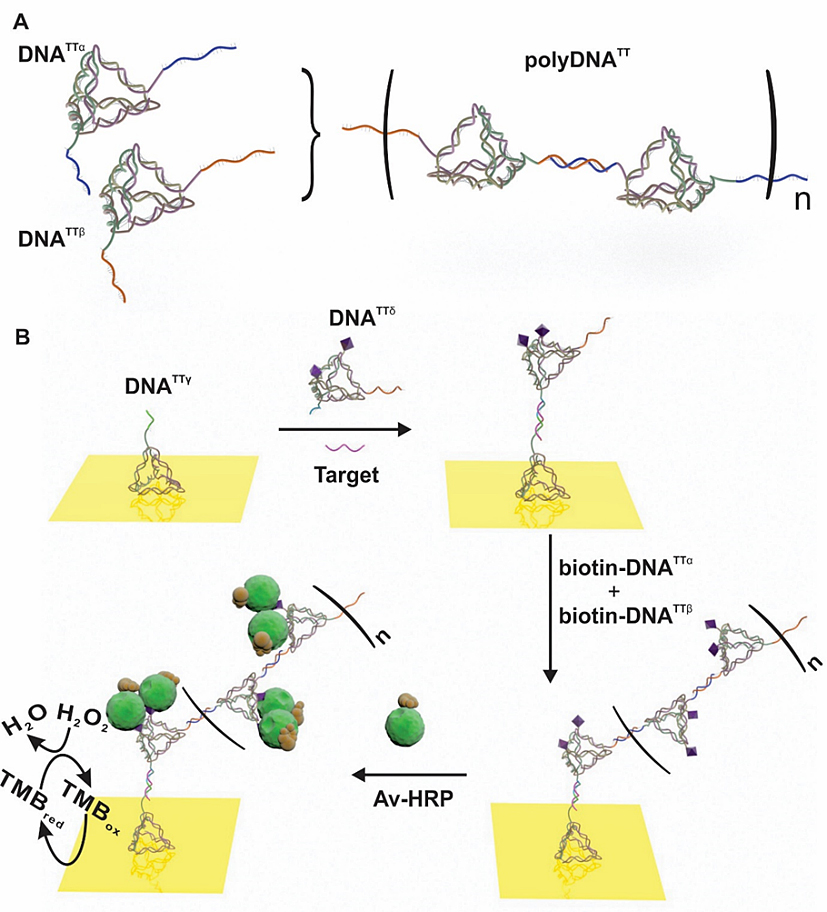
图1. 示意图:(A) 双四面体扩增子交替形成DNA结构超链接;(B) 多四面体复用实现靶标识别和检测。图片来源:Anal. Chem.
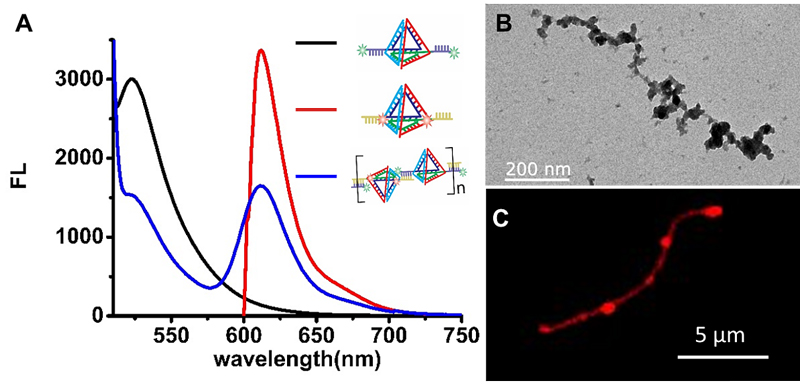
图2. (A) 四面体相互作用的光谱表征;和单根DNA四面体拉链的(B)透射电子显微形貌及(C)激光共聚焦显微成像。图片来源:Anal. Chem.
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Zippering DNA Tetrahedral Hyperlink for Ultrasensitive Electrochemical MicroRNA Detection
Ying Wan, Huan Wang, Jinyu Ji, Kai Kang, Meng Yang, Yaqi Huang, Yan Su, Kefeng Ma, Longyi Zhu, Shengyuan Deng
Anal. Chem., 2020, DOI: 10.1021/acs.analchem.0c03553
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
“光拉链”可控激活DNA纳米机器用于细胞内miRNA精准成像 2020-06-06
-
DNA四面体作为支架调控酶级联催化效率用于电化学灵敏检测DNA 2019-06-13
-
基于上转换纳米粒子参与DNA杂化累积-ICPMS高灵敏检测miRNA 2018-12-15
-
基于DNA四面体结构的分子信标用于活细胞内肿瘤相关mRNA的检测 2016-02-29
-
Ultrasensitive fluorescent detection of telomerase activity based on tetrahedral DNA nanostructures as carriers for DNA-templated silver nanoclusters.Analytical and Bioanalytical Chemistry (IF 3.8) Pub Date : 2022-01-17 ,DOI:10.1007/s00216-022-03883-1Wenting Cheng,Liangliang Xiang,Khan Adeel,Jianchun Zhang,Ying Sun,Zhaoli Zhang,Jinlong Li






































 京公网安备 11010802027423号
京公网安备 11010802027423号