化学的助攻:Nature Chem.综述生物药物给药系统的材料和方法
不得不承认,近年来在医药领域生物药物已经完全抢了化学药物的风头,因其高效性和高选择性而备受青睐,每年销售排行榜中前几名都被生物药物所盘踞,如2015年的药物销售额前十名就有七个生物药:

表格来源:科技导报
这里说的生物药物(biological drugs or biologics),主要包括通过重组技术用哺乳动物、细菌或酵母细胞生产出的多肽或蛋白质,因具有高效性和高选择性成为现代药物中的宠儿。但生物药也不是十全十美,与小分子化学药相比,除价格相对昂贵外,生物药物还有以下问题:(1)在胃肠道内稳定性低而吸收差,导致生物利用度很糟糕,几乎无法口服给药;(2)组织渗透能力有限,还可能引起不必要的免疫反应;(3)在组织和血浆中容易被蛋白酶降解,导致半衰期很短(表1)。

表1 数据来源:Nature Chemistry
幸运的是,药物传递系统的进展和生物药物工程珠联璧合,解决了生物药的给药问题,改善了生物药的吸收、稳定性和靶向性(表2)。丹麦奥胡斯大学的Alexander N. Zelikin和爱尔兰都柏林圣三一学院的Carsten Ehrhardt、Anne Marie Healy在Nature Chemistry撰写了综述性论文,介绍了生物药物给药系统的材料和方法,并讨论了这个领域的前景。(Materials and methods for delivery of biological drugs. Nature Chem., 2016, 8, 997-1007, DOI: 10.1038/nchem.2629)

表2 数据来源:Nature Chemistry
用于生物药物给药的材料
说到生物药物给药的材料,获FDA批准上市的骨移植制剂Gem 21S和Infuse是很好的例子。二者用于牙周骨再生,已经取得了商业上的成功。Gem 21S包含作为骨组织再生基质的磷酸三钙(TCP)和生物药血小板源性生长因子,后者能帮助新生成的骨组织血管化,为组织再生提供充足的血液供应。Gem 21S是生物药物给药材料在组织工程中应用的很好例子,组织工程是生物医学一个很重要的分支,在其中,生物材料有着广泛的应用。要注意的是,除了用于组织工程中的局部植入物,这些生物材料也同样可用于生物药物的系统性给药。
生物可降解有机聚合物
从1976年Langer和Folkman成功实现聚合物作为大分子药物载体的报道起,生物可降解有机聚合物应用在生物药物的给药系统中已有近40年的历史。这些聚合物可被用作组织工程中的基质,或者制成薄片和纳米/微米颗粒用于药物传递。可水解的聚合物如聚酸酐(poly(anhydrides))、聚原酸酯(poly(orthoesters))、聚酯(polyesters),它们的降解时间可设计,短至数秒,长达数年,非常适用于药物传递系统。其中最常见的有聚乳酸-羟基乙酸共聚物(poly(L-lactic-co-glycolic acid),PLGA)和聚己内酯(poly(caprolactone),PCL)(图1)。有机聚合物作为载体,固载药物大部分是小分子化合物和短链多肽,其释放分为药物被动扩散(多孔材料)和载体材料的溶解/侵蚀。但是由于生物药在生产、贮藏和填埋植入过程中的稳定性问题,生物可降解有机聚合物的应用受到了限制。目前市面仅有1款生物药Nutropin(出自Genentech/Alkermes)使用这种技术,这是一种肌肉注射的基于PLGA微球的重组人生长因子缓释剂。尽管如此,这种策略的生物药物给药系统目前仍然备受关注,未来仍可能做出突破。
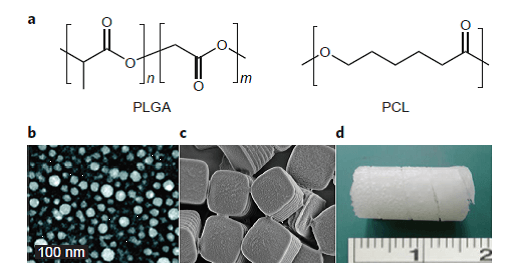
图1. 生物可降解聚合物用于生物药的控释制剂。a. PLGA和PCL因降解速率可调节,可作为需要植入体内几年的填埋型药物的辅料。现在,物质颗粒大小已不是制约因素,按形态可分为b纳米颗粒,c微球,d宏观尺度物体。图片来源:Nature Chemistry
水凝胶
水凝胶是另一种重要的生物药物缓释/控释制剂载体,它具有三维的网状聚合物结构,亲水聚合物链锁定了大量的水,与人体的软组织类似。所有水溶性的聚合物都能形成水凝胶,其中聚乙二醇PEG因溶剂化效应和表面作用最小,在生物药物中的聚合物中被称为“黄金标准”。另一种天然的大分子多糖,模拟了细胞间的基质,也是种流行的水凝胶材料。
水凝胶的生物降解也可预先设计,可控制为聚合物骨架降解(基于生物聚合物的水凝胶)或网络节点的降解(基于酯结构的水凝胶)。水凝胶除了可以被用于组织工程基质支持细胞生长之外,还能被用做可注射的剂型,通过注射器注入体内并在注射点迅速凝胶化。
非反应型水凝胶基质中载药的释放取决于溶质的粒径和凝胶网孔的尺寸,因此载药颗粒越大,网孔越密集,药物溶出越慢。生物药物,例如生长因子,还可以通过反应以共价键结合在水凝胶基质中,以控制药物释放。
水凝胶由于其机械性能(如弹性)可调至与人体组织相匹配,因而非常适合用于组织再生。将细胞工程与水凝胶结合起来,也许是生物医学研究的一条光明之路。
表面涂层
在组织工程中,除了将生物药物整合入可降解基质,还可以将它们涂覆在生物材料的表面,这可以通过多层聚电解质材料来实现(图2)。使用合成或天然的聚电解质材料形成涂层的过程可以全部以亲水的形式完成,这可以避免破坏那些“娇贵”的生物药。可通过表面涂层结合的药物有:生长因子、BMP-2、凝血酶和胰岛素。与水凝胶类似,多层涂层的膜高度亲水,还能控制机械性能(如弹性)以控制细胞粘附和增殖。
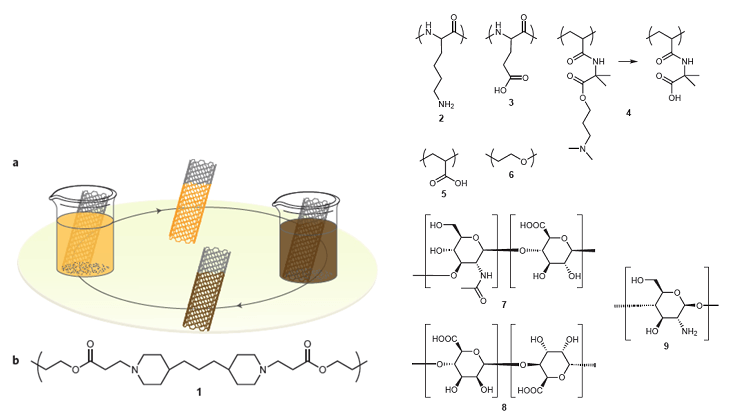
图2. 表面涂层。依次在聚合物薄膜上层层沉积生物药,便于工程控制和定位,特别是用于组织工程和再生医学。a. 下垫面聚合物从溶液中吸附药物到材料表面,依靠最初的互补相互作用(如聚阳离子-聚阴离子,供体-受体的氢键作用),表面性质因此颠倒,反复循环几次,可以得到合适的涂层厚度。而且通过吸附,载药被固定在薄膜上。b. 生物可降解材料包括:1 聚酯;2 生物可降解非天然多肽聚赖氨酸;3 聚谷氨酸;4 电荷转移聚合物;5 氢键供体聚丙烯酸;6 聚乙二醇;7 多糖透明质酸;8 聚海藻酸;9 壳聚糖。图片来源:Nature Chemistry
多层涂层还有另外的优势,通过控制涂层的形成可以控制生物药所处位置的“深度”,甚至可以控制两种及更多种药物分布于不同的位置,这在组织工程中尤其重要,可以实现在特定时间点释放特定的生长因子。
高分子缀合物
将生物药物与高分子连接起来形成高分子缀合物,是目前延长生物药的体内半衰期最成功的策略之一(图3),现在已有药物上市。与高分子缀合带来多种益处,例如降低肾脏中的清除作用,减少蛋白酶降解,还降低了免疫原性。目前所用的高分子主要是还是PEG,第1个PEG化的蛋白在1990年被美国FDA批准上市,即PEG化的门冬酰胺酶。而目前市场上的生物药高分子缀合物,除了一个日本药物之外,其余全是PEG缀合物。

图3. 生物药与非离子型水溶聚合物形成缀合物。这一策略在保护生物药免于快速水解和肾脏清除方面获得巨大成功,它还降低了被免疫系统识别的可能性,从而延长了生物药的半衰期,减少给药频率。这些聚合物有图a中的PEG、PVA、PVP,其中PEG仍是选择聚合物的黄金标准。聚合物缀合有多种方法,如图b所示PEG的N-羟基琥珀酰亚胺衍生物与多肽上的氨基(如赖氨酸残基)一步键合,得到的药物可以注射给药。图片来源:Nature Chemistry
除PEG外,还有其他亲水聚合物也很有希望,如聚乙烯吡咯烷酮PVP(PVP在二战中曾作为血浆扩容剂),还有聚乙烯醇PVA,但这两个聚合物的血液滞留时间都不如PEG。此外,分子量为2-5 KDa的PEG商业可得,且只含一个与生物药发生缀合的基团,可避免交联副反应。现在的临床试验记录也能证明,制药公司现在也更青睐PEG。
多肽缀合物
PEG有众多优点,但也存在一个致命弱点,即它的生物可降解性不理想。越来越多的证据证明,多次给药后PEG长链容易在体内累积,从而导致不良反应。能在体内降解的生物聚合物也因此获得了很多关注。天然多糖类大分子,无法控制合适的分子量,也不能实现位点特异性缀合,并不适用。非天然大分子例如合成多肽则抓住了这个机遇,开环聚合反应可以控制合成多肽的分子量和分布,末端官能团可调整以直接键合生物药物。合成多肽中的佼佼者当属聚谷氨酸(PGA),可用于抗癌药物如阿霉素(doxorubicin)、紫杉醇(paclitaxel)、喜树碱(canptothecin)等的给药,而且现在已经商业可得。
另一种合成多肽PAS基于脯氨酸Pro、丙氨酸Ala和丝氨酸Ser,这项技术源于慕尼黑工业大学(TUM),现在由XL-protein商业化。生物药在重组表达时与合适分子量的PAS多肽序列同时表达(图4a),随后目标蛋白质序列按照天然构象折叠,而PAS仍然保持为非结构序列,呈中性、水溶性良好、不造成免疫效应,还能实现PEG化的效果——延长生物药在循环系统中的滞留时间。PAS与PEG最大的不同,是可以由天然蛋白水解酶分解。另一项类似技术是由Amunix开发的XTEN,它只是与PAS的氨基酸序列不同。如果非要说这两个技术最大的缺点,那就是蛋白重组表达在细菌中完成,这让一般的化学实验室有些难以掌握。

图4. 重组技术构建的生物药衍生物具有显著延长的血液滞留时间。a. 可以构建一个表达质粒,融合表达目标蛋白和非结构多肽PAS,目标蛋白按天然构象折叠,而PAS序列形成一个无规卷曲,增加了整个融合蛋白流体力学体积,从而延长了生物药的生命期。b. 生物药还可以利用重组技术与XTEN蛋白、白蛋白、免疫球蛋白的Fc片段等融合,从而延长生物药的血液滞留时间。图片来源:Nature Chemistry
白蛋白和Fc片段融合
最常用的延长生物药物循环滞留时间的天然蛋白质分子要属白蛋白(albumin,Alb)和免疫球蛋白(immunoglobulin,Ig),它们在血液中的滞留时间可以长达2-3周,远高于具有相当分子量和流体动力学半径的合成高分子。将生物药与白蛋白或免疫球蛋白Fc片段融合表达,可以借助二者的生理学特点,延长整个融合蛋白在血液中的滞留时间。这项技术成功应用在多种上市药物,例如GSK生产了Albiglutide,一种与白蛋白融合的GLP-1多肽二聚体。这项技术最大的优势是得到的表达产物就是终产品,不再需要进一步修饰。与合成高分子相比,白蛋白化和免疫球蛋白化的药物完全生物兼容且可生物降解,并且容易调控(图5a)。
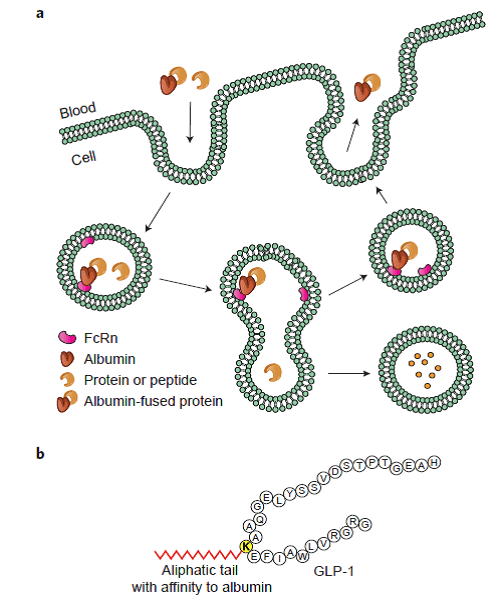
图5. 白蛋白和免疫球蛋白的生理循环。a. 融合蛋白利用白蛋白和免疫球蛋白的生理循环避免被降解和清除。b. 白蛋白可以与疏水性溶质非共价结合,通过给多肽类药物和胰岛素加上一条疏水尾巴,与体内的白蛋白结合,延长半衰期。图片来源:Nature Chemistry
另一种使用白蛋白做为生物药物载体的策略,利用了白蛋白倾向于结合疏水性溶质的特性。例如,诺和诺德(Novo Nordisk)将疏水的脂肪链连接到蛋白质如胰岛素或多肽激素如胰高血糖素样肽(GLP-1)上,得到的缀合物都可以与白蛋白结合,从而延长了半衰期,免于蛋白酶水解和肾脏清除(图5b)。依靠这项技术的GLP-1每日注射剂型liraglutide已经成功上市,而更优的每周注射剂型semaglutide已经完成了二期临床试验,这足以证明这一技术的强大。
非侵入性给药途径
在筛选给药途径时,必须考虑到大部分生物药物分子较大、易聚集和降解的特点。生物大分子的渗透性差,难以穿过人体内天然屏障,如皮肤、胃肠上皮等,而且口服给药途径会导致生物药物在胃肠中的降解,因此,绝大部分生物药均是注射给药。对需要经常用药的患者来说,注射给药相当痛苦,患者渴求非侵入性给药,早在1923年患者就希望胰岛素能够口服给药。除口服外,还有口腔含服、经皮给药、经鼻给药、经肺给药等途径在研究中。它们的优缺点如图6所示。

图6. 非侵入性给药途径,红色为缺点,绿色为优点。图片来源:Nature Chemistry
蛋白质水解是口服生物药的大挑战。解决方法之一是与蛋白酶抑制剂复方,但这不会从根本上增加生物利用度;之二是与聚合物缀合,屏蔽蛋白酶的降解作用,如Nobex/Biocon开发的口服胰岛素HIM2,但不幸的是它的人体生物利用度很低(低于1%,与皮下注射胰岛素相比),这抵消了降解减少带来的好处。除蛋白酶的水解外,肠道的上皮细胞层覆盖了一层厚厚的凝胶状粘液,粘液不断在肠道表面分泌出来,也成为生物大分子吸收的大障碍。应用粘膜粘着剂,延长生物药物在粘液上的粘附,为吸收争取了宝贵时间。粘膜粘着剂有多种,包含阳离子聚合物(壳聚糖)、阴离子聚合物(聚丙烯酸)、硫醇化材料等等。粘膜穿透材料的出现,挑战了粘膜粘着剂的地位,例如PEG包裹的纳米颗粒。作为一种与粘液粘附性很低的“不粘型”聚合物,PEG表面电荷呈中性,分子量不超过2000 Da,能帮助粒径不超过500 nm的纳米颗粒“穿越”粘膜。KALA Pharmaceuticals优化这种技术,并将其用于多种药物的传递,也很有希望用于生物药物。
即使成功躲过了蛋白酶的降解和粘液的阻挡,生物药物的生物利用度依然很低,这是因为生物药物或药物载体要穿透胃肠道进入血液循环,难度依然很大。为提高生物利用度,策略之一是利用受体-配体这种高亲和度和特异性的相互作用。为药物或药物载体装配一些特定受体的配体,那些受体在人体中起吸收必需营养物质或转运特殊蛋白质的作用,例如维生素B12和FcRn受体。另一种策略是使用渗透增强剂,作用于紧密结合肠上皮细胞,暂时增强跨膜运输。渗透增强剂包括离子螯合剂、表面活性剂、阳离子多糖壳聚糖等。还有另一种更成功的方式,即通过增加跨细胞转运能力来提高生物药的吸收。应用商业可得的一些亲脂性分子(如带电或中性的表面活性剂、胆汁酸及其盐或酯),暂时增加细胞膜的渗透性(表3)。这个策略已成功应用在含服给药和经鼻给药途径中。例如CPEX Pharmaceuticals公司开发的经鼻给药胰岛素药物Nasulin,用环十五内酯增强渗透性,尽管这个药物在二期临床实验就宣告失败。Aegis Therapeutics利用中等链长的烷基糖苷类化合物,将降血钙素的经鼻吸收生物利用度从6%提高至36%。现在这个领域还有很多提升空间,许多低毒高效的分子都可作为渗透促进剂,它们的两元或三元混合物还有协同增效的效果,有望进一步促进生物药物给药。

表3 数据来源:Nature Chemistry
增加生物大分子本身的亲脂性也能增加其渗透性,例如通过可逆缀合或非共价结合将疏水性化学基团装配到生物大分子的外部。这一策略的成功案例当属Emisohere的Eligen技术,它使用N-[(2-羟基苯甲酰)胺基)]辛酸钠(SNAC)与生物药物非共价结合,通过加强肠上皮细胞膜的流动性和药物及载体的跨膜运输,增加药物在胃肠道的吸收。药物与SNAC非共价结合,所以二者亲和力低,进入血液后就可释放生物药物,发挥药理功能。前文提到诺和诺德已经完成了二期临床试验的semaglutide,正是使用了这一技术。其他生物药物,例如胰岛素、降钙素、甲状旁腺激素都有望采用此类技术提升生物利用度。
经肺给药
胰岛素被发现后不久的1924年,就有经肺给药的报道。肺泡具有较高的表面积,同时蛋白水解酶含量少,适宜生物大分子的快速吸收,可吸收的生物大分子分子量可高达40 kDa。在过去的20年里,生物药物吸入给药取得的巨大进步。不过,并不是所有的生物药物都适合经肺吸收。为顺利通过口咽部,气雾剂颗粒的空气动力学直径不能大于5微米;为顺利到达支气管和肺泡,气雾剂颗粒的空气动力学直径不能大于3微米。大于6微米的颗粒,容易撞击口腔或咽喉并被直接咽下,而小颗粒物质(100纳米到1微米)容易随着呼气排出。第一个经肺给药的重组蛋白制剂是人脱氧核糖核酸酶,用于治疗囊性纤维化病(cystic fibrosis)。胰岛素是经肺给药研究的大热门,第一个被美国FDA批准上市的胰岛素吸入剂是Nektar/辉瑞(Pfizer)的Exubera,但几个月后因销售额远低于预期而退市。旋即赛诺菲(Sanofi)/MannKind的胰岛素吸入剂Afrezza获准上市,它应用了MannKind的Technosphere技术,使用专利辅料FDKP(bis-3,6(4-fumarylaminobutyl)-2,5-diketopiperazine)可自组装为微粒,它的生物利用度为33%,大概是Exubera的两倍,而且在Afrezza中胰岛素以单体形式被吸收,比一般的六聚体的吸收和起效都更快。不过Afrezza的销售成绩一直不让人满意,赛诺菲最近也终止了和MannKind的合作。另一种胰岛素吸入剂Dance-501正在临床研究中。
经皮给药
经皮给药(或透皮给药)系统,药物以一定的速率通过皮肤,经毛细血管吸收进入体循环而产生药效,可产生持久、恒定和可控的血药浓度,使因体内新陈代谢迅速而半衰期很短的药物活性提高,避免肝脏的首过效应和胃肠道因素的干扰,而且患者可自己使用,因此经皮吸收一直是个令人兴奋的领域,特别是对于生物大分子药物。不过,皮肤的最外层角质层连亲水性分子都透不过,更别提蛋白质、多肽等大分子了。但尼古丁和止痛药的透皮贴剂,目前已经十分成功。渗透促进剂在透皮贴剂中也很流行,这在小分子化合物透皮给药系统广泛应用,生物大分子中的应用还寥寥无几。微针(microneedle)的出现给生物大分子经皮给药带来了曙光。微针通常装配成阵列,无数微针穿过角质层透过皮肤,但不深入组织,不会出血也基本无痛,很受患者欢迎。
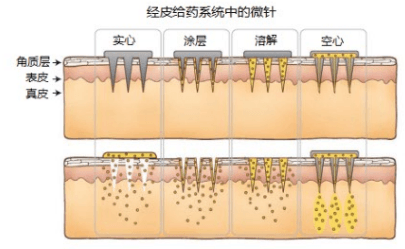
图7 生物药物的经皮吸收。微针可以是实心的,暂时穿过不渗透的皮肤,并释放药物。表面有生物药物涂层的微针,针头处沉积药物,并在接触的位置释放。可溶解针头,包括载药基质材料,随着针头溶解,药物释放出来。中空的空心微针载药后兼具注射剂和透皮贴剂的优势。图片来源:Nature Chemistry
生物药物的微针给药如图7所示。生物可降解材料如PLGA或水溶性聚合物,沉积在针头处逐渐崩解和释放载药。PVP和PVA也是制作微针的理想材料,这两种聚合物已经广泛用作药物赋形剂,还有蛋白质冷冻保护效果,可在微针制备过程中稳定生物药物。Zosano Pharma已经完成了甲状旁腺激素(PTH)微针给药的二期临床试验,他们的胰高血糖素(glucagon)微针给药的二期临床试验正在进行中。甲状旁腺激素微针给药正处于二期临床试验的还有Corium International的MicroCor和Radius的Abaloparatide-TD。
结论和展望
毫无疑问,在生物药物给药系统中涌现了多种化学手段,并获得了成功。但让人有些挫败感的是,能上市的新剂型太少了,就算成功上市,有些也因为一些非科学的原因苦苦挣扎甚至退市,胰岛素吸入剂就是个典型的例子。
不过,药物的销售成绩如何、市场推广做的好不好、药企内部如何取舍……这些非科学的因素,化学家们很难影响。化学家还是应该着眼于生物药所面临的科学挑战。现在,保持生物药在血液中活性的技术,要比将药物带入循环系统的技术更成功。这也就是说,发展可靠的生物药非侵入性给药技术是当前最大的挑战。另外,口服生物药的生物利用度太低,解决这个问题是个重要的任务。此外,提高生物药在药物载体中的稳定性,特别是缓释控释给药的情况下,也是个挑战。最后,想办法提高生物药物剂型的储存稳定性,减少运输及流通的成本(比如在流通过程中避免使用“冷链”),让公众更容易获得,这对于生物药取得商业上的成功非常重要。
化学家还需要做出更多的努力,给生物药这个“大牌前锋”更多的助攻!
http://www.nature.com/nchem/journal/v8/n11/full/nchem.2629.html
