有机小分子催化的不对称插烯Pinacol重排反应
Pinacol重排是指在酸性条件下基于碳正离子机理将1,2-二醇转化为酮类化合物的反应。然而,该反应的不对称催化由于以下两个因素而具有很大的挑战:首先,如何控制在酸性条件下只生成一个类型的碳正离子中间体。其次,高活性平面碳正离子中间体潜手性面的识别。为了避开这些困难,许多Semipinacol重排应运而生。虽然这种替代转化也有很好的合成价值,然而底物结构上的限制使得Pinacol重排反应的改进很有必要。瑞士洛桑联邦理工学院(EPFL)的祝介平(Jieping Zhu)教授(点击查看介绍)长期以来专注于手性磷酸(CPA)催化领域的研究,他的课题组最近报道了手性磷酰胺催化的插烯Pinacol重排反应,成功的将1,4-二醇转化为手性的β,γ-不饱和酮类化合物(Scheme 1)。第一作者为Hua Wu博士。(Organocatalytic Enantioselective Vinylogous Pinacol Rearrangement Enabled by Chiral Ion Pairing. Angew. Chem. Int. Ed., 2016, DOI : 10.1002/anie.201609911)
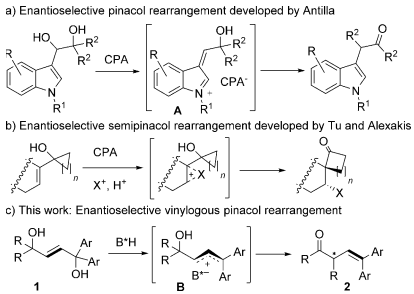
Scheme 1. 手性Brønsted酸催化的Pinacol重排。图片来源:Angew. Chem. Int. Ed.
首先,作者选择底物1a对条件进行了筛选,包括催化剂、溶剂、温度等参数。在室温条件下,使用甲苯作为溶剂,筛选了7种手性磷酸催化剂3a-3g(Table 1, entries 1-7),其中催化剂3f表现出最好的催化选择性,以97%的产率和38%的对映选择性得到产物2a(Table 1, entry 7)。在相同条件下,把温度降低到-20 ℃,产物对映选择性增加到56%(Table 1, entry 8 vs. 7)。随后,在-20 ℃条件下筛选了一系列的溶剂,MTBE表现出最高的对映选择性(Table 1, entry 15)。而当尝试进一步降低温度到-40 ℃时,产物对映选择性保持不变,产率稍有下降(Table 1, entry 16)。反应体系中添加分子筛对反应ee值提高也有帮助(Table 1, entry 13 vs 12)。综上,最佳反应条件是:3f作为催化剂,MTBE作为溶剂,分子筛作为添加剂,-20 ℃作为反应温度。
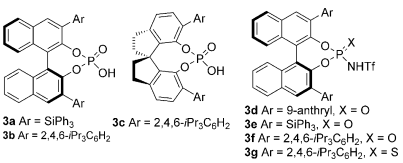
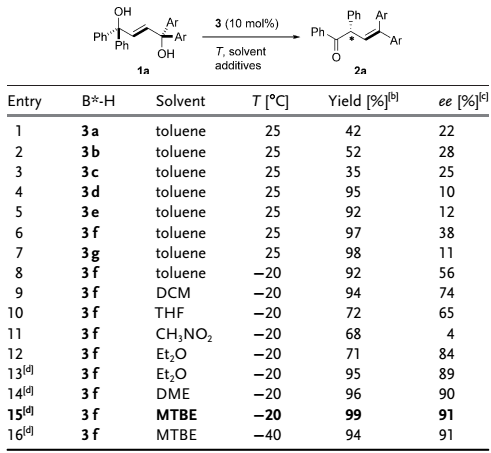
Table 1. 条件筛选。图片来源:Angew. Chem. Int. Ed.
在最佳反应条件下,作者对底物的底物普适性进行了考察。作者首先固定Ar为对甲氧基苯基,考察了R取代基。当R为芳环时,不管取代基在芳环的对位还是间位,是富电子基团还是贫电子基团,目标产物都能以中等到高收率(64-99%),中等到高对映选择性(75-96%)得到。当R为烷基取代基时,只能以41%的对映选择性得到目标产物。此外,作者还对Ar取代基进行了考察,不管是杂环还是普通芳环都能以良好的结果得到目标产物(Table 2)。

Table2. 底物拓展。图片来源:Angew. Chem. Int. Ed.
为了证明该方法的实用性,作者还对重排产物进行了一系列的衍生实验。产物2a通过还原双键得到产物9,随后9通过硼氢化钠还原以定量收率得到醇10,醇10通过酸催化发生分子内的Friedel–Crafts烷基化反应得到四氢萘衍生物11。产物2a也可通过硼烷还原得到顺式产物7,产物7在NBS作用下发生环化反应得到多取代的手性呋喃衍生物8(Scheme 2)。
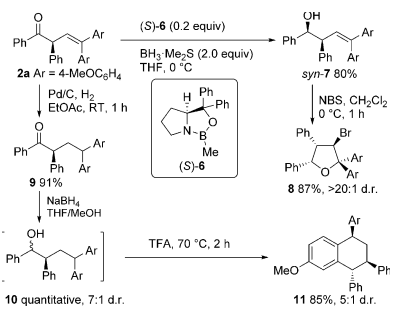
Scheme2. 衍生实验。图片来源:Angew. Chem. Int. Ed.
根据实验结果,作者提出了如下的机理(Scheme 3)。首先二醇在催化剂作用下通过过渡态C生成烯丙基正离子过渡态E,随后发生取代基迁移得到产物。磷酰胺磷氧双键中的氧原子与醇形成氢键从而达到控制手性的目地。作者认为,由于Ar是富电子芳基,因而过渡态C是优势过渡态,对过渡态E的共振贡献更大,生成的过渡态E从动力学角度来看更快。
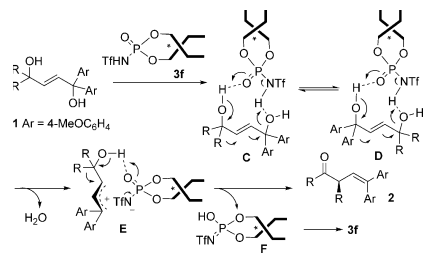
Scheme3. 反应机理。图片来源:Angew. Chem. Int. Ed.
为了验证这些假设,作者进行了一系列的控制实验(Scheme 4)。首先,使用1g作为底物,在标准条件下,在反应体系中添加乙醇,以98%的产率得到烷氧基化的产物4,这就证明了C是优势过渡态并且证明了烯丙基正离子的存在。如果是按照SN2机理,通过中间体C或者D生成目标产物,那么二者就是一个竞争关系,并且应该中间体D占优势,因为富电子取代基迁移更容易,那这样得到的就不是目标产物了,这也就简介否定了SN2机理。当作者使用顺式的二醇1v作为底物时,以98%的产率得到的是关环产物5,这说明在标准条件下,关环速度比双键通过烯丙基正离子异构化的速度更快。
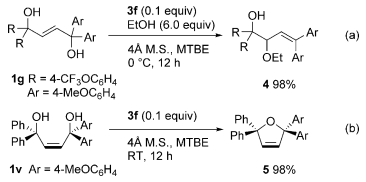
Scheme4. 控制实验。图片来源:Angew. Chem. Int. Ed.

祝介平教授在清华大学做讲座。图片来源:清华大学
总结:
祝介平课题组首次报道了有机小分子催化的插烯Pinacol重排,将1,4-二醇以高收率、高对映选择性成功转化为手性的β,γ-不饱和酮类化合物。该催化方法的实用性广泛,通过简单的衍生化反应就可以制备手性的四氢萘衍生物和四氢呋喃衍生物。
http://onlinelibrary.wiley.com/doi/10.1002/anie.201609911/full
导师介绍
祝介平教授:http://www.x-mol.com/university/faculty/2766
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
铑催化联烯插入碳碳键快速构建烯基四氢萘类骨架 2016-03-30
-
基于aza-pinacol重排策略合成Indolines/Indolenines骨架结构 2015-11-02


































 京公网安备 11010802027423号
京公网安备 11010802027423号