美女教授Doyle在JACS报道制备含放射性氟原子化合物的新方法
C-F键的构建在医药、农药以及材料领域都有着广泛的应用。我们所熟知的氟原子是19F,而其另外一个同位素18F具有放射性,是一个很好地正电子源,常被用于正电子发射计算机断层现象技术(PET),因此将18F引入到有机小分子中对于临床研究药物的代谢途径及其动力学有着非常重要的意义。然而,C-F键的构建本身就具有一定难度,在分子中引入18F中则更具挑战性,主要是因为18F试剂类型比较有限,而且18F的半衰期只有110 min。
最近普林斯顿大学的美女教授Abigail Doyle在JACS上发表了铜催化α重氮羰基化合物的H-F插入反应(Scheme 1)。使用KF和六氟异丙醇,高效构建α氟代羰基化合物。反应简单高效,能够一步大量制备含18F标记的小分子化合物,可以应用于PET示踪剂的合成(Nucleophilic (Radio)Fluorination of α-Diazocarbonyl Compounds Enabled by Copper-Catalyzed H-F Insertion. J. Am. Chem. Soc., 2016, 138, 10802-10805, DOI: 10.1021/jacs.6b06770)。
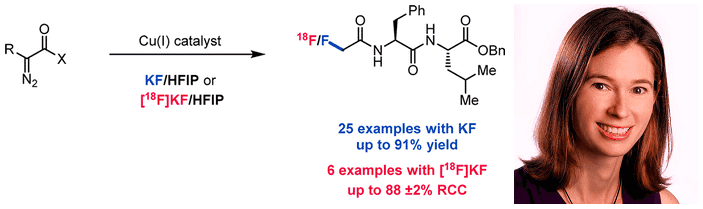
Scheme 1. 图片来源:J. Am. Chem. Soc.以及Doyle课题组网站
α-氟代羰基化合物广泛存在于药物分子中(Scheme 2A),文献报道的制备α-18F羰基化合物的方法需要将底物预官能团化,反应步骤较长,产率低(Scheme 2B)。Doyle教授使用金属铜作为催化剂,以α-羰基重氮化合物为底物,一步得到α-氟代羰基化合物(Scheme 2C)。
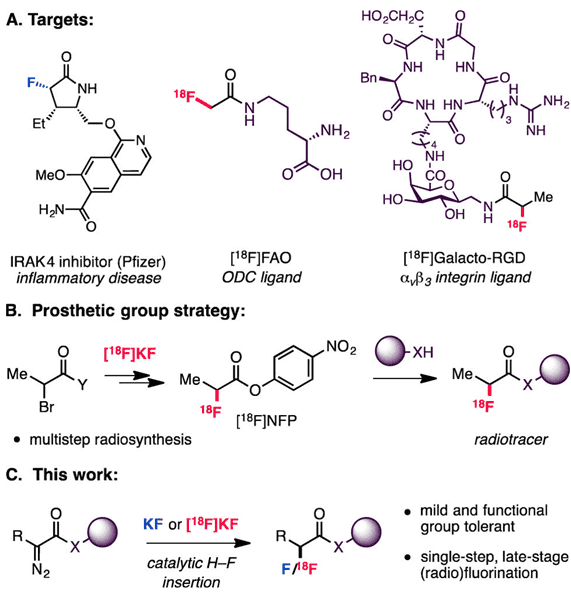
Scheme 2. 图片来源:J. Am. Chem. Soc.
多种过渡金属可以催化α-羰基重氮化合物的分解,生成金属卡宾中间体,该中间体可以进行对碳-氢键、碳-杂键以及杂(O、N、S、B、Si等)-氢的插入反应,而对H-X(X为卤素)的插入反应还没有报道。Doyle小组使用H-F或者类似H-F的试剂,以1a为底物,在铜(I)和双恶唑啉配体作用下对反应条件进行优化:当使用KF与六氟异丙醇时,能以68%的收率得到产物;使用苯甲酰氟为氟源时也能够以64%的收率得到产物,但含放射性氟源18[F]PhCOF很不易得到。反应中六氟异丙醇起到了非常最重要的作用,提高六氟异丙醇的当量可以提高反应的收率以及选择性,同时减少副产物3的生成。可能是因为增加六氟异丙醇的量能够提高KF的溶解度,或者由于溶剂效应等原因提高了KF的活性。氘代试验显示产物羰基α-位的氢原子来源于六氟异丙醇。研究小组还尝试了其它过渡金属如Rh2(OAc)4,以及其它双恶唑啉配体,反应收率未有改善(Scheme 3)。使用手性配体L1时能够得到31% ee(虽然ee值较低,但也是该反应的首次不对称报道)。
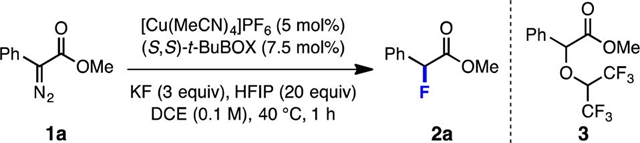
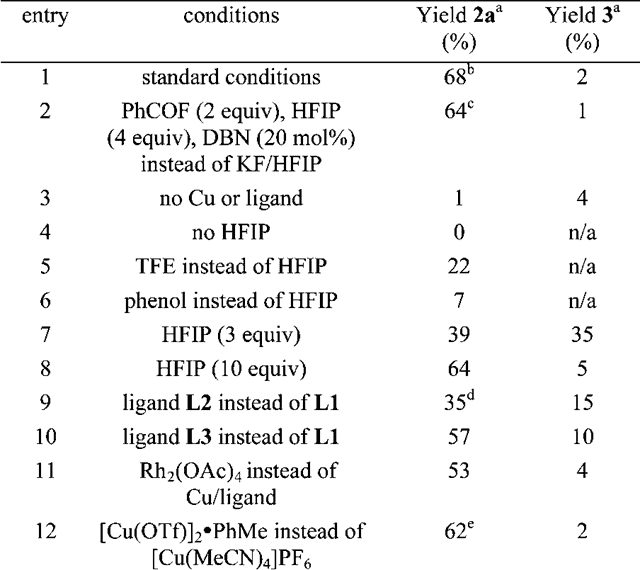
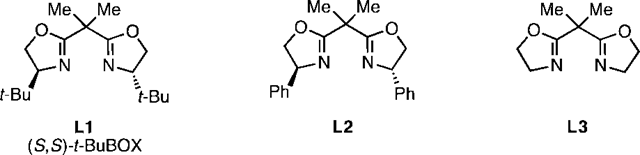
Scheme 3. 图片来源:J. Am. Chem. Soc.
随后,在最优条件下,研究小组对底物进行了拓展。芳香环上含有不同取代基时都能以中等到良好的收率得到产物(Scheme 4, 2a-2n)。含有酯、酰胺、酮类等官能团的底物以及含生物活性的多肽和葡萄糖类底物参与的反应也能顺利地得到产物(Scheme 4),α-烷基取代的底物参与的反应,主要得到α,β-不饱和羰基化合物。
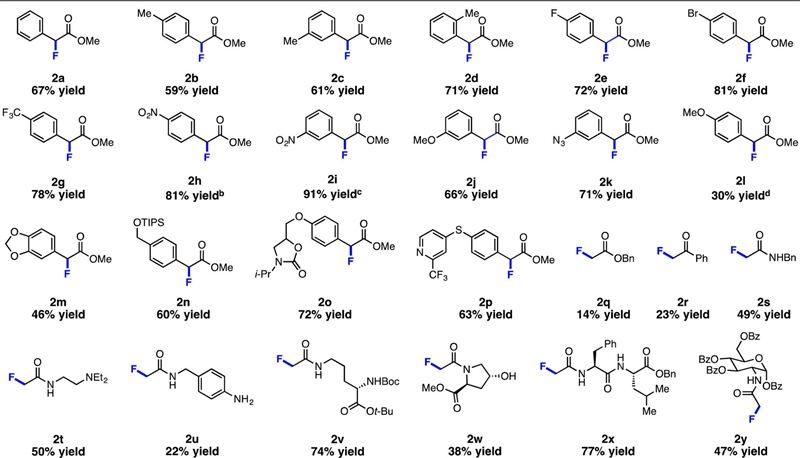
Scheme 4. 图片来源:J. Am. Chem. Soc.
随后研究小组将[18F]KF-K222应用到反应体系中,在加热到50 ℃反应10min就有80%的转化率,并以良好的收率得到产物(Scheme 5)。研究小组发现,当按照之前反应条件,使用[Cu(MeCN)4]PF6时得到产物的比放射性强度率仅为24 mCi/μmol。考虑到铜盐中的PF6-中氟负离子可能会导致放射性活度降低,研究小组将[Cu(MeCN)4]PF6 换为[Cu(MeCN)4]ClO4,比放射性强度率提高到了1300 mCi/μmol。
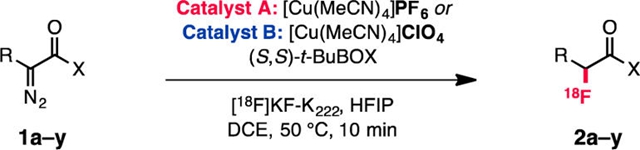
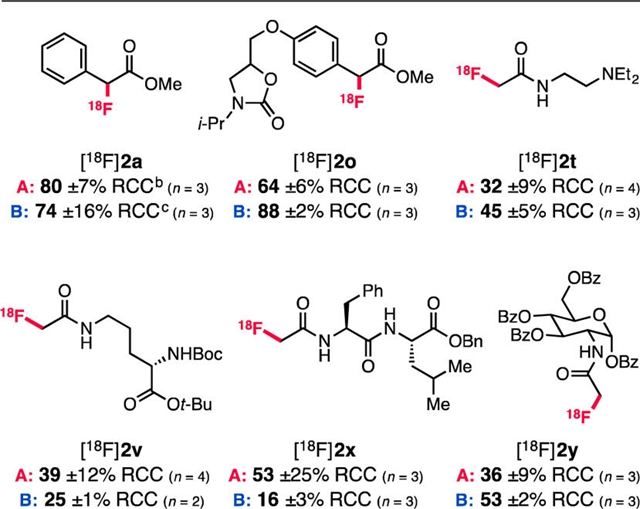
Scheme 5. 图片来源:J. Am. Chem. Soc.
总结:
Doyle教授小组报道了新的构建C-F/18F的方法,简单高效地得到了α-化羰基化合物,并且能够在具有生物活性的小分子上一步引入放射性18F,为新型PET示踪剂的合成提供了新方法。接下来研究小组可能在不对称催化方面继续研究。
http://pubs.acs.org/doi/abs/10.1021/jacs.6b06770
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号