《Nature Mater.》:癌症转移谁说了算——界面几何形状
癌症是目前人类健康的主要杀手之一。恶性肿瘤组织内部松散,一些细胞很容易逃逸出来,渗透进入血液循环从而转移到其他器官甚至遍布全身组织,并在新位点处形成新的肿瘤,这也就是谈之色变的癌症转移。当前的抗癌疗法主要目标还是除去癌细胞,如根治性手术切除肿瘤、放疗和化疗等,均可破坏恶性肿瘤及其生长微环境,不过,这些治疗方案都需要面对肿瘤转移和复发的问题。在肿瘤转移和复发过程中,占比非常小的肿瘤干细胞(Cancer Stem Cell,CSC)起到了非常重要的作用。
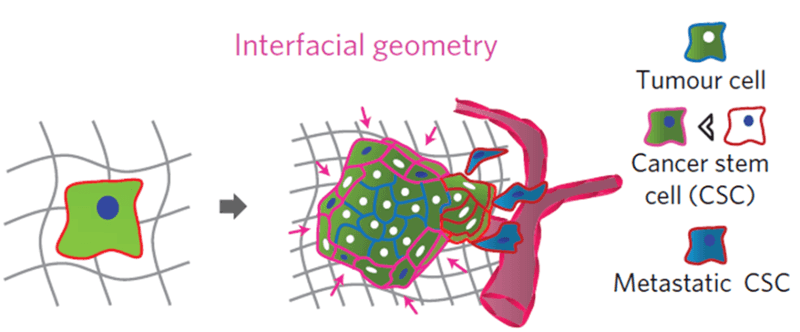
肿瘤转移模型。图片来源:Nature Materials
通常来说,肿瘤干细胞转移与肿瘤位置、外界刺激、肿瘤生长微环境等有关。最近,美国伊利诺伊大学香槟分校Kristopher A. Kilian教授领导的一个研究团队在《Nature Materials》上发表文章,揭示肿瘤组织的界面几何形状也会诱导肿瘤干细胞的形成和富集,并影响其在肿瘤组织内的分布,进而影响肿瘤的转移。(Interfacial geometry dictates cancer cell tumorigenicity. Nature Mater., 2016, DOI: 10.1038/nmat4610)
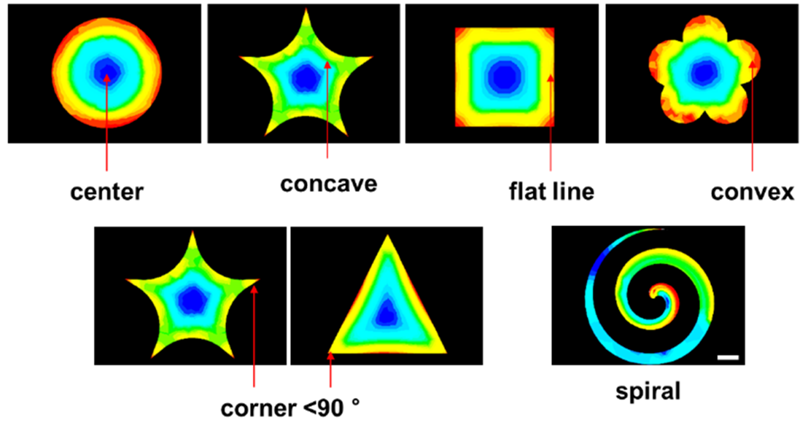
基质模型截面。图片来源:Nature Materials
研究者采用不同弹性的改性聚丙烯酰胺凝胶,通过软光刻技术制备具有不同大小和形状的二维和三维图案化微环境,用于培养黑色素瘤细胞。由于组织内部的细胞粘附可以调节组织的周长应力,他们设计了可以改变曲率及周长面积比的直线和圆环形貌。研究发现在圆环的外凸面曲率区域相比于内部凹入区域有更高的肿瘤干细胞标记物表达。他们设计了一系列的图案,包括边缘、凹凸区域等,研究肿瘤细胞群的周边界面因素的组合是如何指导细胞形成组织和表达肿瘤干细胞的标记物。结果显示,在所有的几何形状中,不同于正常的干细胞多分布在柔软、湿润的组织内部位置,高效表达肿瘤干细胞标志物的细胞多分布在图案化肿瘤微环境的边缘或外围附近,尤其是位于其凸面和转角处。
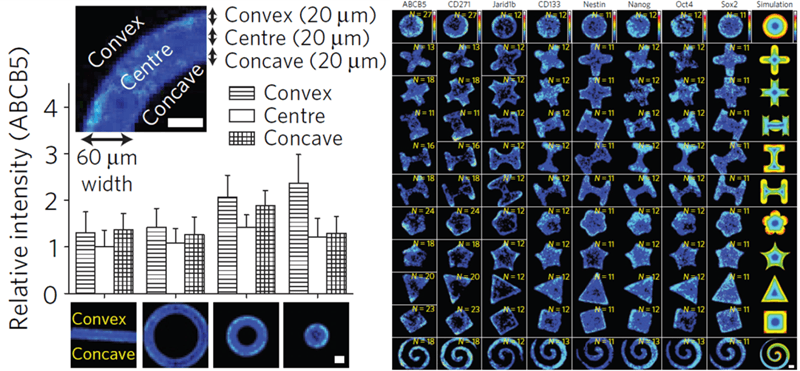
不同界面几何图案影响肿瘤干细胞标志物的表达。图片来源:Nature Materials
研究人员也对螺旋图案凝胶基质模型中的肿瘤干细胞开展了全基因组表达分析,结果表明界面几何图案可以通过调节integrin α5β1、MAPK和STAT等细胞信号蛋白的活性来调控肿瘤干细胞的形状和粘附。创伤修复和Boyden小室入侵检测实验均表明培养在3D螺旋图案基质中的细胞,其迁移和侵袭能力更强,具有更强的肿瘤转移潜能和致瘤性。研究人员随后在小鼠模型中开展了皮肤癌干细胞的测试研究,结果表明从模型环境中获取的细胞比从正常培养皿中获取的细胞更容易导致皮肤肿瘤的形成。
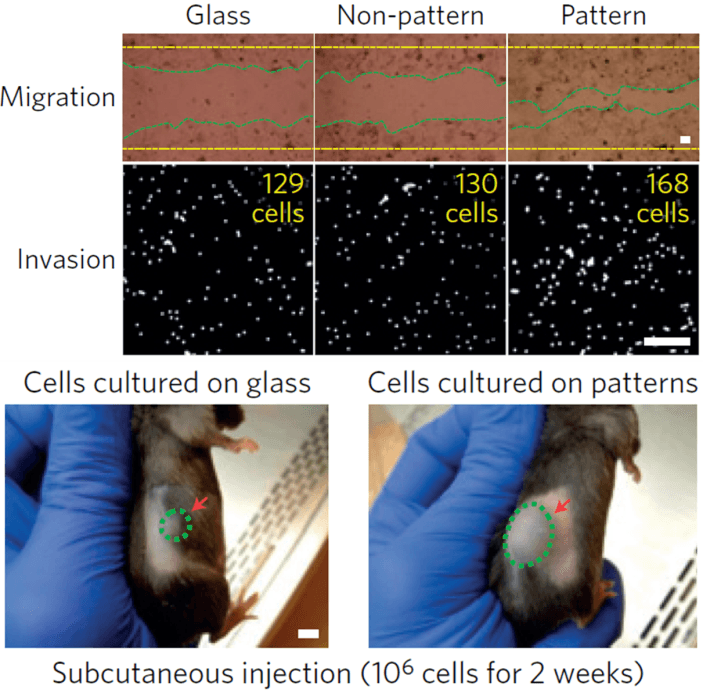
肿瘤干细胞转移和侵袭及小鼠模型致瘤性对比。图片来源:Nature Materials
随后研究人员对宫颈癌、肺癌和前列腺癌等多种癌细胞系进行了类似研究,不同种类的肿瘤干细胞均对图案化微环境产生了相似的响应。
界面几何形状在肿瘤转移过程中发挥了激活干细胞样细胞的独特作用,这一发现有助于在活检和肿瘤切除手术中指导肿瘤微环境的临床分析,在个性化治疗领域中促进特定模型设计、开发和转化的进步。
http://www.nature.com/nmat/journal/vaop/ncurrent/full/nmat4610.html
(本文由瀚海弄潮供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号