邻苯二甲醛(OPA)导向的天然未保护多肽的化学选择性环肽方法
作为生物大分子相互作用的调控因子,各种环肽化合物由于具有不同生物活性,如抗肿瘤、抗菌等,从而被广泛关注。尽管现今有多种环肽合成方法,简单粗暴且高效率的多肽环化条件依旧值得开发和研究。近来,香港大学化学系李学臣教授(点击查看介绍)课题组借助简单的邻苯二甲醛(OPA)化合物实现了天然链状多肽(含一个半胱氨酸及赖氨酸)在温和的磷酸盐缓冲溶液(PBS buffer,pH 7.4)中高效且有选择性的环化。这种基于OPA的多肽环化方法具有多功能性。如,串联天然化学连接法(Native Chemical Ligation, NCL)构建双环肽,借助N-马来酰亚胺基团(N-maleimide moiety)一锅法(one-pot manner)引入多样化的功能分子。这一研究成果近期发表在Journal of the American Chemical Society上,论文的第一作者为博士研究生张越。
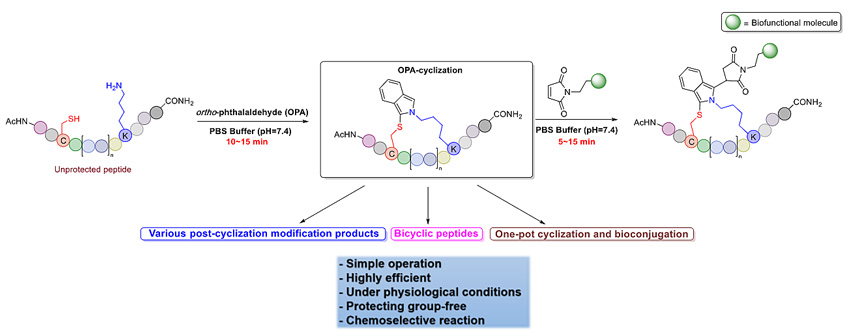
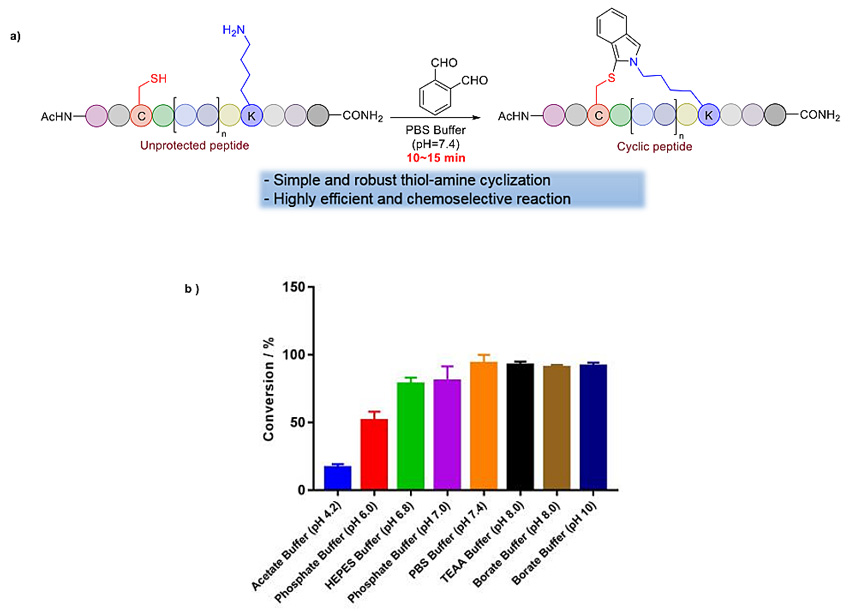
作者首先阐述了邻苯二甲醛(OPA)化合物与氨基及巯基的缩合反应最早被用来检测氨基酸的含量(Anal. Chem., 1971, 43, 880)。在2016年,香港大学李学臣教授课题组成功的使用邻苯二甲醛(OPA)与多肽中天然氨基反应实现了快速干净的化学选择性多肽氨基偶联(PT Ligation)(Org. Lett., 2016, 18, 2600)。在此基础上,作者使用含有半胱氨酸(cysteine)及赖氨酸 (lysine) 的多肽AcNH-KAAAAAACF-CONH2为底物在与PT ligation同样的反应条件(PBS buffer, pH 7.4)下进行实验。结果显示在反应15分钟后,多肽Ac-KAAAAAACF-CONH2 快速且干净的转化为异吲哚链接的环肽。作者经过条件筛选,发现此反应兼容于不同pH的缓冲液体系(HEPES buffer, pH 6.8 ~ borate buffer, pH 10)。随后作者合成了15条多肽底物用于测试此方法,结果表明不同多肽长度及位于半胱氨酸及赖氨酸之间不同氨基酸数量并不影响反应,并且其他天然侧链官能基团也不影响此环肽反应。作者对15条多肽底物的反应混合物分别进行LCMS分析检测,综合反应转化率介于90~98%之间。但是作者也同样指出,OPA环化反应无法准确区分N端氨基与赖氨酸侧链氨基,所以如果需要选择性的让某个氨基参与反应,需要对其他氨基进行的暂时性地保护。
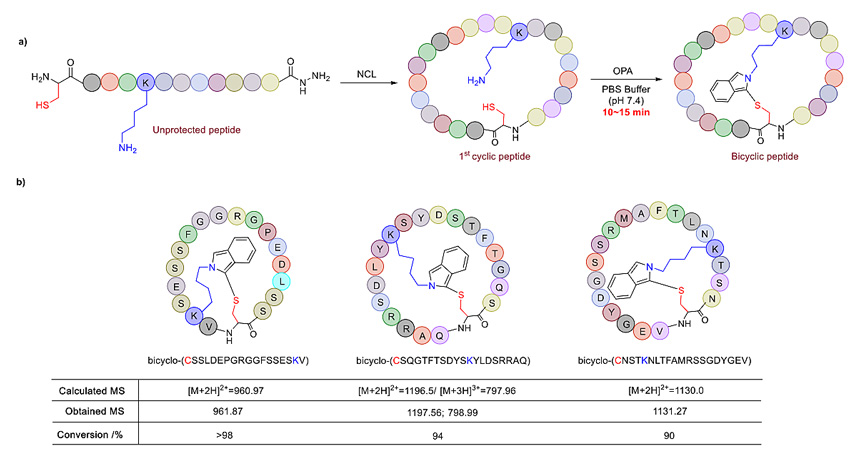
为了进一步将该反应与现有的环肽方法相串联以增加适用性,作者首先使用天然化学连接法(Native Chemical Ligation, NCL)制备环肽,NCL所形成的环肽同时含有一个半胱氨酸及一个赖氨酸。随后串联邻苯二甲醛(OPA)环肽法从而形成一个双环肽的复杂结构。基于串联NCL及OPA环肽法,作者完成了三条双环肽的合成并且经由LCMS分析得到大于90%的OPA环肽反应转化率。
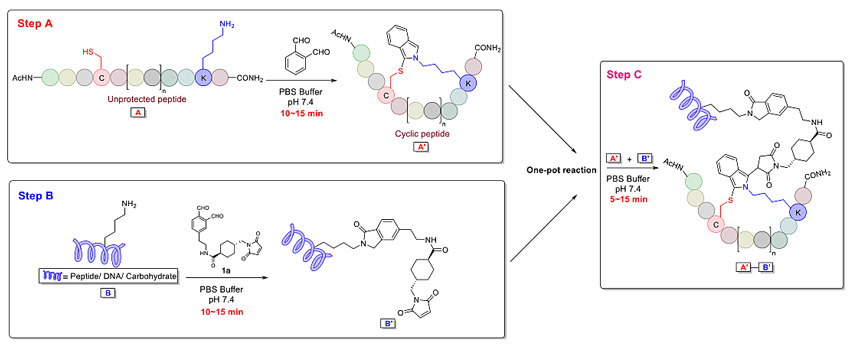
随后,作者对OPA环化后修饰进行更进一步的研究。首先发现丁炔二酸二甲酯(Dimethyl acetylenedicarboxylate, DMAC)可以和OPA环肽形成稳定的产物,随后N-马来酰亚胺基团(N-maleimide moiety)被证明也可以进行OPA环肽后修饰反应。由此作者发现可以使用此反应向OPA环肽上引入不同的功能性基团以促进环肽的多样化应用。作者选择靶向结肠癌细胞的环肽cyclo(CPIEDRPMK)进行实验,首先使用OPA环肽法合成环肽并后续以上述方法进行荧光标记。经过细胞靶向实验表明此方法可以有效的模拟双硫键来环化多肽,并同时保留多肽本身的生物活性。为了进一步增加OPA环肽法的应用,作者将OPA环肽法及环肽后修饰反应与PT ligation 相结合。此方法可以进一步在OPA环肽上引入不同的活性分子(荧光基团,糖,多肽以及修饰的DNA分子)从而极大的扩展了OPA环肽的后续应用。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Chemoselective Peptide Cyclization and Bicyclization Directly on Unprotected Peptides
Yue Zhang, Qing Zhang, Clarence T. T. Wong, Xuechen Li
J. Am. Chem. Soc., 2019, 141, 12274-12279, DOI: 10.1021/jacs.9b03623
李学臣博士简介
李学臣,香港大学化学系教授,2009年起就职于香港大学化学系,并于2018年晋升为教授。李学臣博士主要从事生物大分子(如蛋白质、多肽及多糖)的化学合成和化学生物学研究,具体内容包括蛋白质化学合成新方法研究(丝氨酸/苏氨酸连接反应,STL)、具有重要生物活性的环肽天然产物及结构类似物的合成与药物化学研究、疾病相关多糖的全合成研究、化学选择性蛋白质修饰研究等。
https://www.x-mol.com/university/faculty/7051
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号