Angew. Chem.:叔膦催化贫电子亚甲基环丙烷的开环重排
叔膦催化(phosphine catalysis)已成为碳-碳键、碳-杂键的高效构建方法,尤其在环状化合物的合成方面展示出重要的应用价值。联烯酸酯1是一类具有丰富反应性的底物分子(图1),其在叔膦作用下可转化为偶极中间体A并可与多种亲电/亲核试剂发生环化反应。陆熙炎先生的Lu's [3+2]、Ohyun Kwon教授报道的[4+2]以及童晓峰教授发展的[4+1]环化反应是其中的典型例子,以卢一新教授为代表发展的不对称叔膦催化环化反应也取得了重要进展。
西安交通大学徐四龙(点击查看介绍)课题组近年来致力于发展新的适用于叔膦催化反应的底物分子。最近,该课题组基于亚甲基环丙烷与联烯结构上的相似性,设计将贫电子亚甲基环丙烷2应用于叔膦催化的环化反应。在叔膦作用下,化合物2可望发生高共轭加成(homoconjugate addition)产生一类新的偶极中间体B并由此实现多样的化学转化(图1)。
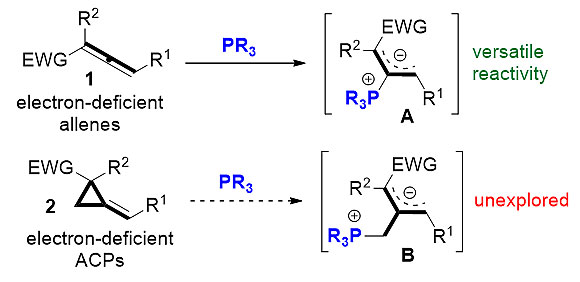
图1. 叔膦对贫电子联烯或亚甲基环丙烷的加成
作者考察了不同结构类型贫电子亚甲基环丙烷在叔膦催化条件下的转化,分别实现了三类底物控制的重排反应(图2),反应均展示出优秀的化学选择性、良好的收率及普适性。
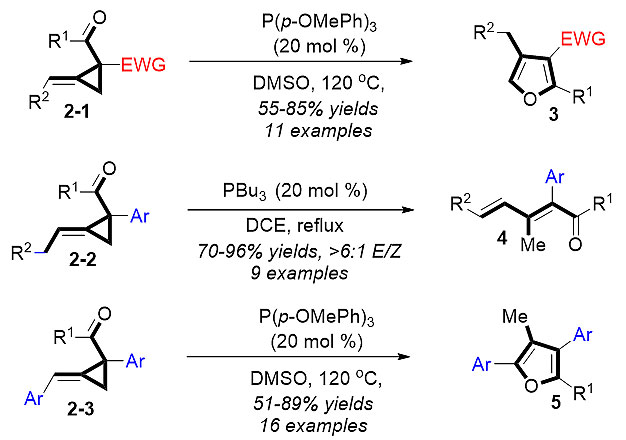
图2. 底物控制的叔膦催化亚甲基环丙烷的重排反应
在可能的机理中(图3),首先叔膦亲核进攻贫电子亚甲基环丙烷生成烯丙基鏻盐中间体B,当R1为烷基、R2为拉电子基团时,中间体B经Path A 发生SN2关环,进一步离去叔膦生成化合物3'并最终异构化生成三取代呋喃3;当R1为烷基、R2为芳香基时(Path B),中间体B经质子转移生成中间体C,离去叔膦生成二烯烃化合物4',进一步异构化生成共轭二烯酮4;当R1、R2均为芳香基团时,中间体B经Path C 发生SN2'关环生成化合物5',最终异构化生成四取代呋喃5。通过31P NMR跟踪实验进一步验证了该机理过程。
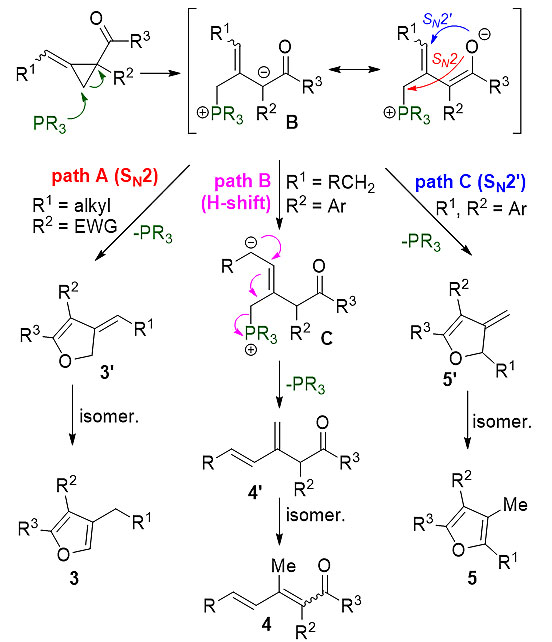
图3. 叔膦催化贫电子亚甲基环丙烷的重排反应可能机理
综上,徐四龙课题组报道了一例叔膦催化贫电子亚甲基环丙烷的开环重排反应,分别合成三、四取代呋喃和共轭二烯酮。研究工作为叔膦催化提供了一种新的底物分子,有望发展新的多样的化学转化。同时,叔膦催化亚甲基环丙烷的开环重排与以往的过渡金属催化亚甲基环丙烷的类似反应形成了鲜明对比,有助于丰富亚甲基环丙烷的反应性。
相关工作发表在Angew. Chem. Int. Ed.上,文章第一作者是西安交通大学理学院博士研究生贺馨。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Phosphine-Catalyzed Activation of Alkylidenecyclopropanes: Rearrangement to Form Polysubstituted Furans and Dienones
Xin He, Yuhai Tang, Yongzhuang Wang, Jian-Bo Chen, Silong Xu, Jianwei Dou, Yang Li
Angew. Chem. Int. Ed., 2019, 58, 10698-10702, DOI: 10.1002/anie.201903320
导师介绍
徐四龙
https://www.x-mol.com/university/faculty/49569
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
















































 京公网安备 11010802027423号
京公网安备 11010802027423号