人工智能助推新药研发
近日,中国科学院深圳先进技术研究院计算机辅助药物设计中心的袁曙光(点击查看介绍)课题组带领团队,在Cell子刊Trends in Pharmacological Sciences(影响因子 11.5)上发表题为“Advancing Drug Discovery via Artificial Intelligence(利用人工智能助推新药研发)”的综述性论文。论文的第一作者为陈显翀,通讯作者为袁曙光,第一单位为中国科学院深圳先进技术研究院。
人工智能(AI)在各行各业起着越来越重要的作用。从图像与声音的识别到无人汽车和无人机的制造,AI技术都功不可没。近年来,随着AI在计算生物学领域的突破与应用,利用AI加速新药研发成为AI应用领域的一个热门方向。传统的新药研发平均需要12年的时间和20-30亿美金的投入。光临床前期研究平均就需要花费5-6年的时间。如何加速新药研发进程,已经成为各大制药公司迫切需要解决的战略性问题。在此大背景环境下,AI在临床前新药研发中的应用优势得到突出体现。本论文作者结合自身的药物研发成功经验,系统介绍了如何利用AI来完成临床前新药创新。AI在临床前的各个阶段都发挥着举足轻重的作用,包括:药物作用靶标的预测、药物分子结合位点预测、靶标蛋白三维结构预测、计算机虚拟筛选、海量虚拟数据的构建、药物分子适应症的预测、化学合成布局、药物分子结构改造、药物毒理毒性预测、药物分子水溶性预测、以及临床前药物研发最后期的分子晶形预测等。与传统新药研发管线比,基于AI和生物计算的新药研发管线平均1-2年就可以完成临床前药物研发。
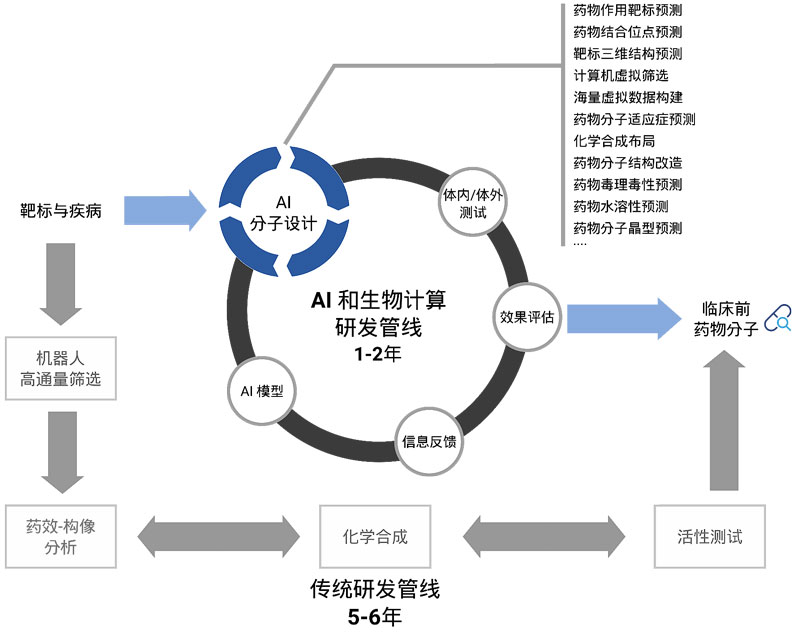
图1. 基于AI和计算生物学的药物研发管线与传统研发管线的对比
基于AI和计算生物学的研发管线,团队成员曾3年将两个临床前first-in-class新药推向临床;成功完成20多个不同药物靶标的计算机虚拟筛选;为多个孤儿受体(orphan receptor)寻找到唯我独有(me-only)的药物分子并以此确定了孤儿受体的生理功能与疾病适应症。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Advancing Drug Discovery via Artificial Intelligence
H.C. Stephen Chan, Hanbin Shan, Thamani Dahoun, Horst Vogel, Shuguang Yuan
Trends Pharmacol. Sci., 2019, DOI: 10.1016/j.tips.2019.06.004
作者简介
袁曙光,中科院深圳先进技术研究院计算机辅助药物设计中心主任、正研究员。2009年获得中科院上海有机化学研究所硕士学位。2009年10月获得欧盟玛丽居里全额奖学金资助,先后在比利时鲁汶大学(KULeuven), 波兰科学院,洛桑瑞士联邦理工学院(EPFL)完成博士学位。2013年6月获得最佳博士论文奖。近年来,袁曙光博士一直致力于GPCRs计算机模拟和基于人工智能的新药研发研究。通过全原子长时间尺度的分子动力学模拟(all-atom long time scale molecular dynamics simulation),揭示GPCRs的激活机制和小分子的特异性原理。2013年,作者首次发现了钠离子在鸦片受体(mu opioid receptor)的激活过程中的机理 (Angew Chem Int Ed, 2013, doi:10.1002/anie.201302244)。2014年,作者通过对Rhodopsin, A2AR和β2AR三个GPCRs受体的系统研究, 首次发现了GPCRs被激活的时候,在GPCRs内部能够形成连续的水分子通路 (Nature Communications, 2014, doi:10.1038/ncomms5733)。同年作者又揭示了GPCRs 形成水分子通路的开关(Angew Chem Int Ed, 2013, doi:10.1002/anie.201409679)。2015年,作者发现了鸦片受体的小分子特异性原理,系统阐述了为什么两个结构上非常相似的小分子其中一个是激动剂,而另外一个则是拮抗剂(Angew Chem Int Ed, 2015, doi:10.1002/anie.201501742)。该工作并被主编选定为热门文章。2016年,作者揭示了5-HT1A受体的立体选择性原理 (Angew. Chem Int Ed, 2016, doi:10.1002/anie.201603766)。同年,作者还发现了P2Y1受体两种不同的拮抗剂抑制机制(Angew Chem Int Ed, 2016, doi:10.1002/anie.201605147) 。2018年,作者通过分子动力学的方法,发现了GPCR药物分子的新的结合位点 (Chemical Science, doi:10.1039/C8SC01680A)。2019年通过生物计算与AI的方法,从160万个化合物出发,为Olfr73受体蛋白寻找到了17个高活性的药物候选分子(Communications Biology, doi: 10.1038/s42003-019-0384-8)。此外作者还带领团队3年将两个临床前first-in-class新药推向临床;成功完成20多个不同药物靶标的计算机虚拟筛选;为多个孤儿受体(orphan receptor)寻找到唯我独有(me-only)的药物分子并以此确定了孤儿受体的生理功能与疾病适应症。
袁曙光
https://www.x-mol.com/university/faculty/45898
课题组链接
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号