非带正电的生物纳米材料与细胞之间的相互作用
有赖于纳米技术的日益提升,纳米研究人员现在能够把不同类型的天然生物分子(例如核酸、蛋白质和脂质)组装成直径为1-100 nm的生物纳米材料,为靶向递送、基因调节、分子诊断和免疫调节等纳米医学应用奠下根基。为了在这些应用中实现最佳性能,纳米粒子必须被有效地递送至特定的器官、组织和细胞。因此,深入详尽地研究纳米材料与生物系统的基础相互作用,有助突破纳米粒子低效靶向递送的瓶颈,从而促进纳米药物的临床转化。
由于细胞膜由阴离子磷脂双分子层构成,带正电的脂质体和脂质纳米粒子具有较高的细胞膜穿透力,因此它们是递送药物分子的常用载体。然而,带正电的纳米粒子容易引起细胞毒性和免疫反应,可能有碍临床转化。相反,非带正电(即带负电或近中性电荷)的纳米粒子通常表现出较高的生物兼容性,但一般难以被哺乳动物细胞摄取。有趣的是,一些非带正电纳米粒子同时具备高生物兼容性和高细胞摄取率,两样皆为纳米药物载体的优良特点。
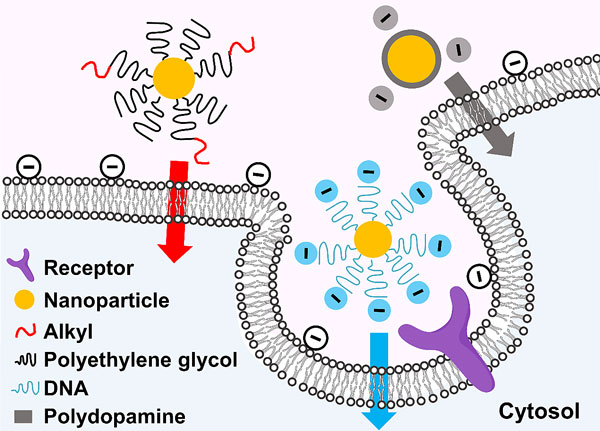
Acc. Chem. Res., 52, 6, 1519-1530 (2019)
为此,香港中文大学工程学院助理院长(学生事务)及生物医学工程系助理教授蔡宗衡,应邀在Accounts of Chemical Research 的「Nanomedicine and Beyond」特辑上撰写题为「Nano−Cell Interactions of Non-Cationic Bionanomaterials」的综述文章。文中,作者介绍了关于非带正电的生物纳米材料与细胞相互作用的研究,并引用了该课题组过往数年发表的文章。首先,作者以近中性电荷的聚乙二醇(polyethylene glycol)修饰的纳米粒子为平台,探索了两种鲜有被研究的物理化学参数对纳米粒子细胞摄取和胞内位置的影响:对细胞施加压力(compression)和对纳米粒子进行烷基化(alkylation)。接下来,作者报道了DNA修饰的纳米粒子和聚多巴胺(polydopamine)包裹的纳米粒子与细胞之间的相互作用。此两种带负电的生物纳米材料富有相当代表性,因为它们具有高效的细胞摄取率,并在过去十年获得广泛的生物医学应用,如基因工程调控、分子诊断、免疫调节、及体内影像引导的肿瘤光热治疗。作者不单探索了控制它们细胞摄取的蛋白和胞内运输途径,还定量分析了DNA修饰的纳米粒子于患病动物模型体内不同器官和组织中的细胞层面分布。这些基础结果提供了设计高效纳米粒子递送细胞的准则,甚至可以指导作者探索一些意料之外的纳米医学应用,例如利用DNA修饰的纳米粒子经静脉注射进入患心血管病动物的体内后靶向动脉粥样硬化斑块及斑块内的巨噬细胞,以及利用聚多巴胺包裹的「等离子体纳米虫」其吸收近红外光的特质来光热杀死癌细胞和其散射红光的特质进行无标记的暗场散射细胞成像。最后,作者简明扼要地阐述了对「纳米-生物相互作用」领域的展望,呼吁同侪关注把纳米粒子修饰不同官能团的角色,以及更精确地研究纳米粒子在细胞器层面上的分布和纳米粒子在体内分布的遗传基础。
综述文章内提及的研究工作获得研究资助局、香港博士研究生奖学金计划、信兴高等工程研究所、周毓浩创新医学技术中心、裘槎基金会以及裘槎前瞻科研大奖(Croucher Innovation Award)的资助。相关文章在线发表在Accounts of Chemical Research上,文章的第一作者是香港中文大学博士后研究学者何乐为(Lok Wai Cola Ho),其他作者为博士生刘瑶(Yao Liu)、韩瑞芳(Ruifang Han)和柏芊芊(Qianqian Bai),通讯作者为蔡宗衡(Chung Hang Jonathan Choi)。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nano-cell interactions of non-cationic bionanomaterials
Lok Wai Cola Ho, Yao Liu, Ruifang Han, Qianqian Bai, Chung Hang Jonathan Choi*
Acc. Chem. Res., 2019, 52, 6, 1519-1530, DOI: 10.1021/acs.accounts.9b00103
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号