压电纳米结构诱导干细胞神经分化
修复神经损伤一直是临床治疗中面临的巨大挑战。实现神经修复需要足够数量的神经元,然而,神经元作为一种高度分化的细胞,其增殖能力有限。因此,将干细胞诱导分化为神经元,进而进行细胞移植是解决这一问题的理想方案之一。在细胞微环境中,细胞外基质的生物物理特性,如微纳结构、硬度和生物电特性等,会对干细胞的黏附、增殖、迁移和分化等产生复杂的调控作用。因此,通过生物材料的结构、性能设计与调控,模拟干细胞的生理微环境,有望诱导干细胞的定向分化,实现组织修复方面的应用。
围绕电活性纳米生物材料的设计及对干细胞调控,中科院北京纳米能源与系统研究所李琳琳课题组和合作者在前期工作中开展了相关研究,发展了多种导电性生物支架并通过电刺激诱导、增强干细胞的定向分化(Appl. Mater Today, 2018, 10, 164;Adv. Bios. 2017, 1600042;ACS Nano2016, 10, 5086)。
在此基础上,近日,中科院北京纳米能源所李琳琳研究员(点击查看介绍)、王中林院士(点击查看介绍)、李舟研究员(点击查看介绍)通过对压电材料的微纳结构进行设计,使干细胞自身粘附、迁移产生的机械力牵引压电材料发生形变,产生表面压电势并反作用于细胞,诱导干细胞的神经样分化。为了提高细胞牵引力产生的压电材料形变和表面压电势,他们优化获得了两种尺度的聚偏二氟乙烯(PVDF)坑条阵列结构(高度,宽度和阵列间隔均为200 nm和高度,宽度和阵列间隔均为500 nm)(图1),综合探究了压电性和纳米结构两种特性对大鼠骨髓间充质干细胞的增殖、细胞黏着斑形成和细胞神经样分化的影响。通过对细胞牵引力诱发的压电电势进行了有限元模拟计算,细胞牵引力为10 nN时,纳米坑条阵列的压电薄膜可产生3.4 mV的压电势,足够对干细胞的行为活动产生影响(图2)。通过对细胞形貌、mRNA、蛋白表达的检测,发现了这一细胞粘附迁移——压电材料变形——产生压电势——反作用于细胞的途径可以有效地诱导、调控干细胞向神经样细胞进行分化(图3)。这一设计与发现为如何更加精确地设计纳米生物材料,调控干细胞的定向分化提供了新的思路。
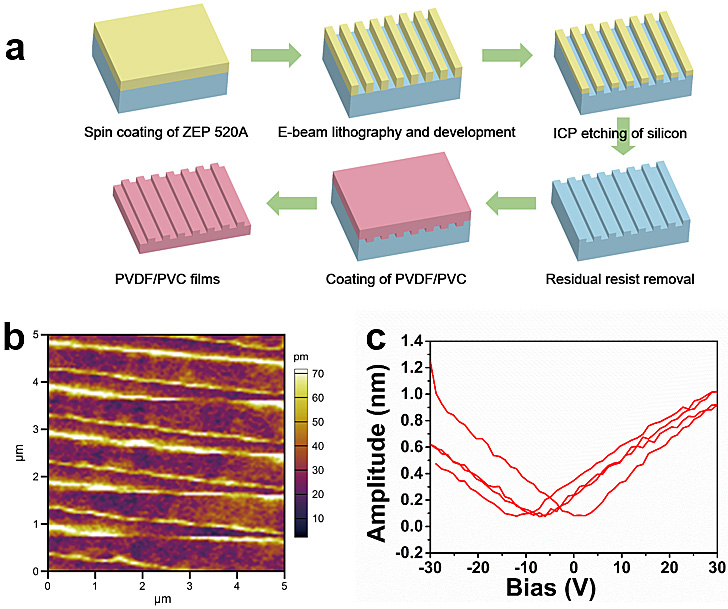
图1. 聚偏二氟乙烯(PVDF)坑条阵列结构制备流程及压电性表征
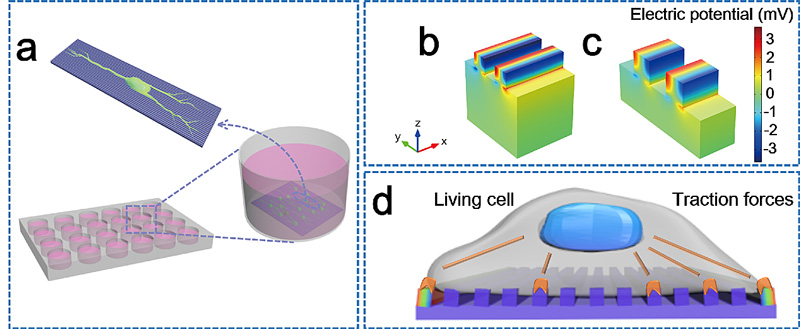
图2. 细胞牵引作用于坑条阵列结构产生压电势的有限元模拟计算
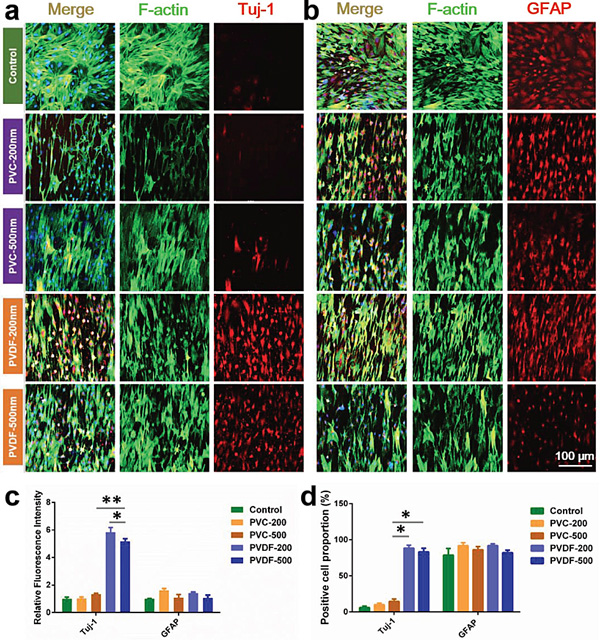
图3. 特异性神经标志物Tuj-1和GFAP的免疫荧光检测
相关研究成果发表在Adv. Funct. Mater.,中科院北京纳米能源所李琳琳研究员、王中林院士、李舟研究员为该文章的共同通讯作者;中科院北京纳米能源所的博士研究生张晓笛与中科院北京纳米能源所-广西大学联合培养博士生崔鑫为文章的并列第一作者;电子科技大学/中科院北京纳米能源所的张岩教授参与了压电势有限元模拟计算方面的工作。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Piezoelectric Nanotopography Induced Neuron-Like Differentiation of Stem Cells
Xiaodi Zhang, Xin Cui, Diancan Wang, Shu Wang, Zhirong Liu, Gengrui Zhao, Yan Zhang, Zhou Li,* Zhong Lin Wang,* Linlin Li*
Adv. Funct. Mater., 2019, DOI: 10.1002/adfm.201900372
导师介绍
李琳琳
https://www.x-mol.com/university/faculty/23493
王中林
https://www.x-mol.com/university/faculty/48479
李舟
https://www.x-mol.com/university/faculty/50126
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!









































 京公网安备 11010802027423号
京公网安备 11010802027423号