更小却更强——光声成像超小金纳米棒
光声成像(photoacoustic imaging, PAI)是近年来发展起来的一种基于光声效应的新型生物医学成像方法。在光声成像中,当非电离激光脉冲照射生物组织时,组织中的内源性分子(例如血红蛋白或黑色素)或者外源造影剂吸收光能,这种光学吸收与生理性质密切相关,并最终转换成携带该组织光吸收特征信息的超声信号,通过仪器检测和数据分析可以重建出2D或3D光吸收分布图像。这一技术综合了光学成像的高选择性和超声成像的深穿透性,可得到高分辨率和高对比度的组织图像。不过,由于生物大分子的自身性质,活体成像的背景往往会干扰对特定组织和细胞的观察。对于近红外光,生物组织产生最低背景信号的波长位于1000-1200纳米区间,也被称为第二近红外(second near-infrared, NIR-II)窗口。然而,在这个光谱范围内,少数几种可用的造影剂的大尺寸不利于它们的药代动力学,并降低了它们的热稳定性,导致光声成像不可靠。因此新型造影剂的研究迫在眉睫。
最近,美国斯坦福大学的Sanjiv Sam Gambhir研究团队和美国佐治亚理工学院的Stanislav Emelianov团队合作,报道了一种比传统尺寸小5-11倍的超小金纳米棒,展现出3倍稳定性和3.5倍光声成像信号强度。理论计算和数值分析表明,光声信号不仅与纳米颗粒溶液的光吸收成正比,而且与纳米颗粒的表面体积比成正比。在携带肿瘤的小鼠活体研究中,这些靶向超小金纳米棒的药物传递效率提高了30%,并光声对比度提高4.5倍。这一结果近期发表在Nature Nanotechnology 上。
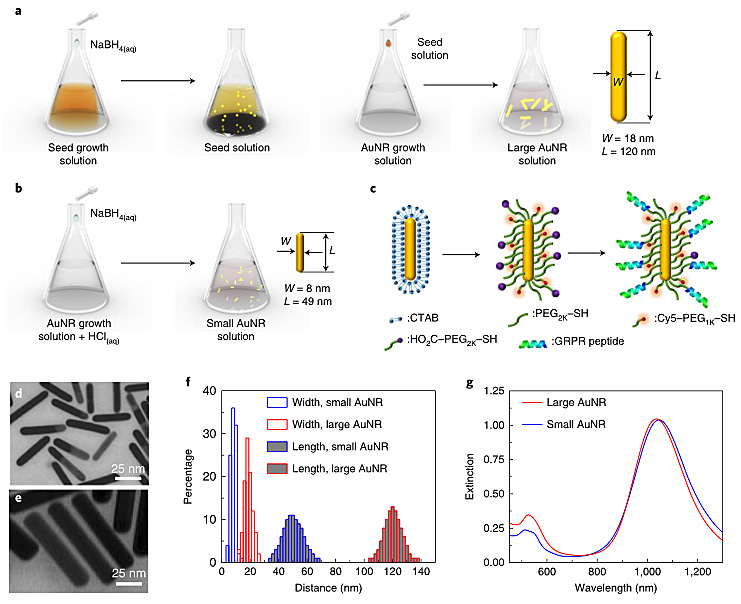
图1. (a-c)超小金纳米棒合成与表面修饰。(d-g)超小金纳米棒的表征。图片来源:Nat. Nanotech.
作者首先合成和表征了金纳米棒。使用传统的晶种法,一般会得到了长径比为6的产品,但其尺寸太大,一般为80-150纳米长,12-25纳米宽(图1a)。作者认为晶种是阻碍纳米棒变小的因素,他们加入高浓度强还原剂硼氢化钠,虽然可以缩小金纳米棒的尺寸,但往往得到的尺寸分布太宽(图1b)。另一方面,如果减小pH值到4以下,可以减小还原电势和减慢晶种生长速度,当pH小2时,纳米棒甚至会停止生长。因此,作者通过在金纳米棒生长过程中,控制硼氢化钠浓度和pH值,得到了宽8 ± 2纳米、长49 ± 8纳米的超小金纳米棒,并通过透射电镜等手段进行了表征(图1d-g)。
在高强度脉冲激光照射下,金纳米棒可能会被破坏,引起光声信号的光吸收变化和衰减。因此,在研究光声性能之前,测试这种超小金纳米棒的光损伤阈值非常关键。作者首先测试了不同光通量下,金纳米棒溶液的光声信号。他们发现,在光通量低于6.1 mJ cm-2时,普通的大尺寸金纳米棒(宽18 ± 4纳米、纳米120 ± 17纳米)和超小金纳米棒的光声信号没有衰减(图2a)。然而,当光通量达于18.2 mJ cm-2时,200次脉冲后,普通金纳米棒衰减了42%,而超小金纳米棒只衰减了10%(图2b)。扫描电镜图像(图2c-f)证实,在光通量为20 mJ cm-2照射下,大多数超小金纳米棒仍然可以保持其形状,而超过65%的普通金纳米棒会发生变形。接着,作者测试了金纳米棒溶液的光声信号。超小金纳米棒产生的光声信号强度比光密度(optical density)匹配的普通金纳米棒高约3.5倍,并且至少比补偿后的普通金纳米棒的吸收高2倍(图2g-i)。
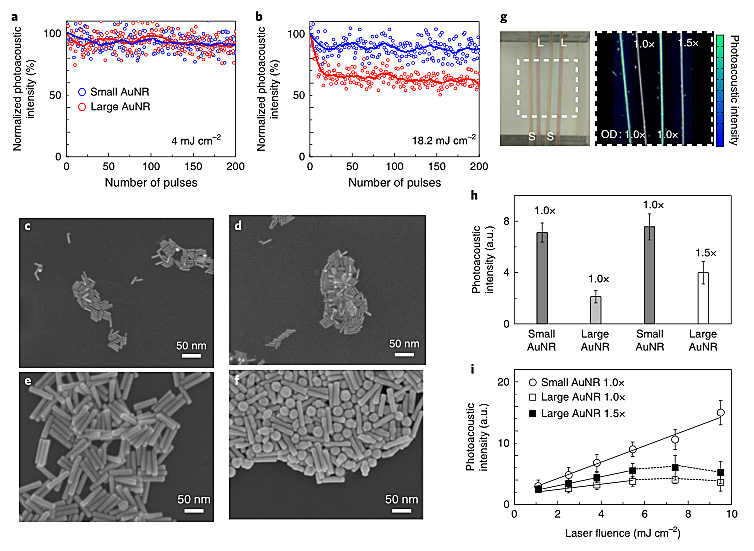
图2. 光声信号衰减和强度测试。图片来源:Nat. Nanotech.
作者接着解释了这一跟传统光声学理论所预测结果相悖的现象。传统光声学理论认为光声信号振幅是Grüneisen系数、吸收系数和局部光通量的乘积。然而,这种关系只有在激光脉冲波长足够短以至于热和应力不能从光吸收体区域逃逸的假设下才成立。而在纳米颗粒溶液中,光主要被纳米颗粒吸收,而不是被溶剂吸收。声信号由时间依赖性的热泄漏,由金纳米棒到水的热传递速率决定。在作者的光声实验中,大小尺寸金纳米棒溶液之间的唯一区别是溶液中金纳米棒的总表面体积比不同(浓度一致),其随着金纳米棒尺寸的减小而增大。因此,作者假设光声信号的增强源于超小金纳米棒的表面体积比的增加,这促进了热传递。为了验证这一的假设,他们从理论上研究了光声信号的产生(图3)。计算表明,理论上超小金纳米棒比普通金纳米棒的光声效率要高约2倍。
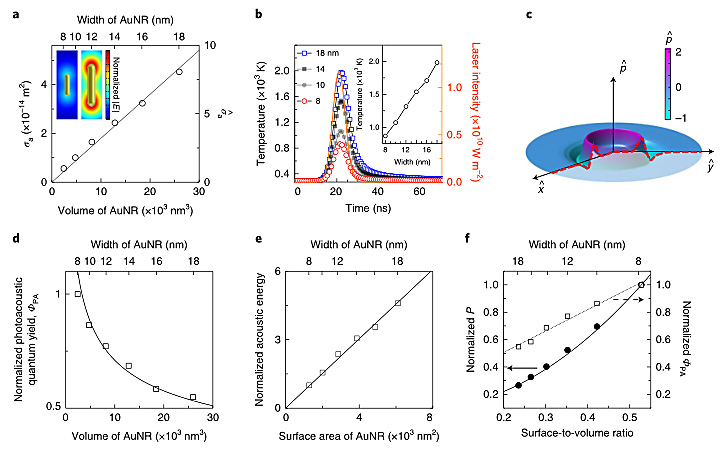
图3. 光声量子产率的理论计算。图片来源:Nat. Nanotech.
为了表征金纳米棒的靶向特异性,作者用GRPR靶向肽和Cy5染料对金纳米棒进行了功能化修饰(图1c)。接着他们通过Zeta-电势测试了表面电荷(图4a),并且测试了修饰后的金纳米棒荧光强度,证明其适合生物成像(图4b)。通过共聚焦荧光显微镜,他们观察了金纳米棒对于PC-3细胞(有GRPR受体)和DU-145细胞(无GRPR受体)的细胞定位。结果只有GRPR受体的PC-3细胞中可以观察到Cy-5染料的荧光(图4c和图4g),证明有金纳米棒进入细胞。而无GRPR受体的DU-145细胞中没有观察到这一现象(图4d-4h)。这说明GRPR修饰的金纳米棒具有靶向特异性。
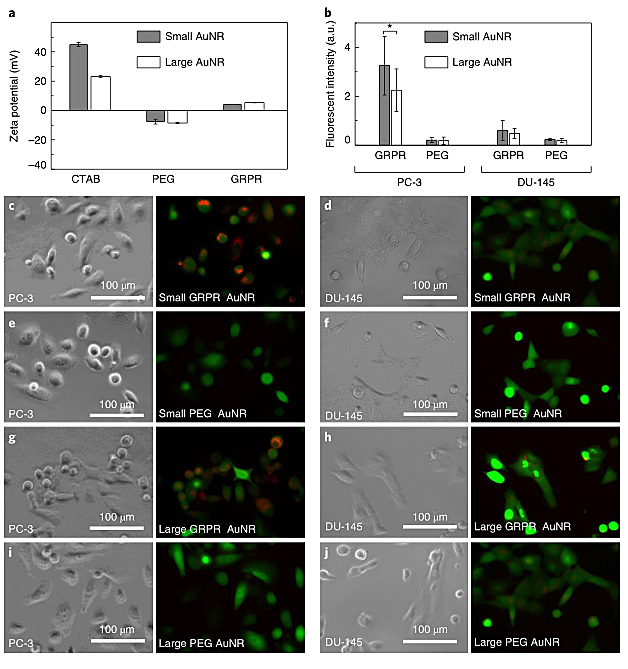
图4. 细胞实验和成像。图片来源:Nat. Nanotech.
为了验证金纳米棒能够作为光声分子成像剂,作者使用小鼠前列腺癌模型进行了体内光声成像。靶向超小金纳米棒的信号强度(图5d)明显高于靶向普通金纳米棒(图5c),而无靶向的两种金纳米棒差别并不显著(图5a-b),这显示了靶向超小金纳米棒具有更高的肿瘤穿透率和肿瘤结合特异性。有趣的是,靶向普通金纳米棒的信号衰减很明显,再次验证了过大尺寸的金纳米棒的热不稳定性,而超小金纳米棒则没有明显的信号衰减。荧光信号分析表明,靶向超小金纳米棒主要集中在肿瘤和肝脏,具有良好药代动力学和高度靶向特异性,其信号强度几乎是靶向普通金纳米棒和非靶向金纳米棒的两倍。
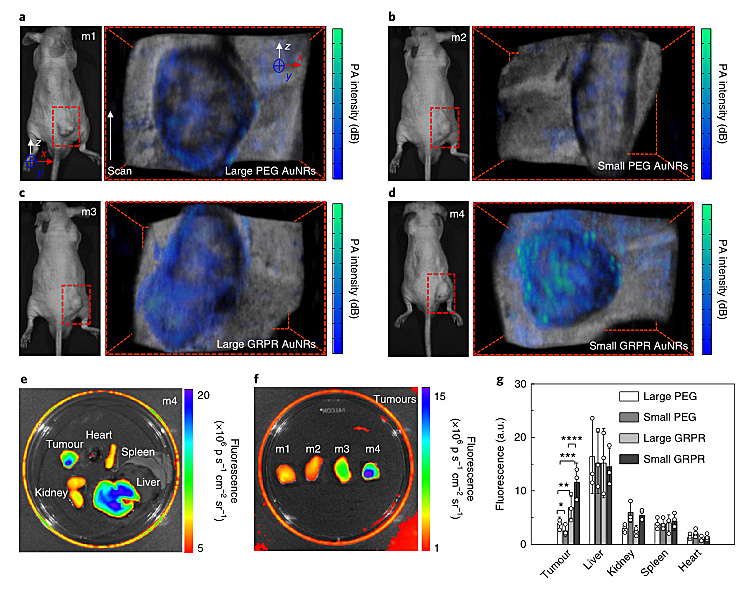
图5. 活体成像实验。图片来源:Nat. Nanotech.
总结
作者合成了一种超小金纳米棒光声造影剂,它能够在NIR-II窗口有光吸收并产生稳定、高强度的光声信号,用于体内成像研究。更重要的是,他们证明了这种反常的现象是基于光声信号强度与纳米颗粒的表面体积比相关。这些发现为未来光声造影剂的设计提供了一个新的策略,并可能在NIR-II窗口启发更多的光声分子成像应用。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Miniature gold nanorods for photoacoustic molecular imaging in the second near-infrared optical window
Yun-Sheng Chen, Yang Zhao, Soon Joon Yoon, Sanjiv Sam Gambhir, Stanislav Emelianov
Nat. Nanotech., 2019, DOI: 10.1038/s41565-019-0392-3
导师介绍
Sanjiv Sam Gambhir
https://www.x-mol.com/university/faculty/54964
(本文由叶舞知秋供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号